Clear Sky Science · fr
Lgmn cible deux RCPG distincts, PAR2 et µ-OR1, et induit la mort cellulaire dans la leucémie lymphoblastique aiguë via un déséquilibre intracellulaire en Ca²⁺ déclenché par la libération de Ca²⁺ du RE
Comment une enzyme parasite pourrait aider à combattre la leucémie pédiatrique
La leucémie lymphoblastique aiguë (LLA) est le cancer du sang le plus fréquent chez l’enfant ; bien que les traitements actuels puissent en guérir beaucoup, ils s’accompagnent souvent d’effets secondaires sévères et d’un risque de rechute. Dans un retournement inattendu, des chercheurs étudiant une protéine utilisée par des parasites intestinaux courants pour attaquer les cellules humaines ont découvert que cette même molécule peut pousser sélectivement les cellules leucémiques vers l’autodestruction. En retraçant comment cette protéine perturbe l’équilibre du calcium à l’intérieur des cellules cancéreuses, l’étude met en lumière de nouvelles façons d’éliminer les cellules leucémiques tout en suggérant de nouvelles cibles médicamenteuses.
Une arme cachée provenant de parasites courants
Le travail porte sur la légumain, une enzyme sécrétée par des protozoaires intestinaux et urogénitaux tels que Blastocystis et Trichomonas. Ces parasites utilisent la légumain comme partie de leur arsenal pour envahir et endommager les tissus hôtes. Des recherches antérieures ont montré que la légumain peut cliver un récepteur sur les cellules humaines connu sous le nom de PAR2 et, ce faisant, déclencher une élévation du calcium intracellulaire. Mais même lorsque PAR2 était supprimé ou rendu résistant au clivage, la légumain parvenait encore à augmenter les niveaux de calcium, ce qui implique l’existence d’un autre déclencheur. Comme un médicament largement utilisé contre la leucémie, l-asparaginase, agit aussi sur PAR2 et sur un second récepteur appelé µ-OR1, les auteurs se sont demandé si la légumain n’utiliserait pas également plusieurs voies pour perturber la vie intérieure des cellules leucémiques.
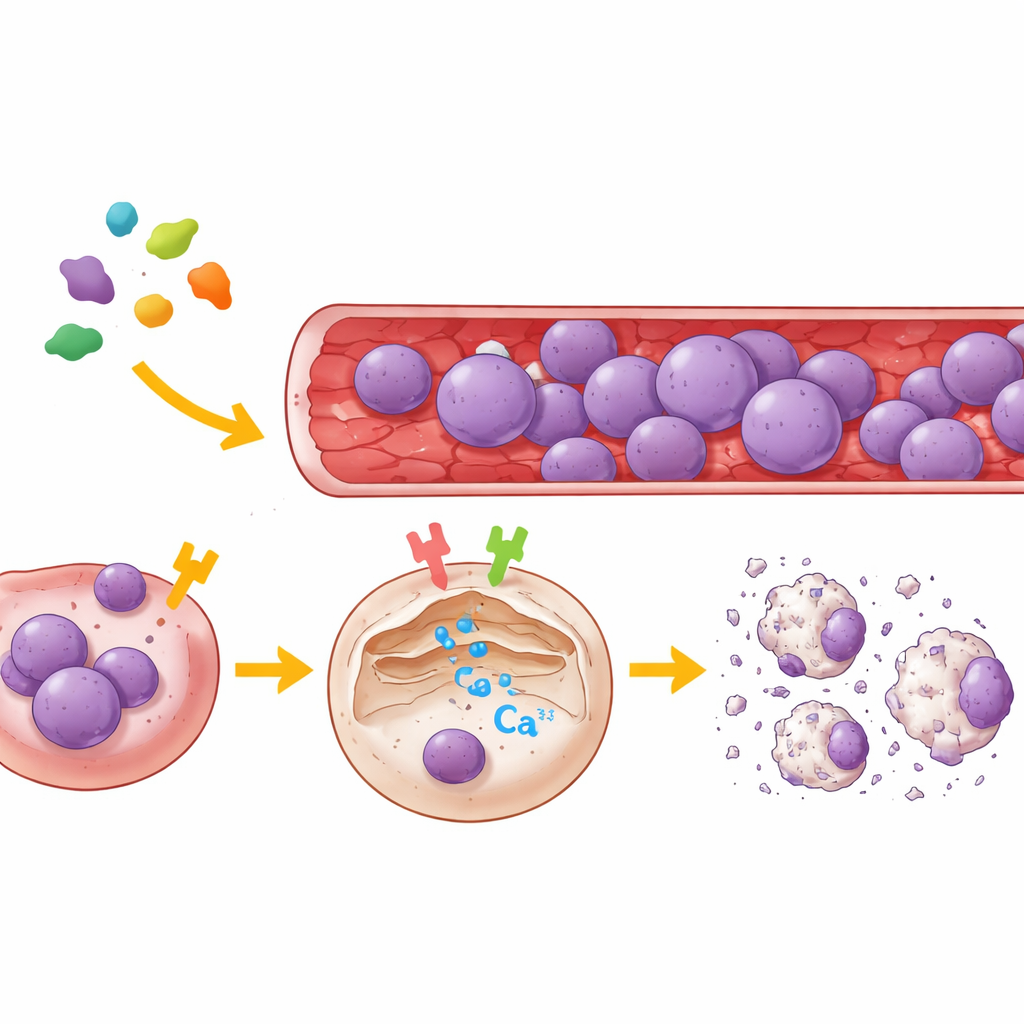
Deux interrupteurs cellulaires qui contrôlent le calcium
Pour cartographier les cibles de la légumain, l’équipe a utilisé à la fois des cellules rénales humaines et plusieurs types de cellules de LLA provenant de patients. Ils ont réduit sélectivement soit PAR2 soit µ-OR1 dans ces cellules, ou les ont bloqués avec des inhibiteurs petites molécules très spécifiques, puis ont observé les mouvements de calcium dans des cellules individuelles à l’aide d’une sonde fluorescente qui rend compte de la libération de calcium depuis le réticulum endoplasmique, la principale réserve interne de calcium de la cellule. Les résultats étaient clairs : la légumain provoquait une forte libération de calcium depuis cette réserve seulement lorsqu’au moins un des deux récepteurs était actif. L’inhibition de µ-OR1 atténuait fortement la poussée calcique, tandis que le blocage de PAR2 produisait une réduction plus faible mais notable. Lorsque les deux récepteurs étaient désactivés, la légumain ne pouvait plus provoquer la libération de calcium. Dans plusieurs lignées leucémiques B et T, µ-OR1 s’est révélée être l’interrupteur dominant, PAR2 jouant un rôle de soutien.
Des signaux déréglés font basculer les cellules vers la mort
Après avoir établi que la légumain cible les deux récepteurs, les chercheurs ont suivi les cascades de signalisation qui relient ces interrupteurs de surface aux événements profonds à l’intérieur de la cellule. PAR2 se couple à une protéine G qui active directement une enzyme appelée PLC, laquelle à son tour ouvre les « vannes » calciques sur le réticulum endoplasmique. µ-OR1, en revanche, signale principalement via une autre protéine G qui réduit la production du messager cAMP et calme ainsi une enzyme connue sous le nom de protéine kinase A (PKA). Normalement, la PKA impose des « freins » inhibiteurs sur la PLC et maintient l’activité d’une protéine de survie appelée BAD dans un état non létal. Lorsque la légumain stimule µ-OR1, les niveaux de cAMP chutent, l’activité de la PKA diminue, ces freins sont relâchés, et la PLC est libre de libérer davantage de calcium des réserves. Parallèlement, BAD bascule vers une forme qui affaiblit les défenses intrinsèques de la cellule contre la mort.
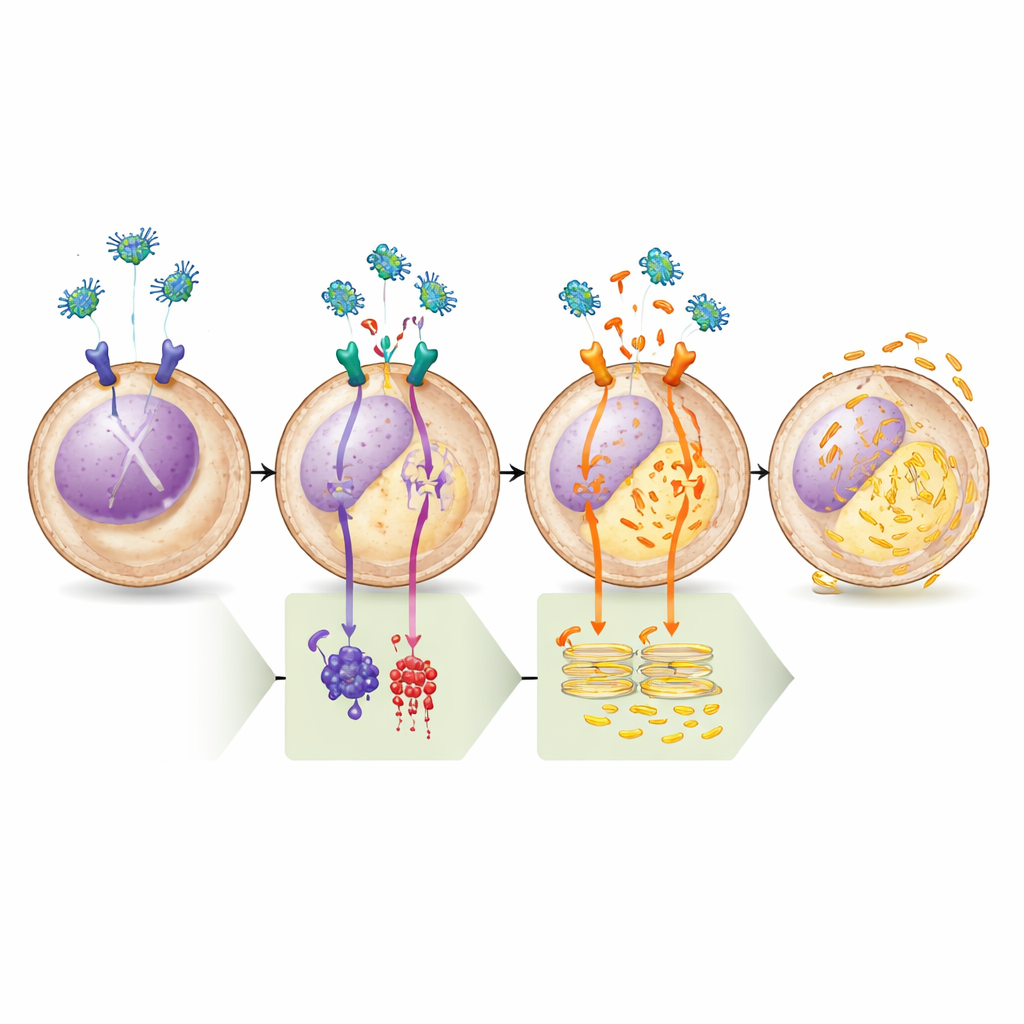
Vérifier la voie pas à pas
L’équipe a validé ce modèle par une série de tests pharmacologiques. Des médicaments qui augmentent le cAMP ou activent directement l’enzyme qui le produit (adénylate cyclase) bloquaient complètement la capacité de la légumain à vider le calcium du réticulum endoplasmique, soulignant l’importance du bras µ-OR1–cAMP–PKA. À l’inverse, un inhibiteur de la PKA hautement sélectif à lui seul suffisait à déclencher la libération de calcium, et l’ajout ultérieur de légumain n’entraînait aucun effet supplémentaire, montrant qu’une fois la PKA désactivée, la voie est déjà pleinement engagée. Des analyses biochimiques ont confirmé que le traitement par la légumain réduisait les « étiquettes » de phosphate sur la PLC et BAD à des sites connus pour être contrôlés par la PKA, correspondant au changement d’activité prédit. Enfin, lorsque les chercheurs ont bloqué le canal calcique du réticulum endoplasmique ou supprimé une protéine d’échafaudage clé requise pour ce canal, la légumain n’induisait plus la mort cellulaire, reliant fermement l’issue létale au déséquilibre calcique.
Ce que cela pourrait signifier pour les traitements futurs de la leucémie
Au terme de cette cascade de signalisation, les cellules leucémiques subissent un afflux soutenu de calcium depuis leurs réserves internes, couplé à l’arrêt d’un circuit de survie critique. Ensemble, ces changements poussent les cellules vers la mort programmée, ou apoptose. Pour le lecteur non spécialiste, le message est que la légumain agit comme un saboteur à deux mains : elle enfonce simultanément les deux « boutons d’activation » de la libération calcique tout en coupant les fils de ses systèmes de sécurité. Bien que la légumain elle-même provienne de parasites et nécessiterait une évaluation rigoureuse avant toute utilisation thérapeutique, l’étude met en évidence µ-OR1, PAR2 et la PKA comme des cibles médicamenteuses prometteuses. Des médicaments qui miment la perturbation sélective de l’équilibre calcique par la légumain dans les cellules leucémiques — ou qui inhibent stratégiquement la PKA — pourraient un jour aider à traiter des patients dont les cancers résistent aux thérapies actuelles.
Citation: Lee, J.K., Riabowol, K. & Lee, KY. Lgmn targets two distinct GPCRs, PAR2 and µ-OR1, and induces cell death in acute lymphoblastic leukemia through an intracellular Ca²⁺ imbalance triggered by ER Ca²⁺ release. Cell Death Discov. 12, 143 (2026). https://doi.org/10.1038/s41420-026-03003-3
Mots-clés: leucémie lymphoblastique aiguë, légumain, signalisation calcique, récepteurs couplés aux protéines G, apoptose