Clear Sky Science · tr
REDD1/DDIT4, endoplazmik retikulum kaynaklı strese bağlı apoptozu TRAILR2/DR5 ölüm reseptörünün ifadesini kontrol ederek engelliyor
Neden stres altındaki tümör hücreleri önemli?
Kanser hücreleri konfor içinde büyümez. Bir tümör içinde hücreler düşük oksijen, sınırlı besin ve hasarlı protein birikimiyle karşılaşır. Bu baskı altında bazı hücreler ölürken, diğerleri uyum sağlar ve tedaviye karşı daha dirençli hale gelir. Bu makale, kolon kanseri hücrelerinin hücresel bir iç stres türü — protein katlanma fabrikası olan endoplazmik retikulumdaki aksaklık — ile nasıl başa çıktığını inceliyor ve bu stresli hücrelerin kendi kendini yok etmesini engelleyen moleküler bir “fren”i tanımlıyor.
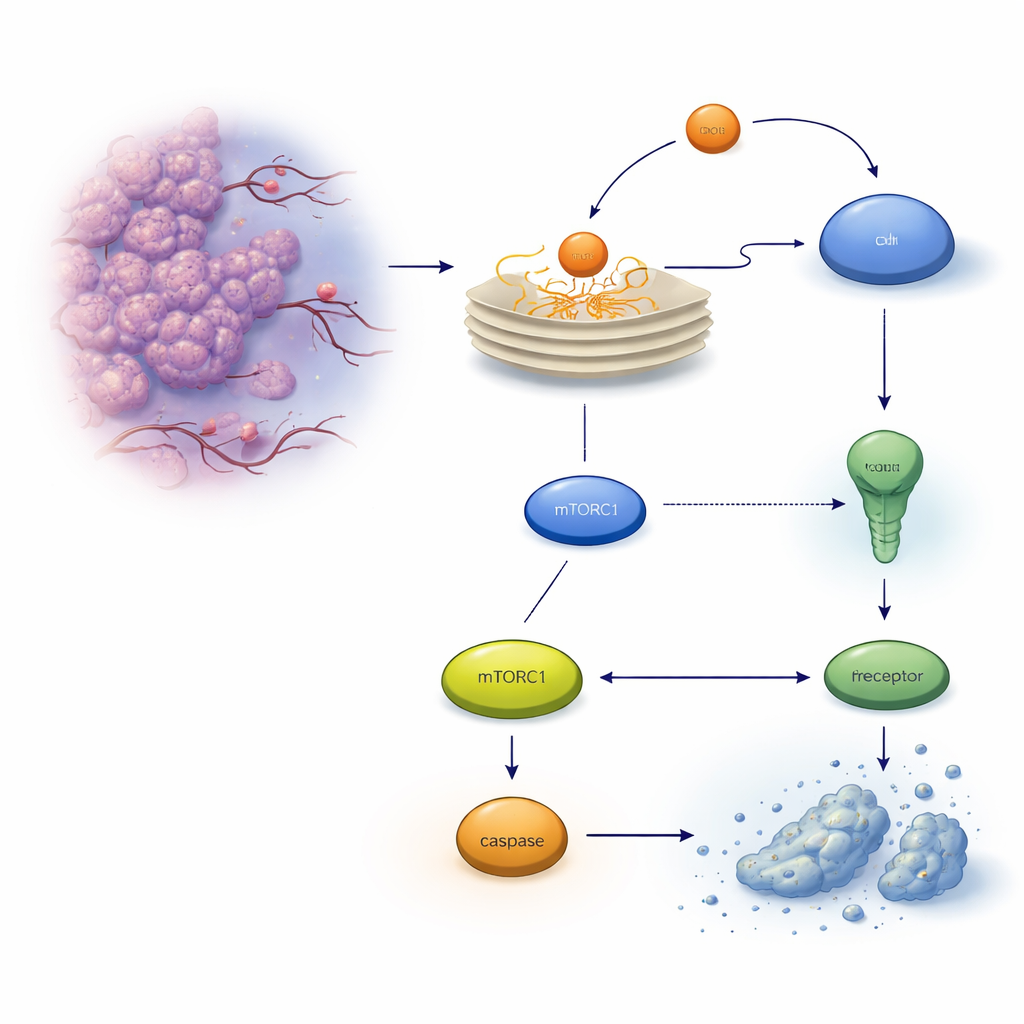
Tümör hücrelerinin içindeki gizli bir emniyet valfi
Proteinler düzgün katlanmadığında endoplazmik retikulumda (ER) birikir ve yanlış katlanmış proteinlere yanıt olarak katlanmamış protein yanıtı (UPR) adı verilen bir alarm sistemi başlatılır. İlk aşamada bu yanıt dengeyi yeniden kurmaya çalışır, ancak stres çok güçlü veya uzun sürerse, bu yanıt apoptoz olarak bilinen bir kendini yok etme programına dönüşebilir. Kolon kanseri hücrelerinde önemli yürütücülerden biri hücre yüzeyindeki TRAILR2/DR5 adlı ölüm reseptörüdür; bu reseptör kaspaz‑8 adlı bir proteazı aktive ederek hücre ölümüne yol açabilir. Yazarlar, zor koşullara uyum sağlamaya yardımcı olduğu bilinen başka bir stresle indüklenen protein olan REDD1/DDIT4 üzerine odaklanmış ve bu proteinin yaşam‑ve‑ölüm kararını etkileyip etkilemediğini araştırmışlar.
Bir stres proteini hayatta kalma lehine nasıl dengeleri kaydırıyor
Araştırmacılar insan kolon kanseri hücre hatlarını ER stresi oluşturan ilaçlara maruz bıraktı ve zaman içinde REDD1 düzeylerini izledi. ER stresinin ATF4 adlı başka bir stres yanıt faktörü tarafından düzenlenen düzenli bir süreçle REDD1 üretimini hızla artırdığını buldular. REDD1 bulunduğunda, büyüme ve protein sentezinin ana düzenleyicilerinden biri olan mTORC1 aktivitesini zayıflattı. RNA müdahalesi veya CRISPR gen düzenlemesiyle REDD1’i baskılamak ya da silmek, kanser hücrelerini ER stresi altında apoptoza çok daha yatkın hale getirdi; bu ek hücre ölümünü kaspaz inhibitörleri veya farmakolojik olarak mTORC1’in kapatılmasıyla engellemek mümkündü; bu da REDD1’in normalde stresteyken bu büyüme yolu üzerinde baskı kurarak hücreleri koruduğunu gösteriyor.
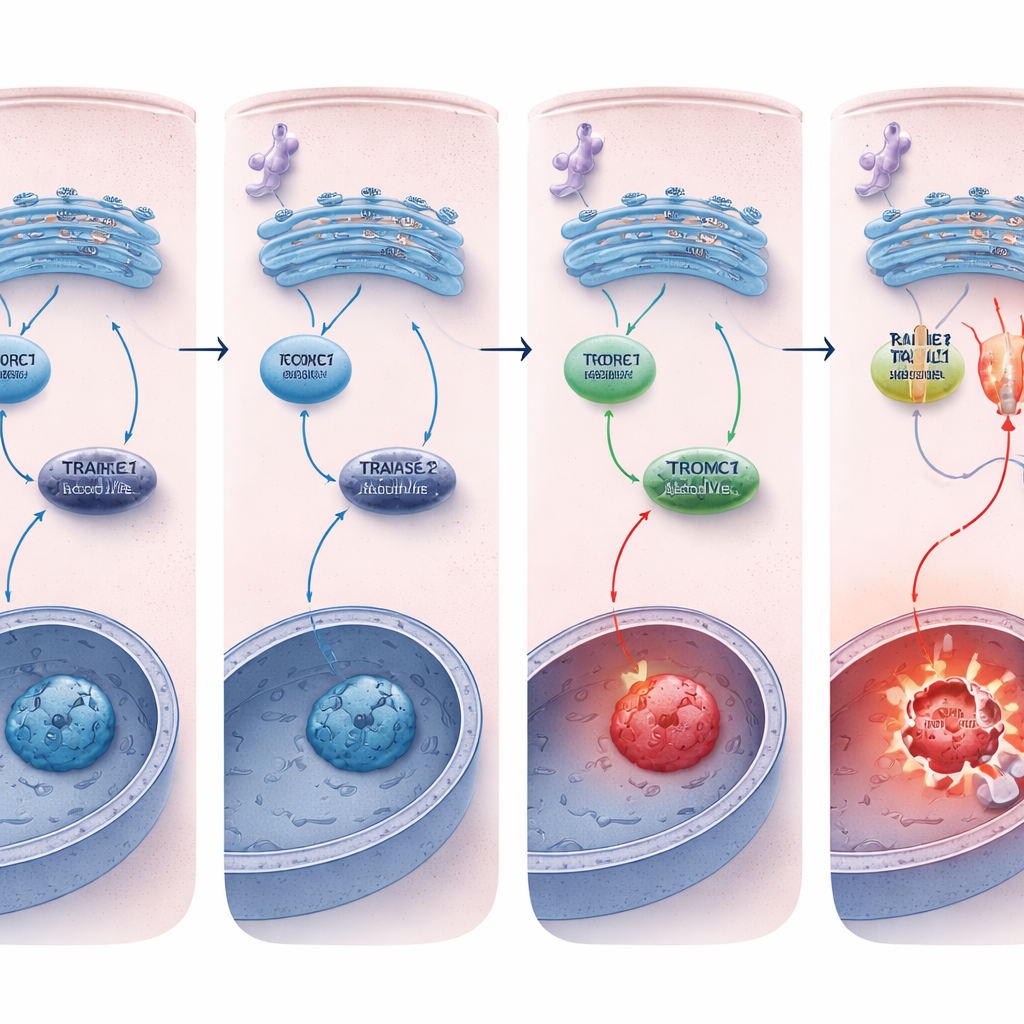
Ölüm anahtarını kapalı tutmak
REDD1 eksik hücrelerin neden daha kolay öldüğü sorusu vardı. Ana fark TRAILR2/DR5 ölüm reseptöründeydi. Kronik ER stresi altında hem normal hem de REDD1 eksik hücreler yukarı akış stres yollarını benzer şekilde aktive etti, ancak REDD1 eksik hücrelerde TRAILR2/DR5’in hem RNA hem de protein düzeyinde çok daha büyük bir artış gösterdiği ve bunun kaspaz‑8’in daha güçlü aktivasyonuyla birlikte olduğu görüldü. TRAILR2/DR5’in susturulması, ilgili başka bir reseptörün susturulmasının aksine, bu REDD1 eksik hücrelerde apoptozu önemli ölçüde azalttı; bu da artan ölüm yanıtının başlıca olarak bu reseptör aracılığıyla yönlendirildiğini kanıtlıyor. Gerçek tümörleri daha iyi taklit eden ve doğal olarak stres biriktiren üç boyutlu tümör sferoidlerinde REDD1 düzeyleri zaten yüksekti ve mTORC1 aktivitesi düşüktü; REDD1’in ortadan kaldırılması bu mini‑tümörleri tekrar ER stresiyle tetiklenen hücre ölümüne karşı çok daha savunmasız hale getirdi.
Transkripsiyonel bir frenin rolü
REDD1’in TRAILR2/DR5’i nasıl kontrol ettiğini anlamak için ekip, REDD1 kaybında düzeyi değişen düzenleyicileri aramak üzere RNA dizilemesi kullandı. Kanser büyümesi ve gen baskılanmasıyla daha önce ilişkilendirilmiş EVI‑1/MECOM adlı bir transkripsiyon faktörünü saptadılar. REDD1 eksik hücrelerde EVI‑1/MECOM düzeyleri düştü. EVI‑1/MECOM’u normal hücrelerde azaltmak, hücreleri ER stresine daha duyarlı hale getirdi, TRAILR2/DR5 ifadesini artırdı ve kaspaz‑8‑bağımlı apoptozu tetikleyerek REDD1 kaybının etkisini taklit etti. Yazarlar ayrıca bazı tümörlerde EVI‑1/MECOM’un bilinen ortakları olan CtBP1/2 adlı ko‑baskılayıcıların, hücre tipine özgü şekilde TRAILR2/DR5 düzeylerini ve stres duyarlılığını daha da ayarlayabileceğini buldular. Birlikte bu bulgular REDD1’in TRAILR2/DR5 geninin EVI‑1/MECOM temelli baskılanmasını sürdürmeye yardımcı olduğunu ve uzun süren stres sırasında ölüm anahtarının etkinleşmesini geciktirdiğini gösteriyor.
Gelecekteki kanser tedavileri için ne anlama geliyor?
Halkın anlayacağı şekilde ana çıkarım, kolon kanseri hücrelerinin şiddetli protein stresini “atlatmalarına” izin veren içsel bir mekanizmaya sahip olmalarıdır; yani olması gerektiği zamanda ölmek yerine hayatta kalabiliyorlar. REDD1 bir emniyet valfi gibi davranır: önemli bir büyüme yolunu sakinleştirir ve güçlü bir ölüm reseptörü olan TRAILR2/DR5’in gereğinden erken açılmasını engelleyen bir gen‑baskılama sistemini destekler. REDD1 veya ortaklarından EVI‑1/MECOM uzaklaştırıldığında, stres altındaki kanser hücreleri kendilerini yok etmeye çok daha yatkın hale gelir. Bu çalışma, REDD1’i veya onun aşağı akış baskılayıcılarını hedeflemenin, tümörlerin bu koruyucu tamponunu ortadan kaldırarak, tümörün zorlu ve besinsiz bölgelerindeki kanser hücrelerini ER stresini artıran ve hücreleri apoptoza iten tedavilere karşı daha hassas hale getirebileceğini düşündürmektedir.
Atıf: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Anahtar kelimeler: ER stresi, kolorektal kanser, apoptoz, TRAILR2/DR5, REDD1/DDIT4