Clear Sky Science · fr
REDD1/DDIT4 contrecarre l'apoptose induite par le stress du réticulum endoplasmique en contrôlant l'expression du récepteur de mort TRAILR2/DR5 dans les cellules cancéreuses
Pourquoi les cellules tumorales stressées importent
Les cellules cancéreuses ne croissent pas dans le confort. À l'intérieur d'une tumeur, les cellules font face à un faible apport en oxygène, à des nutriments rares et à une accumulation de protéines endommagées. Sous cette pression, certaines cellules meurent, mais d'autres s'adaptent et deviennent plus difficiles à éliminer par les traitements. Cet article explore comment les cellules du cancer du côlon survivent à un type spécifique de stress interne — des perturbations du réticulum endoplasmique, l'usine de repliement des protéines de la cellule — et identifie un « frein » moléculaire qui empêche ces cellules stressées de s'autodétruire.
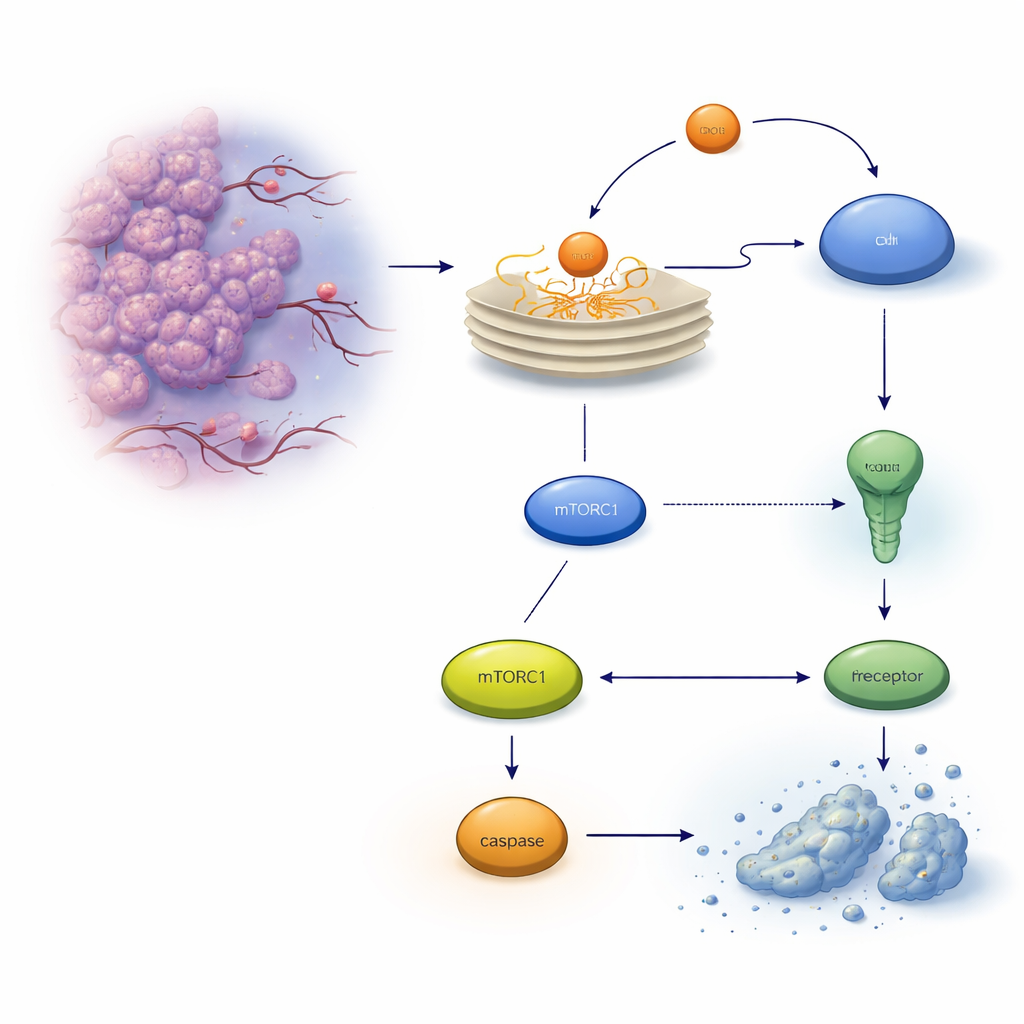
Une soupape de sécurité cachée à l'intérieur des cellules tumorales
Lorsque les protéines ne sont pas correctement repliées, elles s'accumulent dans le réticulum endoplasmique (RE), déclenchant un système d'alarme appelé réponse aux protéines mal repliées. Au départ, cette réponse tente de rétablir l'équilibre, mais si le stress est trop intense ou persiste, elle peut basculer en un programme d'autodestruction connu sous le nom d'apoptose. Dans les cellules du cancer du côlon, un exécuteur clé est un récepteur de mort à la surface cellulaire appelé TRAILR2/DR5, qui peut activer une enzyme découpeuse de protéines, la caspase-8, et finalement tuer la cellule. Les auteurs se sont concentrés sur une autre protéine induite par le stress, REDD1/DDIT4, déjà connue pour aider les cellules à s'adapter à des conditions difficiles, et ont cherché à savoir si elle influence cette décision de vie ou de mort.
Comment une protéine de stress incline la balance vers la survie
Les chercheurs ont exposé des lignées cellulaires humaines de cancer du côlon à des médicaments provoquant le stress du RE et ont suivi les niveaux de REDD1 au fil du temps. Ils ont constaté que le stress du RE augmentait rapidement la production de REDD1 selon une dynamique ordonnée contrôlée par un autre facteur inductible par le stress, ATF4. Lorsque REDD1 était présent, il diminuait l'activité de mTORC1, un régulateur majeur de la croissance et de la synthèse protéique. L'inhibition ou la suppression de REDD1 par interférence ARN ou modification génomique CRISPR rendait les cellules cancéreuses beaucoup plus susceptibles de subir l'apoptose sous stress du RE, et cette surmortalité cellulaire pouvait être empêchée par des inhibiteurs de caspases ou par l'inhibition pharmacologique de mTORC1, montrant que REDD1 protège normalement les cellules en retenant cette voie de croissance pendant le stress.
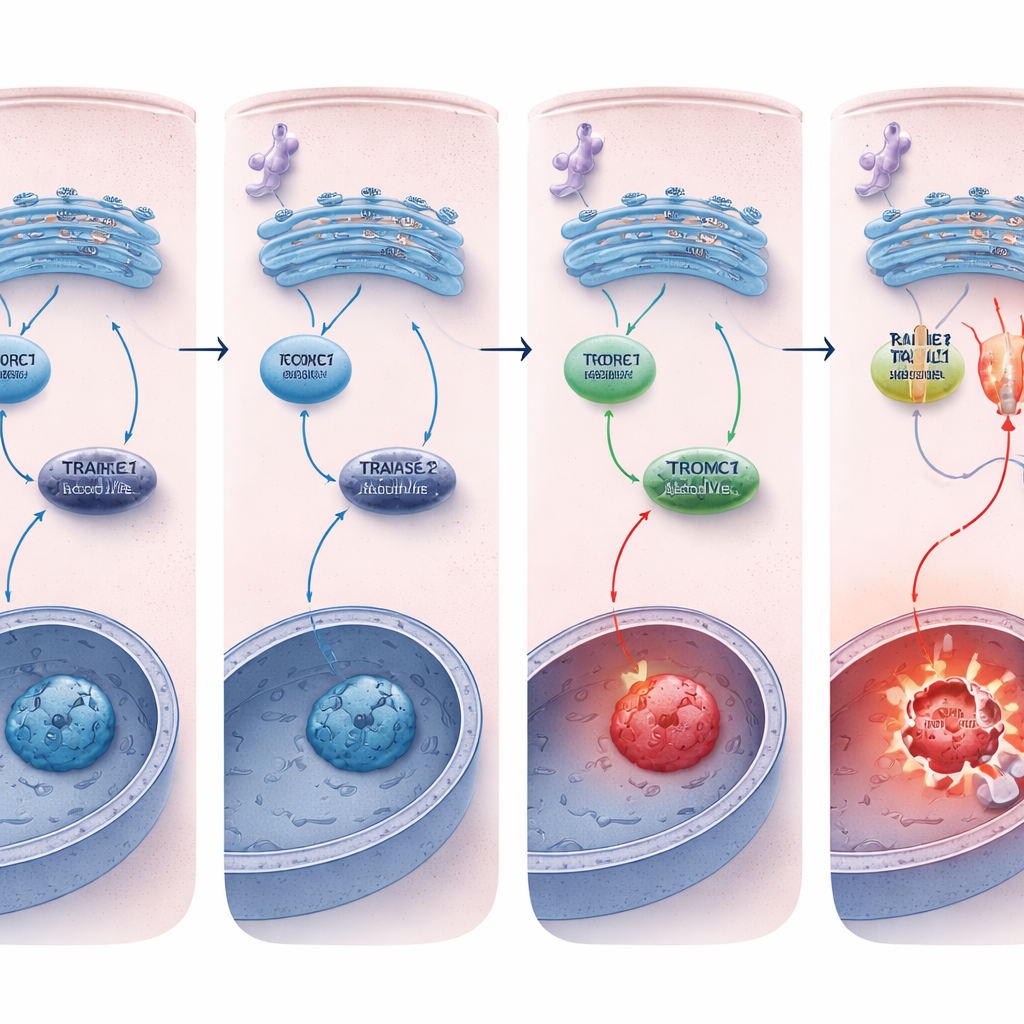
Maintenir l'interrupteur de la mort réglé bas
Pourquoi les cellules déficientes en REDD1 mouraient-elles plus facilement ? La différence clé résidait dans le récepteur de mort TRAILR2/DR5. Sous stress chronique du RE, les cellules normales et déficientes en REDD1 activaient de manière comparable les voies de stress en amont, mais les cellules sans REDD1 montraient une augmentation beaucoup plus importante de TRAILR2/DR5 au niveau de l'ARN et de la protéine, accompagnée d'une activation plus forte de la caspase-8. L'extinction de TRAILR2/DR5, mais pas d'un récepteur apparenté, réduisait fortement l'apoptose dans ces cellules déficientes en REDD1, prouvant que la réponse de mort amplifiée était principalement conduite par ce récepteur. Dans des sphéroïdes tumoraux tridimensionnels, qui imitent mieux les tumeurs réelles et accumulent naturellement le stress, les niveaux de REDD1 étaient déjà élevés et l'activité de mTORC1 faible, et la suppression de REDD1 rendait à nouveau ces mini-tumeurs beaucoup plus vulnérables à la mort cellulaire induite par le stress du RE.
Le rôle d'un frein transcriptionnel
Pour comprendre comment REDD1 contrôle TRAILR2/DR5, l'équipe a utilisé le séquençage d'ARN pour rechercher des régulateurs dont les niveaux changeaient lorsque REDD1 était perdu. Ils ont identifié un facteur de transcription appelé EVI-1/MECOM, précédemment associé à la croissance tumorale et à la répression génique. Dans les cellules déficientes en REDD1, les niveaux d'EVI-1/MECOM diminuaient. La réduction d'EVI-1/MECOM dans des cellules par ailleurs normales les rendait plus sensibles au stress du RE, augmentait l'expression de TRAILR2/DR5 et déclenchait une apoptose dépendante de la caspase-8, reproduisant l'effet de la perte de REDD1. Les auteurs ont également observé que des corépresseurs appelés CtBP1/2, partenaires connus d'EVI-1/MECOM dans certains cancers, pouvaient moduler davantage les niveaux de TRAILR2/DR5 et la sensibilité au stress de façon spécifique au type cellulaire. Ensemble, ces résultats suggèrent que REDD1 contribue à maintenir la répression du gène TRAILR2/DR5 par le biais d'EVI-1/MECOM, retardant l'activation de l'interrupteur de la mort pendant un stress prolongé.
Ce que cela signifie pour les traitements du cancer à venir
Pour un public non spécialisé, la conclusion principale est que les cellules du cancer colorectal possèdent un mécanisme interne qui leur permet de « traverser » un stress protéique sévère au lieu de mourir quand elles le devraient. La protéine REDD1 agit comme une soupape de sécurité : elle calme une voie de croissance majeure et soutient un système de répression génique qui empêche l'activation prématurée d'un puissant récepteur de mort, TRAILR2/DR5. Lorsque REDD1 ou son partenaire EVI-1/MECOM sont supprimés, les cellules cancéreuses stressées ont beaucoup plus tendance à s'autodétruire. Ce travail suggère que cibler REDD1 ou ses répressseurs en aval pourrait dépouiller les tumeurs de cette protection, rendant les cellules tumorales situées dans des régions pauvres en ressources plus vulnérables aux thérapies qui augmentent le stress du RE et poussent les cellules vers l'apoptose.
Citation: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Mots-clés: stress du RE, cancer colorectal, apoptose, TRAILR2/DR5, REDD1/DDIT4