Clear Sky Science · nl
REDD1/DDIT4 tegengaat endoplasmatisch reticulum-stressgeïnduceerde apoptose door de expressie van de doodsreceptor TRAILR2/DR5 in kankercellen te beheersen
Waarom gestreste tumorcellen ertoe doen
Kankercellen groeien niet in comfortabele omstandigheden. Binnen een tumor ervaren cellen lage zuurstof, schaarse voedingsstoffen en een ophoping van beschadigde eiwitten. Onder deze druk sterven sommige cellen, maar andere passen zich aan en worden moeilijker te doden met behandeling. Dit artikel onderzoekt hoe darmkankercellen één specifiek soort interne stress overleven — problemen in het endoplasmatisch reticulum, de eiwitvouwfabriek van de cel — en identificeert een moleculaire "rem" die deze gestreste cellen weerhoudt van zelfvernietiging.
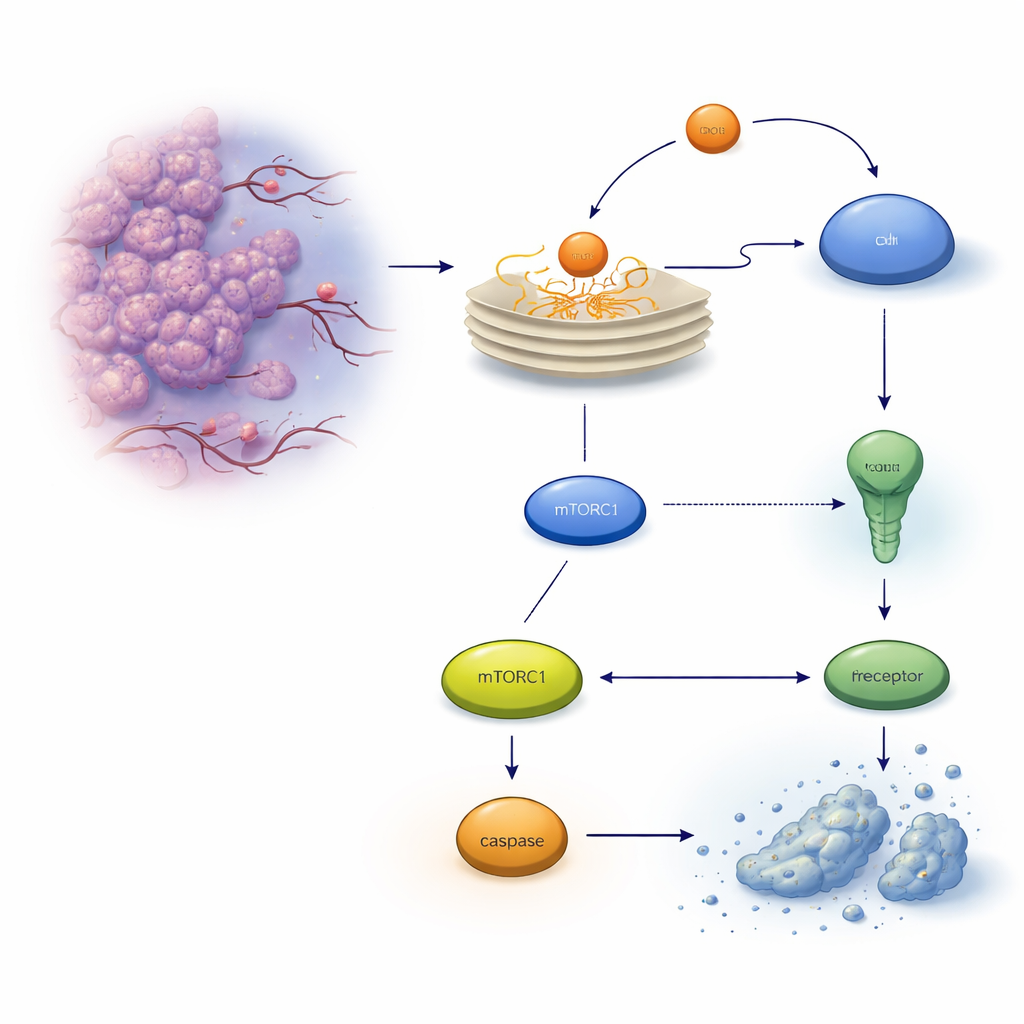
Een verborgen veiligheidsklep binnen tumorcellen
Wanneer eiwitten niet goed worden gevouwen, hopen ze zich op in het endoplasmatisch reticulum (ER) en activeren ze een alarmsysteem dat de unfolded protein response wordt genoemd. In eerste instantie probeert deze respons het evenwicht te herstellen, maar als de stress te sterk is of te lang aanhoudt, kan hij omslaan naar een zelfvernietigingsprogramma dat apoptose heet. In darmkankercellen is een belangrijke uitvoerder een doodsreceptor op het celoppervlak, TRAILR2/DR5, die een eiwitknippend enzym, caspase-8, kan activeren en uiteindelijk de cel kan doden. De auteurs richtten zich op een ander stress-geïnduceerd eiwit, REDD1/DDIT4, dat al bekendstaat om te helpen bij aanpassing aan zware omstandigheden, en vroegen zich af of het deze levens-of-doodsbeslissing beïnvloedt.
Hoe een stress-eiwit de balans naar overleven kantelt
De onderzoekers stelden humane darmkankercellijnen bloot aan medicijnen die ER-stress veroorzaken en volgden REDD1-niveaus in de tijd. Ze vonden dat ER-stress snel de productie van REDD1 verhoogde in een ordelijke volgorde onder controle van een andere stress-gevoelige factor, ATF4. Wanneer REDD1 aanwezig was, dempte het de activiteit van mTORC1, een belangrijke regulator van groei en eiwitsynthese. Het onderdrukken of verwijderen van REDD1 met RNA-interferentie of CRISPR-genbewerking maakte de kankercellen veel vatbaarder voor apoptose onder ER-stress, en deze extra celdood kon worden tegengehouden door caspase-remmers of door farmacologische remming van mTORC1, wat aantoont dat REDD1 normaal gesproken cellen beschermt door deze groeipathway tijdens stress te beperken.
De doodsschakelaar laag houden
Waarom stierven cellen zonder REDD1 gemakkelijker? Het belangrijkste verschil zat in de doodsreceptor TRAILR2/DR5. Bij chronische ER-stress activeerden zowel normale als REDD1-tekortcellen upstream stresspaden op vergelijkbare wijze, maar cellen zonder REDD1 toonden een veel sterkere toename van TRAILR2/DR5 op zowel RNA- als eiwitniveau, samen met sterkere activatie van caspase-8. Het stilleggen van TRAILR2/DR5, maar niet van een verwante receptor, verminderde de apoptose in deze REDD1-deficiënte cellen sterk, wat bewijst dat de verhoogde doodsrespons voornamelijk via deze receptor werd aangestuurd. In driedimensionale tumorsfereiden, die echte tumoren beter nabootsen en van nature stress ophopen, waren REDD1-niveaus al hoog en was de mTORC1-activiteit laag, en het verwijderen van REDD1 maakte deze mini-tumoren opnieuw veel kwetsbaarder voor ER-stress-geïnduceerde celdood.
De rol van een transcriptionele rem
Om te begrijpen hoe REDD1 TRAILR2/DR5 reguleert, gebruikte het team RNA-sequencing om naar regulatoren te zoeken waarvan de niveaus veranderden bij verlies van REDD1. Ze identificeerden een transcriptiefactor genaamd EVI-1/MECOM, eerder verbonden aan kankergroei en genrepressie. In REDD1-deficiënte cellen daalden de EVI-1/MECOM-niveaus. Het verminderen van EVI-1/MECOM in verder normale cellen maakte ze gevoeliger voor ER-stress, verhoogde de expressie van TRAILR2/DR5 en veroorzaakte caspase-8-afhankelijke apoptose, wat het effect van verlies van REDD1 nabootste. De auteurs vonden ook dat co-repressoren genaamd CtBP1/2, bekende partners van EVI-1/MECOM in sommige tumoren, TRAILR2/DR5-niveaus en stressgevoeligheid aanvullend konden bijsturen op een celtype-specifieke manier. Gezamenlijk suggereren deze resultaten dat REDD1 helpt de EVI-1/MECOM-gebaseerde repressie van het TRAILR2/DR5-gen in stand te houden en zo de activering van de doodsschakelaar bij langdurige stress uitstelt.
Wat dit betekent voor toekomstige kankerbehandeling
Voor een algemeen publiek is de belangrijkste conclusie dat darmkankercellen een intern mechanisme hebben dat hen in staat stelt ernstige eiwitstress uit te zitten in plaats van te sterven wanneer dat zou moeten gebeuren. Het eiwit REDD1 werkt als een veiligheidsklep: het dempt een belangrijke groeipathway en ondersteunt een genrepressiesysteem dat voorkomt dat een krachtige doodsreceptor, TRAILR2/DR5, te vroeg wordt ingeschakeld. Wanneer REDD1 of zijn partner EVI-1/MECOM worden verwijderd, zijn gestreste kankercellen veel meer geneigd zichzelf te vernietigen. Dit werk suggereert dat het richten op REDD1 of zijn downstream repressoren tumoren deze beschermende buffer zou kunnen ontnemen, waardoor kankercellen in vijandige, slecht voedzame regio’s van een tumor kwetsbaarder worden voor therapieën die ER-stress verhogen en cellen naar apoptose duwen.
Bronvermelding: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Trefwoorden: ER-stress, dikke darmkanker, apoptose, TRAILR2/DR5, REDD1/DDIT4