Clear Sky Science · es
REDD1/DDIT4 contrarresta la apoptosis inducida por el estrés del retículo endoplasmático controlando la expresión del receptor de muerte TRAILR2/DR5 en células cancerosas
Por qué importan las células tumorales estresadas
Las células cancerosas no crecen en condiciones cómodas. Dentro de un tumor, las células afrontan bajo oxígeno, nutrientes escasos y una acumulación de proteínas dañadas. Bajo esta presión, algunas células mueren, pero otras se adaptan y se vuelven más difíciles de eliminar con el tratamiento. Este artículo explora cómo las células de cáncer de colon sobreviven a un tipo específico de estrés interno: problemas en el retículo endoplasmático, la «fábrica» de plegado de proteínas de la célula, e identifica un «freno» molecular que evita que estas células estresadas se autodestruyan.
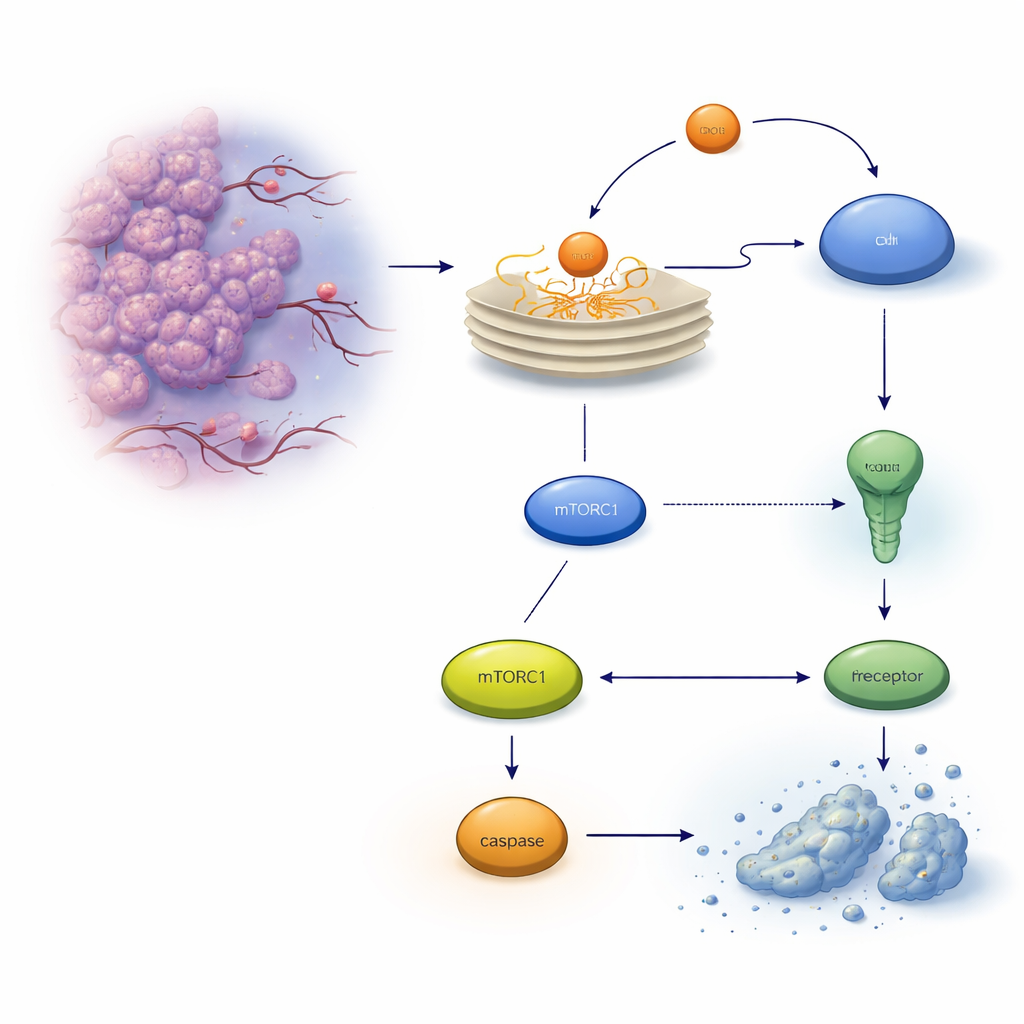
Una válvula de seguridad oculta dentro de las células tumorales
Cuando las proteínas no se pliegan correctamente, se acumulan en el retículo endoplasmático (RE) y activan un sistema de alarma llamado respuesta a proteínas desplegadas. Al principio, esta respuesta intenta restaurar el equilibrio, pero si el estrés es demasiado intenso o se prolonga, puede desencadenar un programa de autodestrucción conocido como apoptosis. En las células de cáncer de colon, uno de los ejecutores clave es un receptor de muerte en la superficie celular llamado TRAILR2/DR5, que puede activar una enzima cortadora de proteínas, la caspasa‑8, y finalmente provocar la muerte celular. Los autores se centraron en otra proteína inducida por el estrés, REDD1/DDIT4, ya conocida por ayudar a las células a adaptarse a condiciones adversas, y se preguntaron si influye en esta decisión de vida o muerte.
Cómo una proteína del estrés inclina la balanza hacia la supervivencia
Los investigadores expusieron líneas celulares humanas de cáncer de colon a fármacos que provocan estrés del RE y siguieron los niveles de REDD1 a lo largo del tiempo. Hallaron que el estrés del RE aumentaba rápidamente la producción de REDD1 de forma ordenada, controlada por otro factor sensible al estrés, ATF4. Cuando REDD1 estaba presente, atenuaba la actividad de mTORC1, un regulador importante del crecimiento y de la síntesis de proteínas. Reducir o eliminar REDD1 mediante interferencia por ARN o edición genética CRISPR hizo que las células cancerosas fueran mucho más propensas a sufrir apoptosis bajo estrés del RE, y esta muerte celular adicional podía bloquearse con inhibidores de caspasas o inhibiendo farmacológicamente mTORC1, lo que demuestra que REDD1 protege normalmente a las células al contener esta vía de crecimiento durante el estrés.
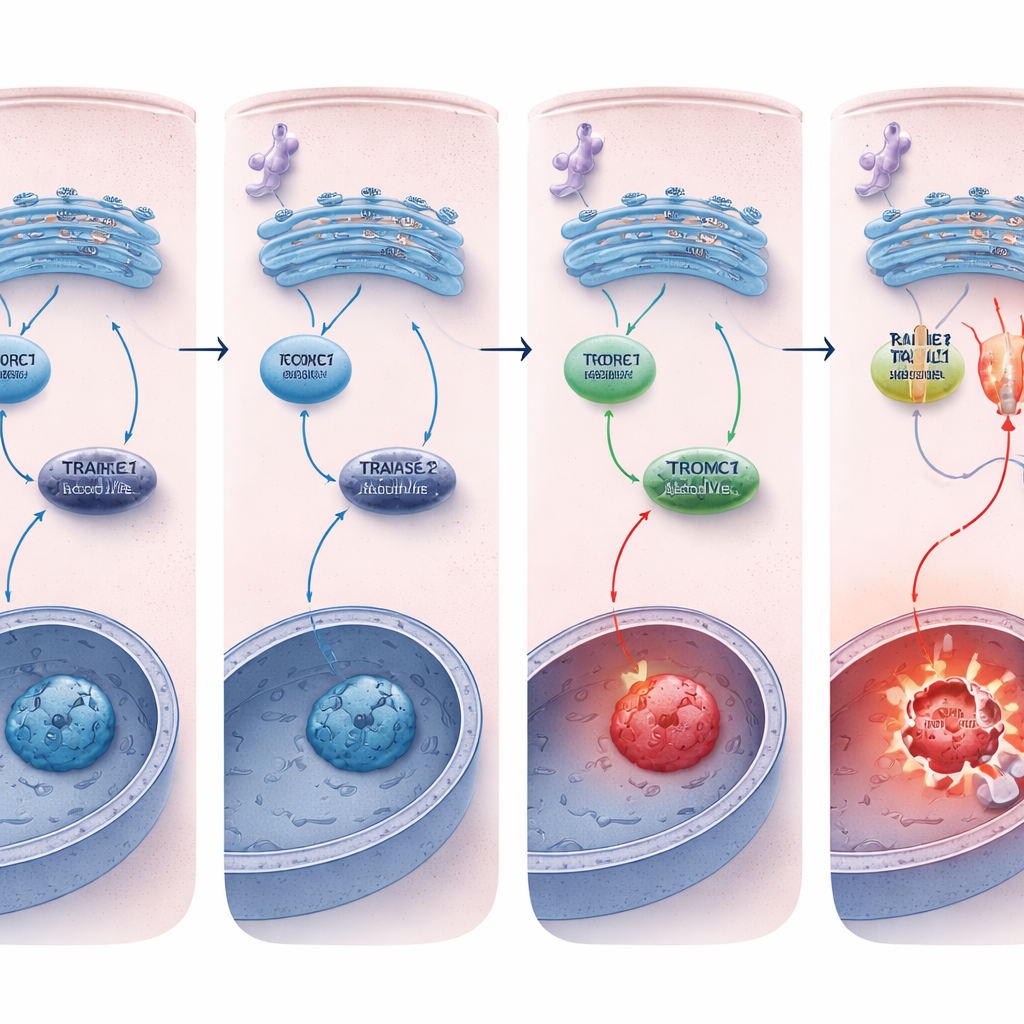
Mantener el interruptor de la muerte bajado
¿Por qué morían más fácilmente las células deficientes en REDD1? La diferencia clave estaba en el receptor de muerte TRAILR2/DR5. Bajo estrés crónico del RE, tanto las células normales como las deficientes en REDD1 activaban de forma similar las vías de estrés aguas arriba, pero las células sin REDD1 mostraron un aumento mucho mayor de TRAILR2/DR5 a nivel de ARN y de proteína, junto con una mayor activación de la caspasa‑8. Silenciar TRAILR2/DR5, pero no un receptor relacionado, redujo drásticamente la apoptosis en estas células deficientes en REDD1, demostrando que la respuesta de muerte amplificada se debía principalmente a este receptor. En esféroides tumorales tridimensionales, que imitan mejor a los tumores reales y acumulan estrés de forma natural, los niveles de REDD1 ya eran altos y la actividad de mTORC1 baja, y eliminar REDD1 volvió a hacer que estos mini‑tumores fueran mucho más vulnerables a la muerte celular inducida por el estrés del RE.
El papel de un freno transcripcional
Para entender cómo REDD1 controla TRAILR2/DR5, el equipo usó secuenciación de ARN para buscar reguladores cuyos niveles cambiaban cuando se perdía REDD1. Identificaron un factor de transcripción llamado EVI‑1/MECOM, previamente vinculado al crecimiento tumoral y a la represión génica. En las células deficientes en REDD1, los niveles de EVI‑1/MECOM disminuyeron. Reducir EVI‑1/MECOM en células por lo demás normales las hizo más sensibles al estrés del RE, aumentó la expresión de TRAILR2/DR5 y provocó apoptosis dependiente de caspasa‑8, imitando el efecto de perder REDD1. Los autores también hallaron que correpresores llamados CtBP1/2, socios conocidos de EVI‑1/MECOM en algunos tumores, podían ajustar además los niveles de TRAILR2/DR5 y la sensibilidad al estrés de forma específica según el tipo celular. En conjunto, estos resultados sugieren que REDD1 ayuda a mantener la represión mediada por EVI‑1/MECOM del gen TRAILR2/DR5, retrasando la activación del interruptor de la muerte durante un estrés prolongado.
Qué significa esto para el tratamiento futuro del cáncer
Para un público general, la conclusión principal es que las células de cáncer de colon poseen un mecanismo interno que les permite «resistir» un estrés proteico severo en lugar de morir cuando deberían. La proteína REDD1 actúa como una válvula de seguridad: apaga una vía de crecimiento importante y apoya un sistema de represión génica que impide que un potente receptor de muerte, TRAILR2/DR5, se active demasiado pronto. Cuando se eliminan REDD1 o su socio EVI‑1/MECOM, las células tumorales estresadas tienen muchas más probabilidades de autodestruirse. Este trabajo sugiere que dirigirse a REDD1 o a sus represores downstream podría despojar a los tumores de este cojín protector, haciendo que las células cancerosas en regiones hostiles y mal nutridas del tumor sean más vulnerables a terapias que aumenten el estrés del RE y empujen a las células hacia la apoptosis.
Cita: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Palabras clave: estrés ER, cáncer colorrectal, apoptosis, TRAILR2/DR5, REDD1/DDIT4