Clear Sky Science · ar
REDD1/DDIT4 يواجه موت الخلايا الناجم عن إجهاد الشبكة الإندوبلازمية من خلال التحكم في تعبير مستقبل الموت TRAILR2/DR5 في خلايا السرطان
لماذا تهم الخلايا الورمية المتعرضة للإجهاد
خلايا السرطان لا تنمو في ظروف مريحة. داخل الورم تواجه الخلايا نقص الأكسجين، وندرة المغذيات وتراكم بروتينات تالفة. تحت هذا الضغط تموت بعض الخلايا، لكن خلايا أخرى تتكيف وتصبح أصعب في القتل بالعلاج. تبحث هذه الورقة في كيفية نجاة خلايا سرطان القولون من نوع محدد من الإجهاد الداخلي — خلل في الشبكة الإندوبلازمية، مصنع طي البروتينات داخل الخلية — وتحدد «فرامل» جزيئية تبقي هذه الخلايا المتعرضة للإجهاد عن الانتحار الذاتي.
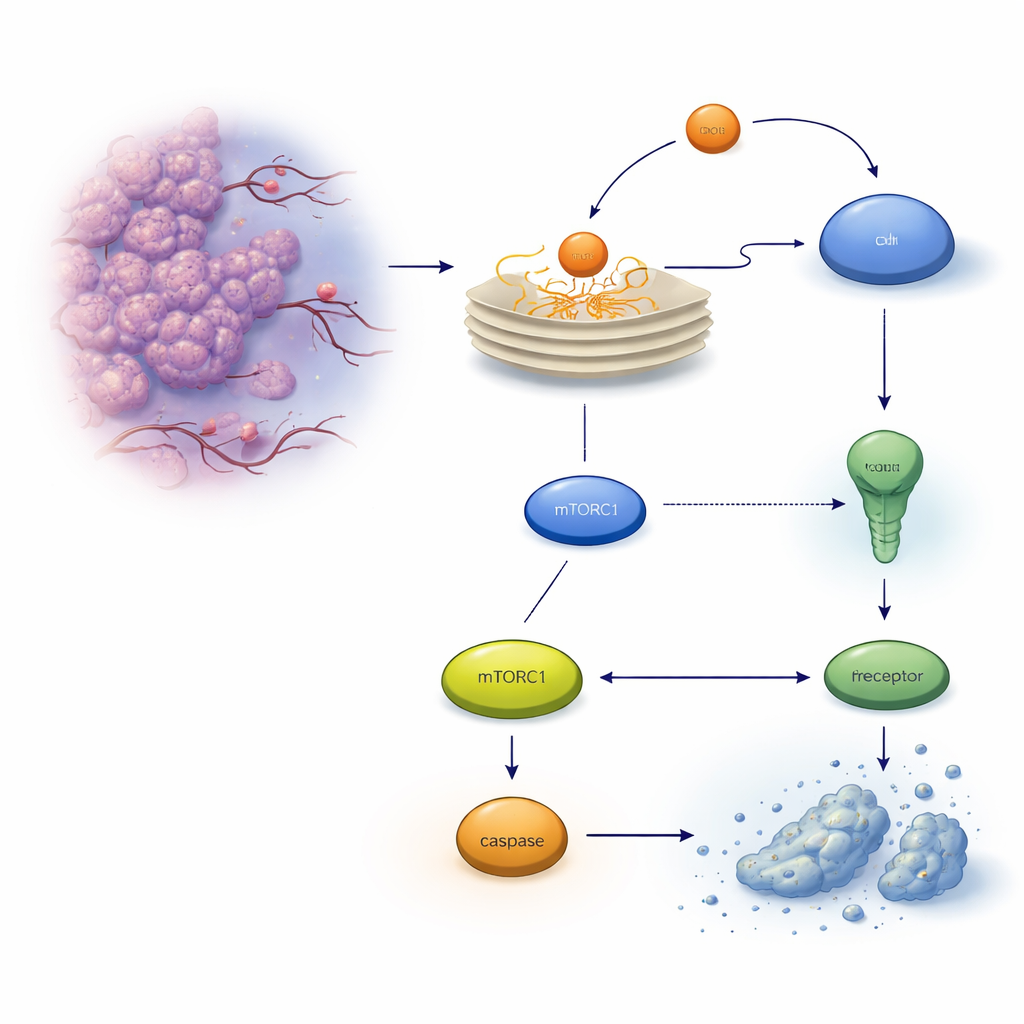
صمام أمان خفي داخل الخلايا الورمية
عندما لا تُطوى البروتينات بشكل صحيح تتراكم في الشبكة الإندوبلازمية، مما يطلق نظام إنذار يسمى استجابة البروتين غير المطوي. في البداية تحاول هذه الاستجابة إعادة التوازن، لكن إذا كان الإجهاد قويًا جدًا أو طويل الأمد، فقد تتحول إلى برنامج انتحاري يعرف بالاستماتة. في خلايا سرطان القولون، أحد المنفذين الرئيسيين هو مستقبل موت على سطح الخلية يسمى TRAILR2/DR5، الذي يمكنه تفعيل إنزيم قاطع بروتينات، الكاسبيز‑8، وفي النهاية قتل الخلية. ركز المؤلفون على بروتين آخر يحفزه الإجهاد، REDD1/DDIT4، المعروف بالفعل بمساعدة الخلايا على التكيف مع ظروف قاسية، وتساؤلوا عما إذا كان يؤثر على قرار الحياة أو الموت هذا.
كيف يميل بروتين الإجهاد الميزان نحو البقاء
عرض الباحثون سلاسل خلايا سرطان القولون البشرية لأدوية تسبب إجهاد الشبكة الإندوبلازمية وتتبعوا مستويات REDD1 مع مرور الوقت. وجدوا أن الإجهاد يزيد بسرعة إنتاج REDD1 بطريقة منظمة تتحكم بها عامل استجابة للإجهاد آخر، ATF4. عندما كان REDD1 موجودًا كان يخمد نشاط mTORC1، وهو منظم رئيسي للنمو وتخليق البروتين. إخماد REDD1 أو حذفه باستخدام التدخّل الريبوزي أو تحرير الجينات CRISPR جعل الخلايا السرطانية أكثر عرضة بكثير للخضوع للاستماتة تحت إجهاد الشبكة الإندوبلازمية، ويمكن حجب هذه الزيادة في موت الخلايا بواسطة مثبطات الكاسبيز أو عن طريق إيقاف mTORC1 دوائيًا، مما يوضح أن REDD1 عادةً يحمي الخلايا عن طريق تقييد هذا المسار النموي أثناء الإجهاد.
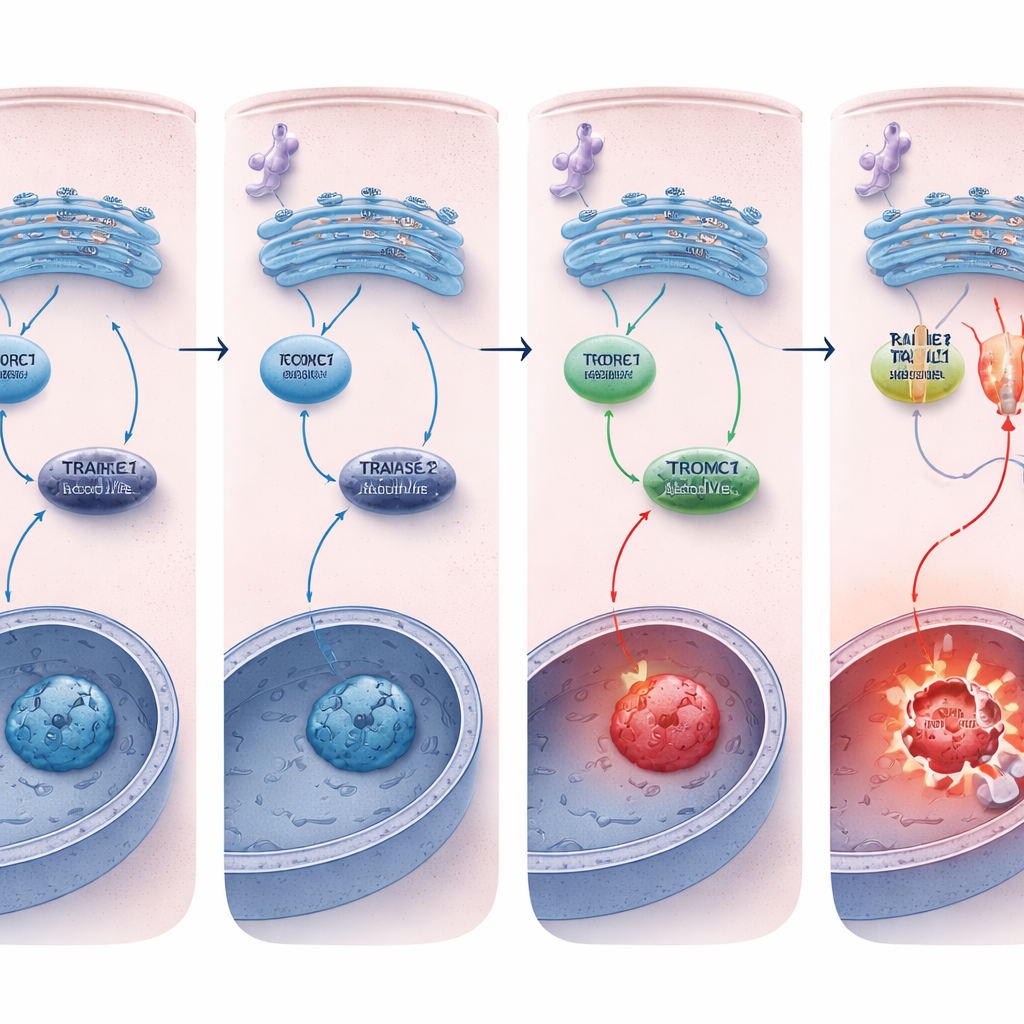
إبقاء مفتاح الموت منخفضًا
لماذا ماتت الخلايا الخالية من REDD1 بسهولة أكبر؟ الاختلاف الرئيسي كان في مستقبل الموت TRAILR2/DR5. تحت الإجهاد المزمن للشبكة الإندوبلازمية، نشّطت كل من الخلايا الطبيعية والخالية من REDD1 المسارات الالتهابية العليا بنفس الطريقة، لكن الخلايا التي تفتقر إلى REDD1 أظهرت ارتفاعًا أكبر بكثير في TRAILR2/DR5 على مستوى الحمض النووي الريبي والبروتين، إلى جانب تفعيل أقوى للكاسبيز‑8. قمع TRAILR2/DR5، ولكن ليس مستقبلًا ذا صلة، قلل بشدة من الاستماتة في هذه الخلايا الخالية من REDD1، مما يثبت أن الاستجابة المفرطة للموت كانت مدفوعة أساسًا عبر هذا المستقبل. في متعضيات ورمية ثلاثية الأبعاد، التي تحاكي الأورام الحقيقية بشكل أفضل وتتراكم فيها الضغوط طبيعيًا، كانت مستويات REDD1 مرتفعة بالفعل ونشاط mTORC1 منخفضًا، وإزالة REDD1 مرة أخرى جعلت هذه الأورام الصغيرة أكثر ضعفًا بكثير أمام موت الخلايا الناجم عن إجهاد الشبكة الإندوبلازمية.
دور فرامل النسخ الجيني
لفهم كيف يتحكم REDD1 في TRAILR2/DR5 استخدم الفريق تسلسل الـRNA للبحث عن منظمات تغيرت مستوياتها عند فقدان REDD1. حدّدوا عامل نسخ يدعى EVI‑1/MECOM، مرتبط سابقًا بنمو السرطان وكبت التعبير الجيني. في الخلايا الخالية من REDD1 انخفضت مستويات EVI‑1/MECOM. تقليل EVI‑1/MECOM في خلايا طبيعية جعلها أكثر حساسية لإجهاد الشبكة الإندوبلازمية، وزاد تعبير TRAILR2/DR5 وقاد إلى استماتة معتمدة على الكاسبيز‑8، مقلدًا تأثير فقدان REDD1. كما وجد المؤلفون أن معاقِسات مشاركة تسمى CtBP1/2، وهي شركاء معروفون لـEVI‑1/MECOM في بعض الأورام، يمكن أن تضبط مستويات TRAILR2/DR5 وحساسية الإجهاد بطريقة خاصة بنوع الخلية. معًا تشير هذه النتائج إلى أن REDD1 يساعد في الحفاظ على كبت جيني قائم على EVI‑1/MECOM لجين TRAILR2/DR5، مما يؤخر تفعيل مفتاح الموت أثناء الإجهاد المطوّل.
ما الذي يعنيه هذا لعلاج السرطان في المستقبل
الخلاصة للقارئ العام هي أن خلايا سرطان القولون تمتلك آلية داخلية تسمح لها «باجتياز» الإجهاد البروتيني الشديد بدلًا من الموت عندما ينبغي أن تموت. يعمل البروتين REDD1 كصمام أمان: يهدئ مسار نمو رئيسي ويدعم نظام كبت جيني يحافظ على مستقبل الموت القوي TRAILR2/DR5 من التشغّل مبكرًا. عندما يُزال REDD1 أو شريكه EVI‑1/MECOM تصبح الخلايا السرطانية المتعرضة للإجهاد أكثر عرضة بكثير للانتحار الذاتي. تشير هذه الدراسة إلى أن استهداف REDD1 أو معاقِساته السفلية قد يَجرد الأورام من هذا الوسادة الواقية، مما يجعل خلايا السرطان في مناطق الورم الفقيرة المغذيات أكثر عرضة للعلاجات التي تزيد إجهاد الشبكة الإندوبلازمية وتدفع الخلايا نحو الاستماتة.
الاستشهاد: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
الكلمات المفتاحية: إجهاد الشبكة الإندوبلازمية, سرطان القولون والمستقيم, الاستماتة (الموت المبرمج), TRAILR2/DR5, REDD1/DDIT4