Clear Sky Science · ja
REDD1/DDIT4 は死の受容体 TRAILR2/DR5 の発現を制御して小胞体ストレス誘導アポトーシスに拮抗する(がん細胞において)
なぜストレスを受けた腫瘍細胞が重要か
がん細胞は快適な環境で増殖しているわけではありません。腫瘍内部では低酸素、栄養不足、損傷タンパク質の蓄積に直面します。このような圧力下で一部の細胞は死にますが、他は適応して治療に対してより耐性を持つようになります。本論文は、大腸がん細胞が細胞内の特定のストレス――タンパク質折りたたみを担う小胞体(ER)の障害――をどのように生き延びるかを探り、こうしたストレス下で細胞の自滅を抑える分子上の“ブレーキ”を同定しています。
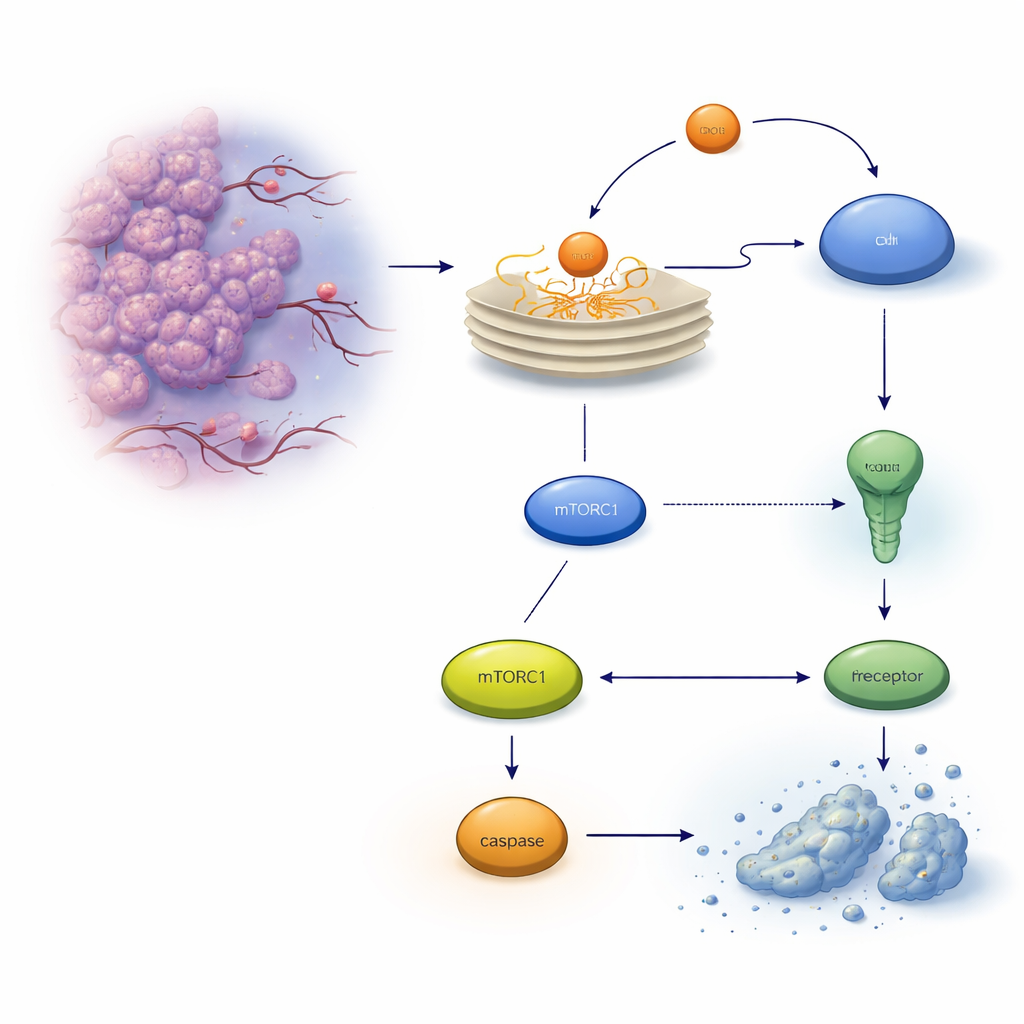
腫瘍細胞内の隠れた安全弁
タンパク質が正しく折りたたまれないと小胞体内に蓄積し、アンフォールデッド・プロテイン応答と呼ばれる警報システムが作動します。当初はこの応答は均衡回復を試みますが、ストレスが強すぎるか長引くと、アポトーシスという自己破壊プログラムに転じることがあります。大腸がん細胞において重要な実行因子の一つは細胞表面の死の受容体である TRAILR2/DR5 で、これがカスパーゼ-8 を活性化して最終的に細胞を死に導きます。著者らは、過酷な条件への適応を助けることが知られるストレス誘導性タンパク質 REDD1/DDIT4 に注目し、これが生死の選択に影響するかを検討しました。
ストレスタンパク質が生存へ傾ける仕組み
研究者たちはヒト大腸がん細胞株に ER ストレスを引き起こす薬剤を投与し、時間経過での REDD1 レベルを追跡しました。ER ストレスは速やかに REDD1 の産生を増加させ、その誘導は別のストレス応答因子 ATF4 によって秩序立てて制御されていることが分かりました。REDD1 が存在すると mTORC1(成長とタンパク質合成を制御する主要経路)の活性が抑えられます。RNA干渉や CRISPR による REDD1 のノックダウン・欠失は、ER ストレス下でがん細胞をアポトーシスに陥らせやすくし、この余分な細胞死はカスパーゼ阻害剤や薬理的な mTORC1 の遮断によって阻止できました。これにより、REDD1 は通常、ストレス時にこの成長経路を抑えることで細胞を保護していることが示されました。
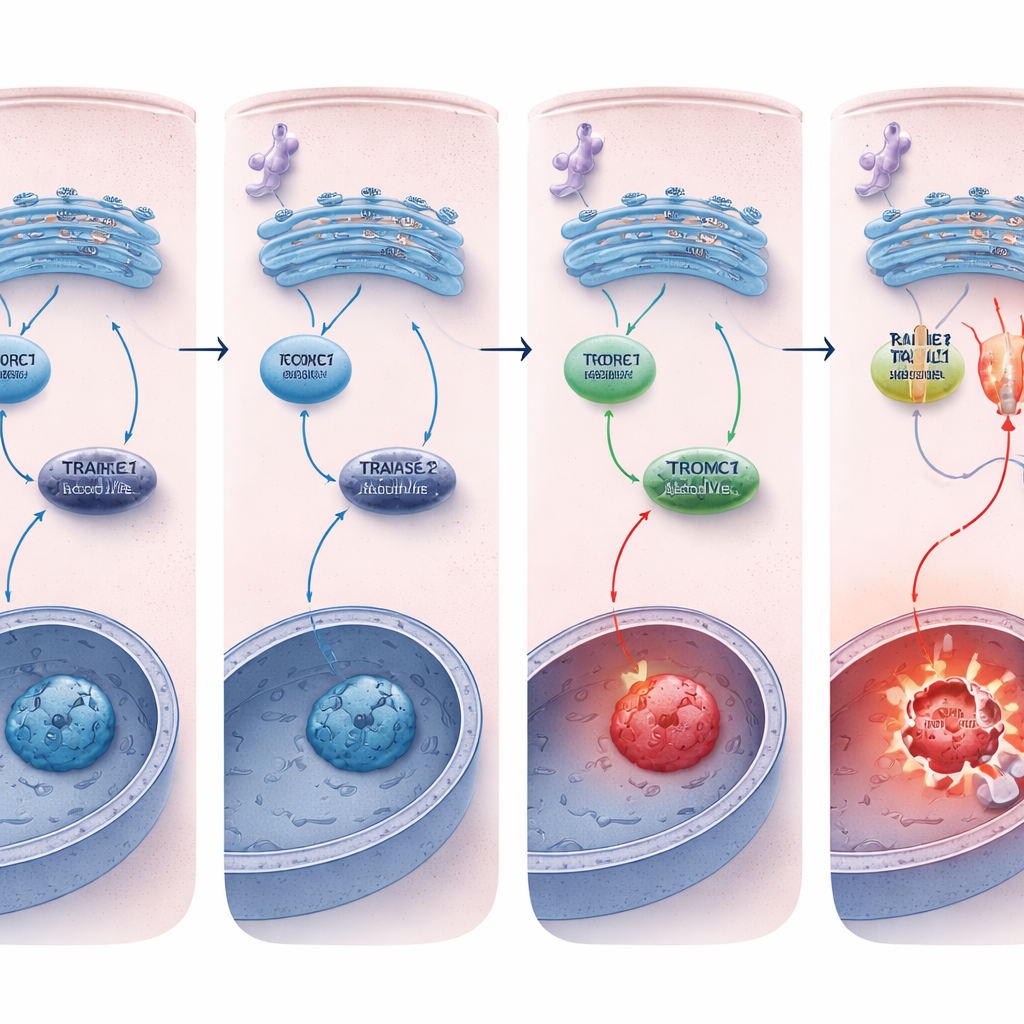
死のスイッチを抑えておく
なぜ REDD1 欠損細胞はより死にやすいのか。その鍵は死の受容体 TRAILR2/DR5 にありました。慢性的な ER ストレス下で、正常細胞と REDD1 欠損細胞は上流のストレス経路を同様に活性化しましたが、REDD1 を欠く細胞では TRAILR2/DR5 の RNA とタンパク質の両方の増加がはるかに大きく、カスパーゼ-8 の活性化も強くなっていました。関連する別の受容体を沈黙させても効果はなく、TRAILR2/DR5 をサイレンシングすると REDD1 欠損細胞のアポトーシスが大きく減少し、この増強された死応答が主にこの受容体を介して駆動されていることが証明されました。三次元腫瘍スフェロイド(実際の腫瘍をよりよく模倣し自然にストレスを蓄積する)では、REDD1 レベルは既に高く mTORC1 活性は低く、REDD1 を除くとこれらのミニ腫瘍も ER ストレス誘導性の細胞死に対してはるかに脆弱になることが確認されました。
転写抑制の役割
REDD1 が TRAILR2/DR5 をどのように制御するかを解明するため、研究チームは RNA シーケンシングで REDD1 を失ったときに変化する調節因子を探索しました。そこで彼らは、がん増殖や遺伝子抑制に関連して報告されている転写因子 EVI-1/MECOM を特定しました。REDD1 欠損細胞では EVI-1/MECOM のレベルが低下していました。正常細胞で EVI-1/MECOM を低下させると ER ストレスに対して感受性が高まり、TRAILR2/DR5 の発現が増え、カスパーゼ-8 依存的アポトーシスが誘導され、REDD1 喪失の効果を模倣しました。著者らはまた、いくつかの腫瘍で EVI-1/MECOM のパートナーとして知られる共抑制因子 CtBP1/2 が、細胞種特異的に TRAILR2/DR5 レベルやストレス感受性をさらに調整し得ることを見いだしました。これらの結果は、REDD1 が TRAILR2/DR5 遺伝子に対する EVI-1/MECOM を介した抑制を維持し、長引くストレス下で死のスイッチの作動を遅らせるのに寄与していることを示唆します。
今後のがん治療への示唆
一般向けの要点は、大腸がん細胞には激しいタンパク質ストレスに直面しても本来死ぬべき時に死なないようにする内部メカニズムが備わっているということです。タンパク質 REDD1 は安全弁のように働き、主要な成長経路を静め、強力な死受容体 TRAILR2/DR5 の早期発現を抑える遺伝子抑制システムを支えます。REDD1 やそのパートナーである EVI-1/MECOM を失うと、ストレス下のがん細胞は自己破壊しやすくなります。本研究は、REDD1 やその下流の抑制因子を標的にすることで、この保護的バッファーを腫瘍から奪い、栄養の乏しい腫瘍内領域にいるがん細胞を ER ストレスを増強してアポトーシスへ追い込む治療に対してより脆弱にできる可能性を示唆しています。
引用: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
キーワード: 小胞体ストレス, 大腸がん, アポトーシス, TRAILR2/DR5, REDD1/DDIT4