Clear Sky Science · he
REDD1/DDIT4 מתנגד לתכ programmedי של ER המוביל לאפופטוזה על ידי בקרה על הביטוי של קולט המוות TRAILR2/DR5 בתאי סרטן
מדוע תאי גידול במצוקה חשובים
תאי סרטן אינם מתפתחים בתנאים נוחים. בתוך הגידול התאים נחשפים לחוסר חמצן, למחסור בחומרי הזנה ולהצטברות חלבונים פגומים. תחת הלחץ הזה חלק מהתאים מתים, אך אחרים מסתגלים והופכים לקשי הרג יותר בטיפולים. המאמר חוקר כיצד תאי סרטן במעי הגס שורדים סוג ספציפי של מתח פנימי — תקלות במערכת האנדופלזמית (ER), בית־המלאכה לקיפול חלבונים — ומזהה "בלם" מולקולרי שמונע מתאים אלה להשמיד את עצמם.
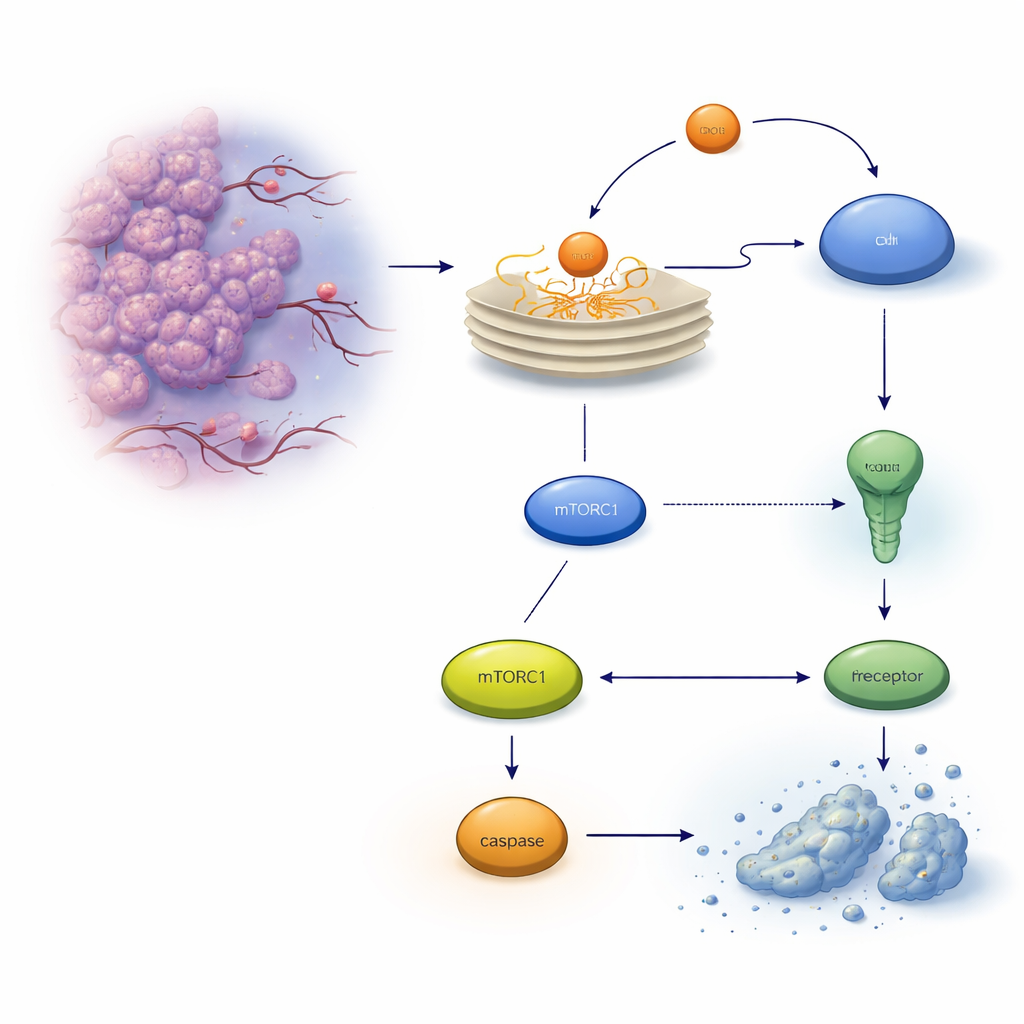
שסתום בטיחות מוסתר בתוך תאי הגידול
כשחלבונים אינם מקופלים כראוי הם מצטברים ב‑ER ומפעילים מערכת אזעקה שנקראת תגובת החלבון הלא מקופל. בתחילה תגובה זו מנסה להשיב את המערכת לאיזון, אך אם הלחץ חזק מדי או ארוך מדי היא עלולה להתהפך לתוכנית השמדה עצמית הנקראת אפופטוזה. בתאי סרטן של המעי הגס אחד המבצעים המרכזיים הוא קולט מוות על פני התא, TRAILR2/DR5, שיכול להפעיל אנזים חותך חלבונים, קספאז‑8, ולבסוף להרוג את התא. החוקרים התרכזו בחלבון אחר שמיוצר בתגובה למתח, REDD1/DDIT4, שידוע מסייע לתאים להסתגל לתנאים קשים, ובחנו האם הוא משפיע על ההחלטה בין חיים ומוות.
כיצד חלבון הלחץ מטה את הכף לטובת הישרדות
החוקרים חשפו קווי תאי סרטן של המעי הגס האנושיים לתרופות שגורמות למתח ב‑ER ועקבו אחרי רמות REDD1 לאורך זמן. הם מצאו שמתח ב‑ER מגביר במהירות את ייצור REDD1 באופן מאורגן הנשלט על ידי גורם תגובה למתח אחר, ATF4. כשה‑REDD1 נוכח, הוא מדכא את פעילות mTORC1, רגולטור מרכזי של גדילה וסינתזת חלבונים. דיכוי או מחיקה של REDD1 באמצעות הפרעה ב‑RNA או עריכת גנים ב‑CRISPR הגדילו משמעותית את הסבירות שתאי הסרטן יעברו אפופטוזה תחת מתח ב‑ER, ומוות התאים המוגבר הזה ניתן לעיכוב על ידי מעכבי קספאז או על ידי כיבוי פרמקולוגי של mTORC1, מה שמראה ש‑REDD1 בדרך כלל מגן על תאים על ידי קיבוע נתיב הגדילה הזה בזמן לחץ.
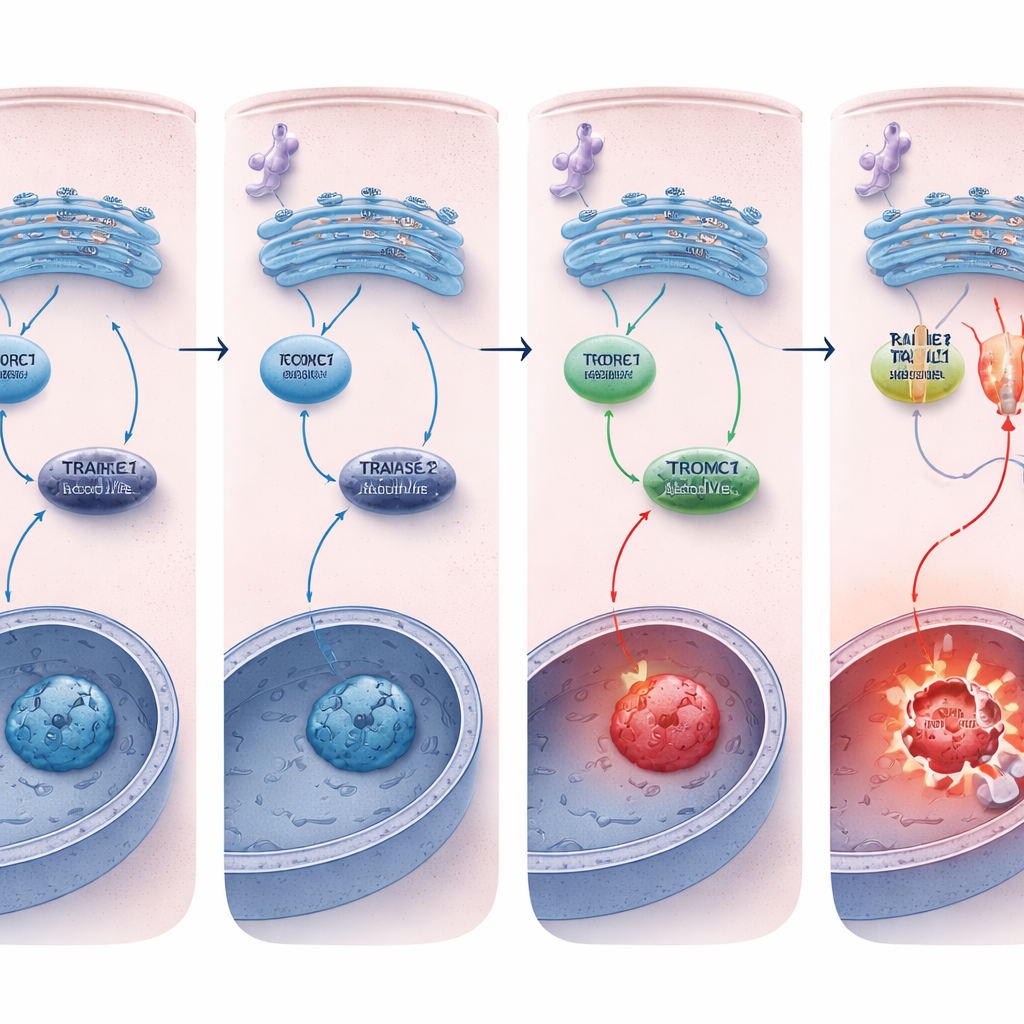
שמירה שהמתג של המוות יישאר מושתק
מדוע תאים חסרי REDD1 מתים בקלות רבה יותר? ההבדל המכריע היה בקולט המוות TRAILR2/DR5. תחת מתח כרוני ב‑ER גם תאים נורמליים וגם תאים חסרי REDD1 הפעילו את מסלולי הלחץ המקוריים בדומה, אך בתאים חסרי REDD1 נצפתה עלייה גדולה בהרבה ב‑TRAILR2/DR5 הן ברמת ה‑RNA והן ברמת החלבון, לצד הפעלה חזקה יותר של קספאז‑8. השתקת TRAILR2/DR5, אך לא של קולט קרוב קשור, הקטינה באופן חד את האפופטוזה בתאים חסרי REDD1, והראתה כי התגובה המוגברת למוות מונעת בעיקר דרך קולט זה. בספירות גידול תלת־ממדיות, המדמות טוב יותר גידולים אמיתיים והצטברות לחץ באופן טבעי, רמות REDD1 היו כבר גבוהות ופעילות mTORC1 הייתה נמוכה, והסרת REDD1 שוב הפכה את ה"מיני־גידולים" האלה לפגיעים יותר למוות תאי המושרה על‑ידי מתח ב‑ER.
תפקיד הבלם בתעתוק
כדי להבין כיצד REDD1 שולט ב‑TRAILR2/DR5, הצוות השתמש בריצוף RNA לחיפוש רגולטורים שרמותיהם משתנות כאשר REDD1 אובד. הם זיהו פקטור שעתוק בשם EVI‑1/MECOM, שנקשר בעבר לצמיחת סרטן ולדיכוי גנים. בתאים חסרי REDD1 רמות EVI‑1/MECOM ירדו. הקטנת EVI‑1/MECOM בתאים נורמליים הפכה אותם לרגישים יותר למתח ב‑ER, העלתה את ביטוי TRAILR2/DR5 והובילה לאפופטוזה תלויית קספאז‑8, מה שהדמה את אפקט אובדן REDD1. החוקרים גם מצאו שמשתקפי‑שעתוק שיתופיים הנקראים CtBP1/2, שידועים כשותפים של EVI‑1/MECOM בכמה גידולים, יכלו לכוונן עוד את רמות TRAILR2/DR5 ואת הרגישות למתח באופן שתלוי בסוג התא. מכלול התוצאות מצביע על כך ש‑REDD1 מסייע לשמר דיכוי מבוסס EVI‑1/MECOM על גן TRAILR2/DR5, ובכך מעכב את הדלקתו של מתג המוות במהלך לחץ ממושך.
מה משמעות הדבר לטיפולי סרטן בעתיד
לציבור הרחב, המסקנה המרכזית היא שתאי סרטן של המעי הגס מחזיקים מנגנון פנימי שמאפשר להם "לשרוד" לחץ חלבוני חמור במקום למות כשהם אמורים. חלבון REDD1 מתפקד כשסתום ביטחון: הוא ממתן נתיב גדילה מרכזי ותומך במערכת דיכוי גנטי שמונעת מהקולטן החזק TRAILR2/DR5 להתפעיל מוקדם מדי. כאשר REDD1 או שותפו EVI‑1/MECOM מוסרים, תאי הסרטן במצוקה נוטים הרבה יותר להשמיד את עצמם. עבודה זו מרמזת כי כיוונון REDD1 או המדכאים שהוא מפעיל עשוי לפגוע במגן ההגנתי של הגידול, ולהפוך תאים באזורים עוינים ועניי מזון בגידול לפגיעים יותר לטיפולים המגבירים לחץ ב‑ER ודוחפים את התאים לאפופטוזה.
ציטוט: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
מילות מפתח: לחץ ER, סרטן המעי הגס, אפופטוזה, TRAILR2/DR5, REDD1/DDIT4