Clear Sky Science · pt
REDD1/DDIT4 contrapõe-se à apoptose induzida por estresse do retículo endoplasmático ao controlar a expressão do receptor de morte TRAILR2/DR5 em células cancerígenas
Por que células tumorais estressadas importam
Células cancerígenas não crescem em conforto. Dentro de um tumor, as células enfrentam baixo oxigênio, nutrientes escassos e acúmulo de proteínas danificadas. Sob essa pressão, algumas células morrem, mas outras se adaptam e se tornam mais difíceis de eliminar com tratamento. Este artigo explora como células de câncer de cólon sobrevivem a um tipo específico de estresse interno — problemas no retículo endoplasmático, a “fábrica” de dobramento de proteínas da célula — e identifica um “freio” molecular que impede essas células estressadas de se autodestruírem.
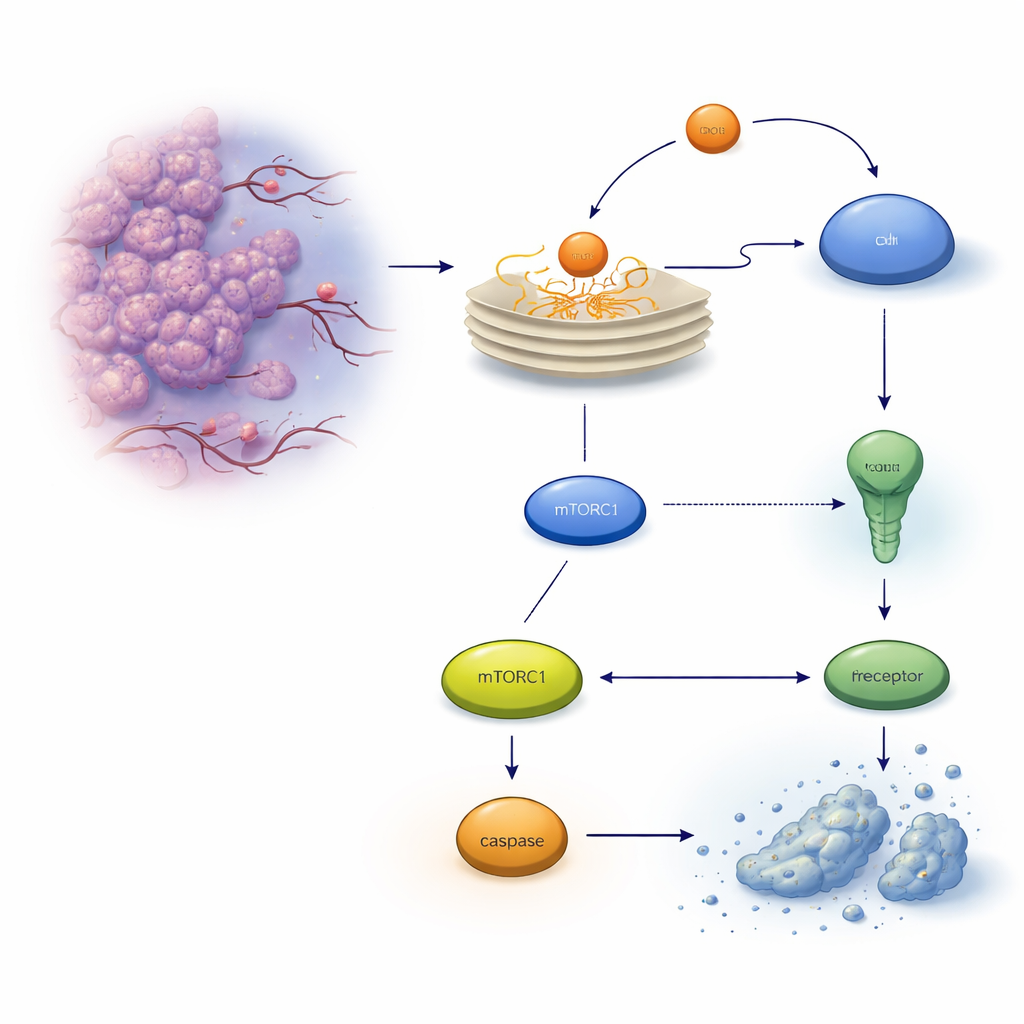
Uma válvula de segurança oculta dentro das células tumorais
Quando proteínas não são dobradas corretamente, elas se acumulam no retículo endoplasmático (RE), acionando um sistema de alarme chamado resposta a proteínas desnaturadas. A princípio, essa resposta tenta restaurar o equilíbrio, mas se o estresse for muito intenso ou persistir por muito tempo, pode convergir para um programa de autodestruição conhecido como apoptose. Em células de câncer de cólon, um executor chave é um receptor de morte na superfície celular chamado TRAILR2/DR5, que pode ativar uma enzima que corta proteínas, a caspase‑8, e, em última instância, matar a célula. Os autores se concentraram em outra proteína induzida por estresse, REDD1/DDIT4, já conhecida por ajudar células a se adaptarem a condições adversas, e investigaram se ela influencia essa decisão entre vida e morte.
Como uma proteína de estresse inclina a balança para a sobrevivência
Os pesquisadores expuseram linhagens de células humanas de câncer de cólon a fármacos que causam estresse no RE e acompanharam os níveis de REDD1 ao longo do tempo. Eles descobriram que o estresse no RE aumentou rapidamente a produção de REDD1 de forma ordenada, controlada por outro fator responsivo ao estresse, ATF4. Quando REDD1 estava presente, ele atenuava a atividade de mTORC1, um importante regulador do crescimento e da síntese proteica. Reduzir ou deletar REDD1 usando interferência por RNA ou edição gênica CRISPR tornou as células cancerígenas muito mais propensas a entrar em apoptose sob estresse do RE, e essa morte celular adicional pôde ser bloqueada por inibidores de caspase ou pela inibição farmacológica de mTORC1, mostrando que REDD1 normalmente protege as células ao conter essa via de crescimento durante o estresse.
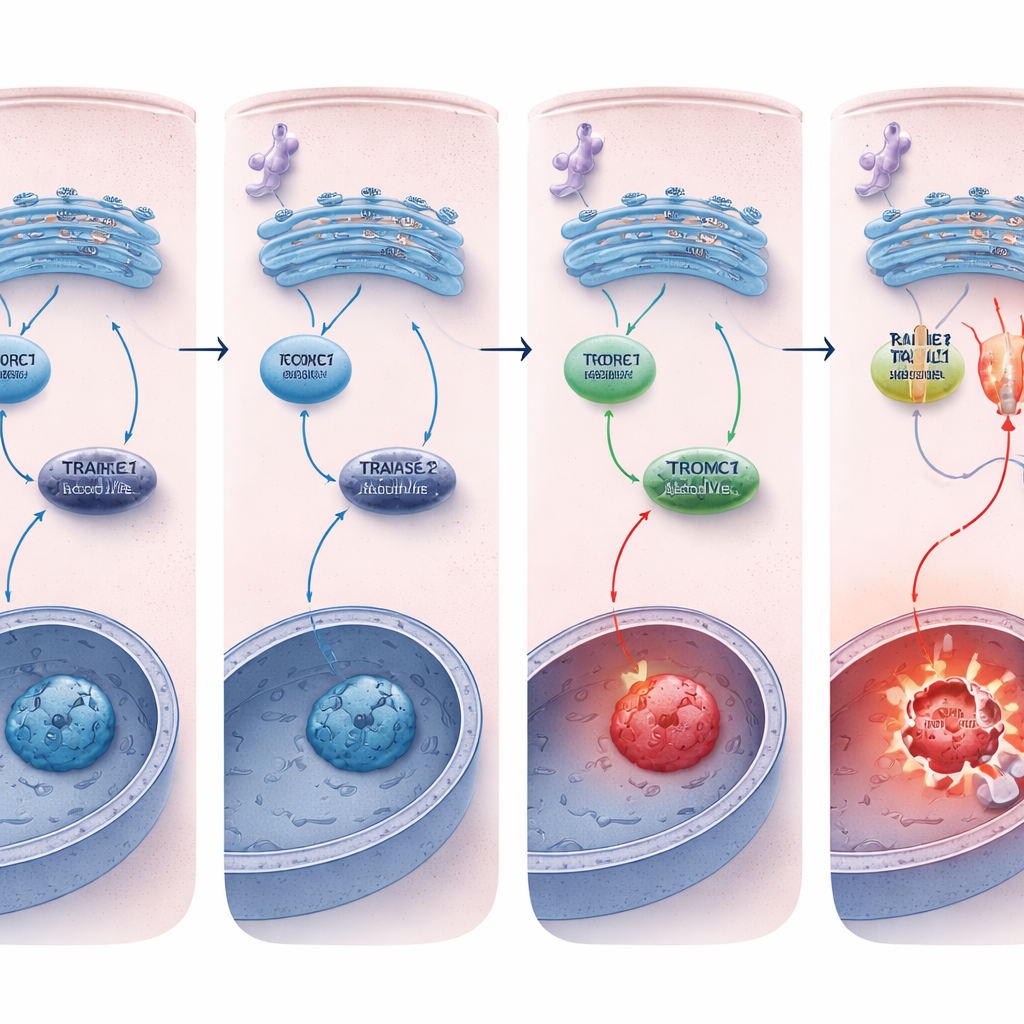
Manter o interruptor da morte reduzido
Por que células deficientes em REDD1 morriam mais facilmente? A diferença chave estava no receptor de morte TRAILR2/DR5. Sob estresse crônico do RE, tanto células normais quanto células deficientes em REDD1 ativaram vias de estresse upstream de forma semelhante, mas as células sem REDD1 apresentaram um aumento muito maior de TRAILR2/DR5 tanto em nível de RNA quanto de proteína, junto com ativação mais forte da caspase‑8. Silenciar TRAILR2/DR5, mas não um receptor relacionado, reduziu acentuadamente a apoptose nessas células deficientes em REDD1, provando que a resposta de morte aumentada era conduzida principalmente por esse receptor. Em esferoides tumorais tridimensionais, que imitam melhor tumores reais e naturalmente acumulam estresse, os níveis de REDD1 já eram altos e a atividade de mTORC1 era baixa, e remover REDD1 novamente tornou esses mini‑tumores muito mais vulneráveis à morte celular induzida por estresse do RE.
O papel de um freio transcricional
Para entender como REDD1 controla TRAILR2/DR5, a equipe usou sequenciamento de RNA para procurar reguladores cujos níveis mudavam quando REDD1 era perdido. Eles identificaram um fator de transcrição chamado EVI‑1/MECOM, previamente ligado ao crescimento tumoral e à repressão gênica. Em células deficientes em REDD1, os níveis de EVI‑1/MECOM caíram. Reduzir EVI‑1/MECOM em células, por outro lado, tornou-as mais sensíveis ao estresse do RE, aumentou a expressão de TRAILR2/DR5 e induziu apoptose dependente de caspase‑8, mimetizando o efeito da perda de REDD1. Os autores também encontraram que correpressores chamados CtBP1/2, parceiros conhecidos de EVI‑1/MECOM em alguns tumores, podiam ajustar adicionalmente os níveis de TRAILR2/DR5 e a sensibilidade ao estresse de maneira específica para cada tipo celular. Juntos, esses resultados sugerem que REDD1 ajuda a manter a repressão do gene TRAILR2/DR5 mediada por EVI‑1/MECOM, adiando a ativação do interruptor da morte durante estresse prolongado.
O que isso significa para tratamentos futuros do câncer
Para um público leigo, a principal conclusão é que células de câncer de cólon possuem um mecanismo interno que lhes permite “suportar” estresse proteico severo em vez de morrer quando deveriam. A proteína REDD1 age como uma válvula de segurança: ela silencia uma via de crescimento importante e sustenta um sistema de repressão gênica que impede que um potente receptor de morte, TRAILR2/DR5, seja ativado prematuramente. Quando REDD1 ou seu parceiro EVI‑1/MECOM são removidos, células cancerígenas estressadas têm muito mais probabilidade de se autodestruir. Este trabalho sugere que mirar em REDD1 ou em seus correpressores a jusante pode retirar dos tumores esse amortecedor protetor, tornando as células em regiões hostis e pobremente nutridas do tumor mais vulneráveis a terapias que aumentam o estresse do RE e empurram as células para a apoptose.
Citação: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Palavras-chave: estresse do RE, câncer colorretal, apoptose, TRAILR2/DR5, REDD1/DDIT4