Clear Sky Science · ru
REDD1/DDIT4 противостоит апоптозу, вызванному стрессом эндоплазматического ретикулума, контролируя экспрессию рецептора смерти TRAILR2/DR5 в раковых клетках
Почему важны стрессовые опухолевые клетки
Раковые клетки не растут в комфортных условиях. Внутри опухоли клетки испытывают дефицит кислорода, нехватку питательных веществ и накопление повреждённых белков. Под этим давлением некоторые клетки умирают, но другие адаптируются и становятся менее чувствительны к лечению. В этой статье изучается, как клетки колоректального рака переживают один специфический тип внутриклеточного стресса — нарушения в эндоплазматическом ретикулуме, «фабрике» сворачивания белков — и выявляется молекулярный «тормоз», который мешает этим стрессовым клеткам саморазрушаться.
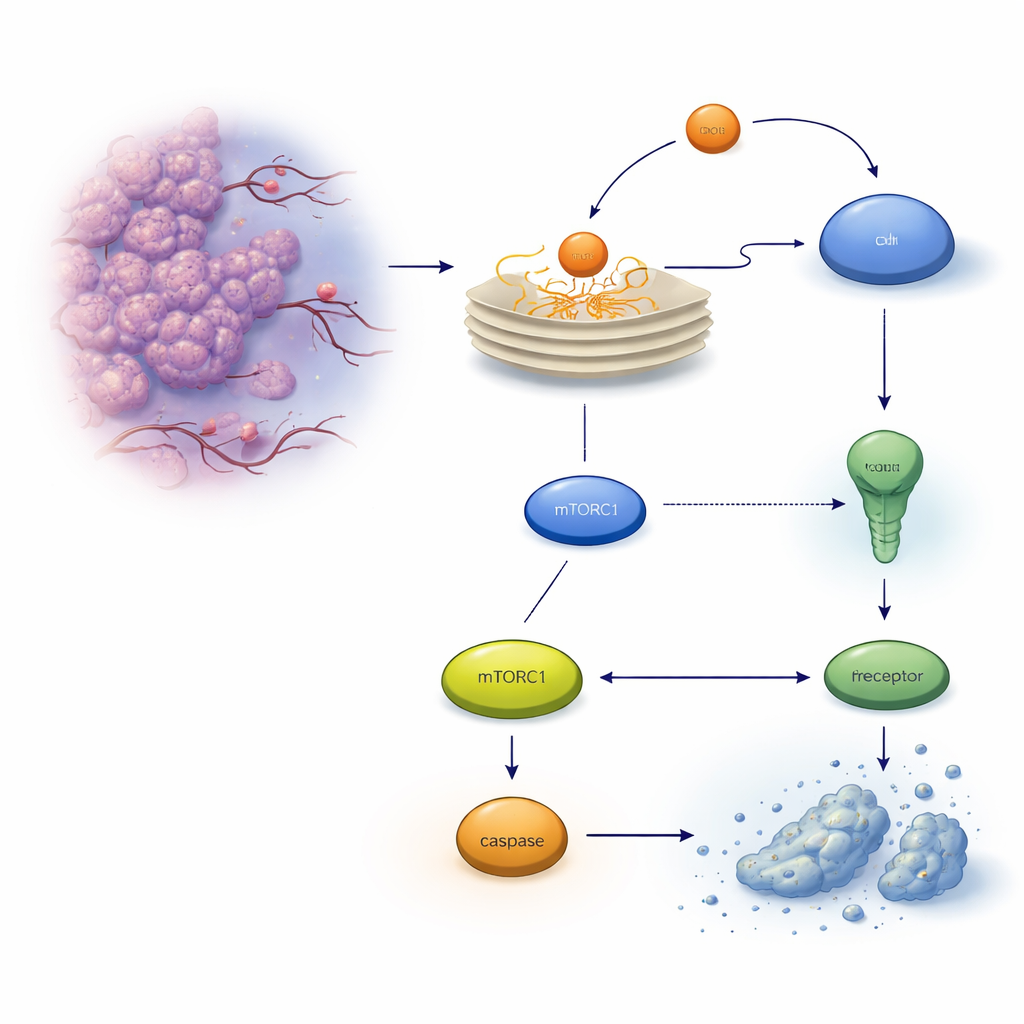
Скрытый клапан безопасности внутри опухолевых клеток
Когда белки неправильно сворачиваются, они накапливаются в эндоплазматическом ретикулуме (ЭР), вызывая систему тревоги, называемую ответом на накопление несвёрнутых белков. Сначала этот ответ пытается восстановить равновесие, но если стресс слишком силён или длится долго, он может переключиться в программу самоуничтожения — апоптоз. В клетках колоректального рака одним из ключевых исполнителей является рецептор смерти на поверхности клетки TRAILR2/DR5, который может активировать протеазу каспазу‑8 и в конечном итоге убить клетку. Авторы сосредоточились на другом индуцируемом стрессом белке, REDD1/DDIT4, уже известном тем, что помогает клеткам адаптироваться к суровым условиям, и выяснили, влияет ли он на это решение — жить или умирать.
Как белок стресса смещает баланс в пользу выживания
Исследователи подвергали линии человеческих клеток колоректального рака воздействию препаратов, вызывающих стресс ЭР, и отслеживали уровни REDD1 со временем. Они обнаружили, что стресс ЭР быстро повышает синтез REDD1 в упорядоченной манере, контролируемой другим стресс‑ответным фактором ATF4. При наличии REDD1 подавлялась активность mTORC1, крупного регулятора роста и биосинтеза белка. Подавление или удаление REDD1 с помощью РНК-интерференции или редактирования генома CRISPR значительно повышало склонность раковых клеток к апоптозу при стрессе ЭР, и это усиленное клеточное гибель можно было блокировать ингибиторами каспаз или фармакологическим подавлением mTORC1, что показывает: REDD1 обычно защищает клетки, сдерживая этот путь роста во время стресса.
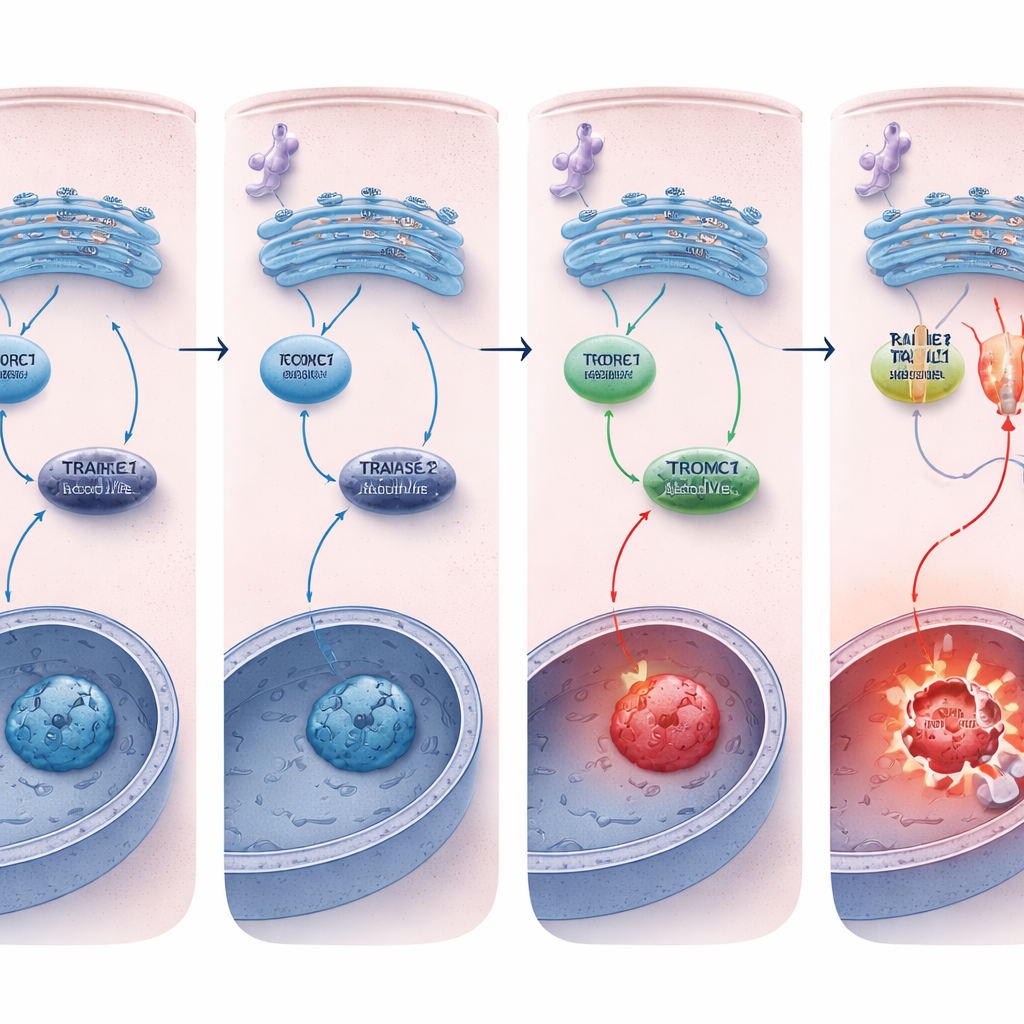
Держать переключатель смерти в пониженном положении
Почему клетки без REDD1 умирали легче? Ключевое отличие оказалось в рецепторе смерти TRAILR2/DR5. При хроническом стрессе ЭР и нормальные, и лишённые REDD1 клетки активировали верхние стресс‑пути примерно одинаково, но в клетках без REDD1 наблюдалось гораздо более сильное повышение TRAILR2/DR5 на уровне РНК и белка, а также более интенсивная активация каспазы‑8. Подавление TRAILR2/DR5, но не родственного рецептора, резко уменьшало апоптоз в этих клетках без REDD1, доказывая, что усиленный ответ смерти в основном опосредован этим рецептором. В трёхмерных опухолевых сфероидах, которые лучше имитируют реальные опухоли и естественно накапливают стресс, уровни REDD1 уже были высоки, а активность mTORC1 — низка; удаление REDD1 вновь делало эти мини‑опухоли значительно более уязвимыми к гибели клеток, вызванной стрессом ЭР.
Роль транскрипционного «тормоза»
Чтобы понять, как REDD1 контролирует TRAILR2/DR5, команда использовала РНК‑секвенирование в поисках регуляторов, чьи уровни менялись при потере REDD1. Они выделили транскрипционный фактор EVI‑1/MECOM, ранее связанный с ростом опухолей и репрессией генов. В клетках без REDD1 уровни EVI‑1/MECOM снижались. Снижение EVI‑1/MECOM в иначе нормальных клетках делало их более чувствительными к стрессу ЭР, увеличивало экспрессию TRAILR2/DR5 и вызывало апоптоз, зависящий от каспазы‑8, имитируя эффект потери REDD1. Авторы также обнаружили, что со‑репрессоры CtBP1/2, известные партнёры EVI‑1/MECOM в некоторых опухолях, могут дополнительно регулировать уровни TRAILR2/DR5 и чувствительность к стрессу в зависимости от типа клетки. В совокупности эти результаты указывают на то, что REDD1 помогает поддерживать репрессию гена TRAILR2/DR5, опосредованную EVI‑1/MECOM, задерживая включение «переключателя смерти» при длительном стрессе.
Что это означает для будущего лечения рака
Для неспециализированной аудитории главное заключение в том, что клетки колоректального рака обладают внутренним механизмом, который позволяет им «пережидать» тяжёлый белковый стресс вместо того, чтобы умирать, когда им следовало бы. Белок REDD1 действует как клапан безопасности: он притупляет крупный путь роста и поддерживает систему репрессии генов, которая не даёт мощному рецептору смерти TRAILR2/DR5 включиться слишком рано. Когда REDD1 или его партнёр EVI‑1/MECOM удаляются, стрессовые раковые клетки гораздо чаще саморазрушаются. Эта работа предполагает, что таргетирование REDD1 или его нижележащих репрессоров может лишить опухоль этой защитной подушки, делая раковые клетки в враждебных, бедных питательными веществами участках опухоли более уязвимыми к терапии, усиливающей стресс ЭР и направленной на индукцию апоптоза.
Цитирование: Mora-Molina, R., El Yousfi, Y., Hagenlocher, C. et al. REDD1/DDIT4 counteracts endoplasmic reticulum stress-induced apoptosis by controlling the expression of death receptor TRAILR2/DR5 in cancer cells. Cell Death Dis 17, 425 (2026). https://doi.org/10.1038/s41419-026-08648-7
Ключевые слова: стресс ЭР, колоректальный рак, апоптоз, TRAILR2/DR5, REDD1/DDIT4