Clear Sky Science · tr
GNE miyopatisinde bozuk otofaji, kanonik olmayan Akt–mTORC1 aktivasyonunun inhibisyonuyla çoklu izojenik modellerde kurtarılır
Kasların kendi kendini temizlemesi neden önemli
Kaslarımız sürekli olarak yıpranmış parçaları yıkar ve yeniden inşa eder. Bu hücresel ev içi temizlik, hücresel geri dönüşüm olarak adlandırılır ve kas liflerini yaşam boyu güçlü tutar. GNE miyopati olarak bilinen nadir kalıtsal bir durumda, genç yetişkinler kas güçlerini yavaşça yitirir; ancak tek bir kusurlu genden başlayan ve kas erimesine yol açan olaylar zinciri belirsiz kalmıştı. Bu çalışma, kök hücre modelleri, genetik olarak düzenlenmiş fare kas hücreleri ve mini nöromüsküler organoidler kullanarak bu zinciri adım adım izliyor: kas hücresinin çevresindeki bozulmuş bir ortamın hücre içindeki geri dönüşümü nasıl kapattığını ve mevcut bir kanser ilacının bunu nasıl yeniden açabileceğini gösteriyor.
Genden zayıf kaslara
GNE miyopati, normalde hücrelerin sialik asit üretmesine yardımcı olan bir gendeki değişikliklerden kaynaklanır; sialik asit birçok yüzey molekülünü süsleyen küçük bir şekerdir. Gen işlevini yitirdiğinde, kas lifleri sialik asit bakımından yetersiz kalır ve sonunda hasta biyopsilerinde mikroskop altında görülen rimli vakuoller adı verilen kabarcık benzeri yapılara dönüşür. Önceki çalışmalar kusurlu hücresel geri dönüşümün sorunun bir parçası olabileceğini ima etmişti, ancak gen kusurundan başarısız geri dönüşüme giden kesin bağlantı bilinmiyordu. Yazarlar, yalnızca ortak bir GNE mutasyonunu taşıyıp taşımamaya göre farklılık gösteren insan kök hücrelerinden elde edilen kas hücrelerinin gen etkinliğini karşılaştırarak işe başladılar. Hastalıklı hücrelerde geri dönüşümle ilgili gen kümelerinde geniş kaymalar gördüler; bu, ev içi temizlik yollarının hastalıklı hücrelerde tutarlı şekilde bozulduğunu düşündürdü.
Eşleşen hücre modelleri oluşturmak
Mekanizmaları derinlemesine incelemek için ekip, standart bir fare miyoblast hattında Gne genini sileyerek daha basit bir kas hücresi sistemi yarattı. Bu mühendislik hücreleri, insan modellerinde ve hastalarda görülen aynı sialik asit eksikliğini gösterdi. Rutin büyüme koşullarında oldukça normal görünseler de, metabolik stresi taklit etmek için şeker kaynakları geri çekildiğinde, kofaktörlüğü ortadan kaldırılan hücreler çok daha kolay ölme eğilimindeydi. Ayrıntılı protein ölçümleri ve görüntüleme, bu stres altındaki hücrelerde otofajozom adı verilen geri dönüşüm yapılarının yetersiz oluştuğunu ve normal materyal akışının hücresel atık bölmelerine doğru engellendiğini ortaya koydu. Bu, GNE eksik kasın enerji talebiyle zorlandığında geri dönüşüm başarısızlığının temel bir zayıflık olduğunu doğruladı.
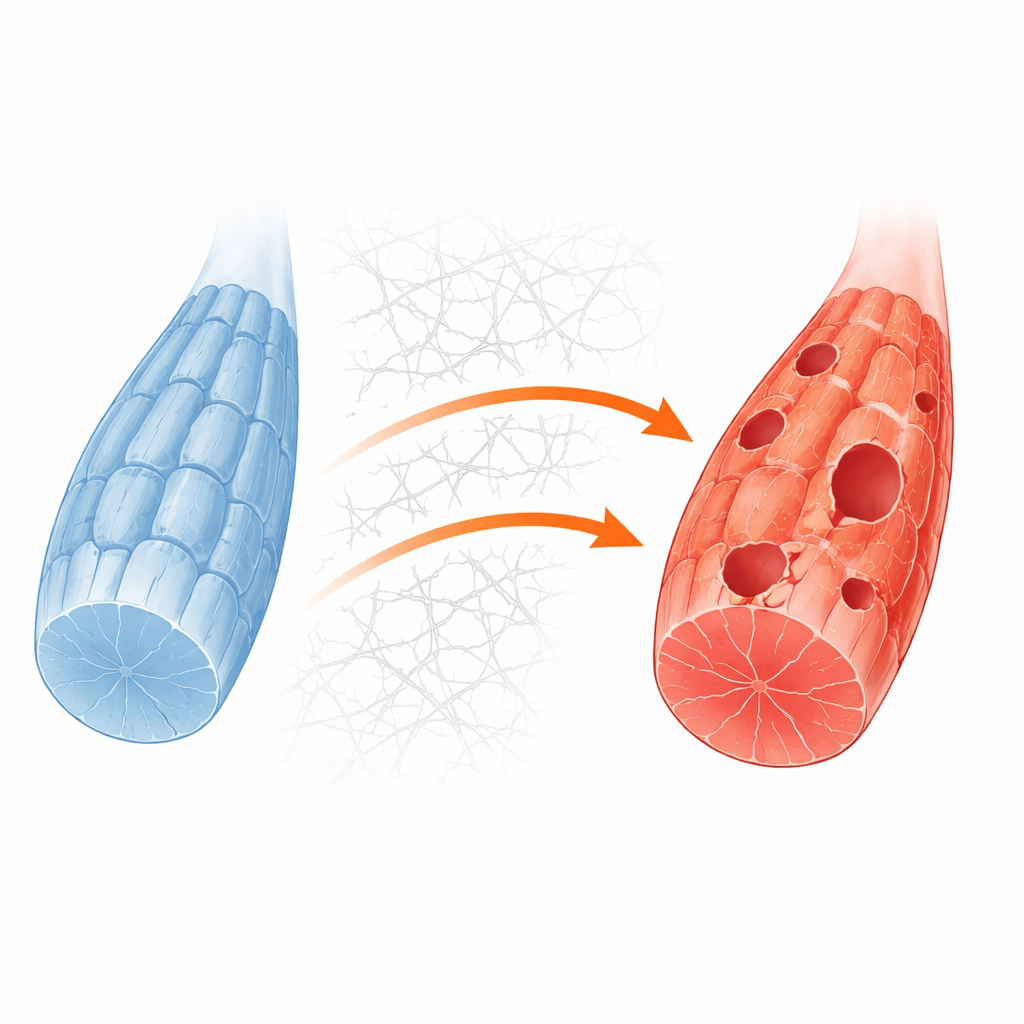
Hücrenin dışı içini nasıl tıkıyor
Araştırmacılar daha sonra geri dönüşümü moleküler düzeyde neyin engellediğini sordular. Analizleri, normalde besin ve büyüme sinyallerine yanıt veren PI3K, AKT ve mTORC1 olarak bilinen proteinlerin yönlendirdiği aşırı aktif bir büyüme kontrol yoluna işaret etti. Sağlıklı kaslarda enerji kıtlığı bu yolu susturur ve ULK1 adlı başlatıcı bir enzimin geri dönüşümü tetiklemesine izin verir. Ancak GNE eksik hücrelerde, yol açlık sırasında bile açık kaldı. Aynı zamanda hücreler kollajen ve çevresel iskelenin diğer bileşenlerini aşırı üretti. Bu aşırı iskelet hücre yüzeyi ile çevresi arasındaki temas noktalarını güçlendirdi; bu da odak adezyon kinazı adlı bir röle molekülünü aktive ederek PI3K–AKT–mTORC1 yoluna besleme sağladı. Sonuç, ULK1 üzerinde geri dönüşümü başlatmayı engelleyen ve onu kapalı tutan kalıcı bir kimyasal işaretti.
Freni gevşeten bir ilacı test etmek
Bu devre şemasıyla donanmış ekip, hastalık imzasına zıt etkileri olan ilaçları bulmak için geniş bir ilaç kaynaklı gen değişikliği veri tabanını taradı. En üstteki birçok aday PI3K veya mTOR inhibitörleriydi ve belirli lenfomalar için onaylı intravenöz bir PI3K inhibitörü olan copanlisib’i daha ileri testler için seçtiler. GNE knockout fare kas hücrelerinde copanlisib, aşırı aktif yol sinyalini azalttı, ULK1 üzerindeki inhibitör etiketi kaldırdı ve orijinal sialik asit eksikliğini düzeltmemesine rağmen geri dönüşüm aktivitesini geri getirdi. Yazarlar daha sonra GNE mutasyonunu taşıyan insan kök hücrelerinden yetiştirilen üç boyutlu nöromüsküler organoidlere döndüler. Bu mini kas- sinir üniteleri düşük sialik asit düzeylerini, geri dönüşüm kusurlarını ve mTORC1 aşırıaktivitesini yeniden üretti. Besin stresi sırasında copanlisib ile muamele edildiğinde, hasta organoidlerde kas lifleri içinde çok daha fazla geri dönüşüm ponctasi oluştu; bu da ev içi temizliğin canlandığını gösteriyordu.
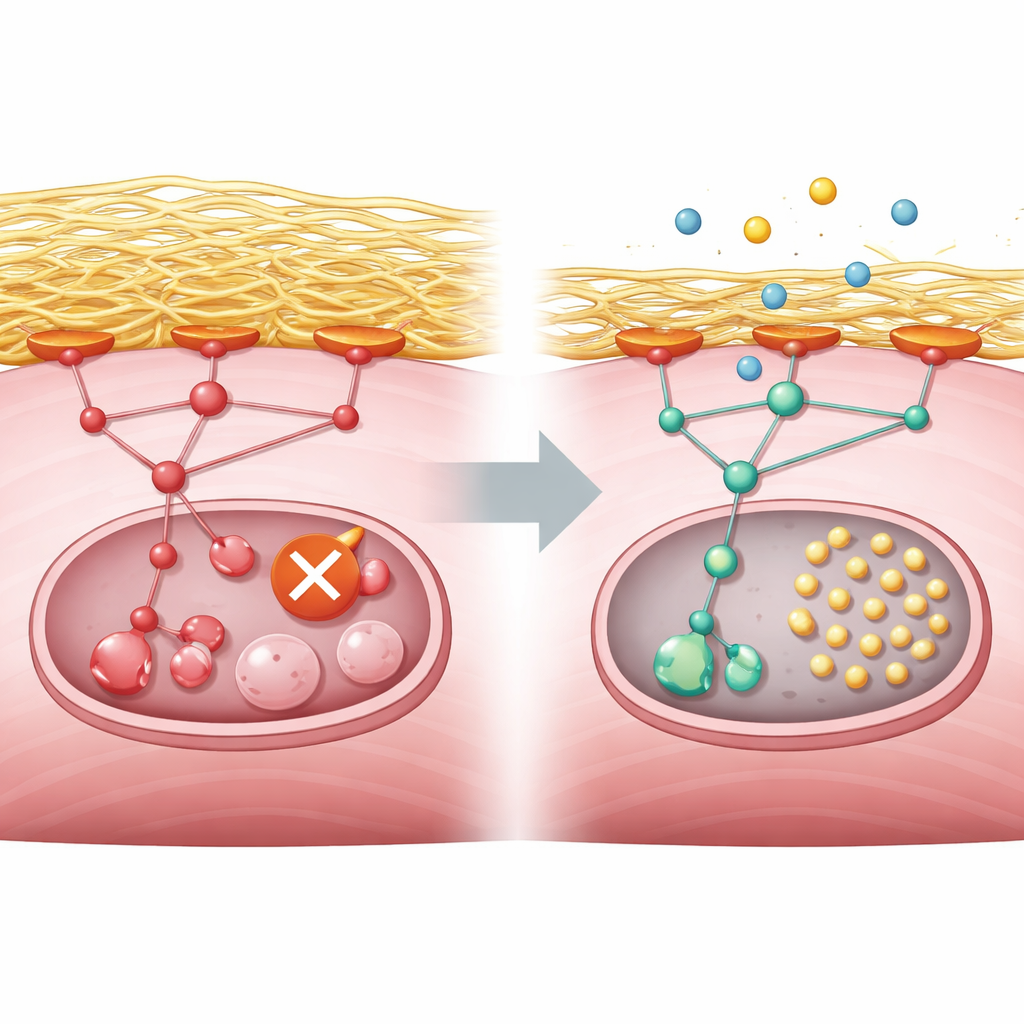
GNE miyopatili kişiler için bunun anlamı
Basitçe söylemek gerekirse, bu çalışma kas hücrelerindeki kusurlu bir şeker üretim genini çevresel iskelenin aşırı birikimine bağlıyor; bu da bir büyüme kontrol yolunu aşırı uyarıyor ve hücrenin temizleme ekibini kapatıyor. Çalışma, bu aynı desenin mühendislik fare hücrelerinde, insan kök hücre kaynaklı kas ve organoidlerde ve hasta biyopsilerinin gen etkinliğinde göründüğünü gösteriyor. Copanlisib henüz GNE miyopati için bir tedavi olmasa da, deneyler PI3K–AKT–mTORC1 yolunun dikkatli şekilde aşağı çekilmesinin geri dönüşüm blokajını hafifletebileceğini ve muhtemelen kas hasarını yavaşlatabileceğini öne sürüyor. Gelecek klinik çalışmalar bu yaklaşımın insanlarda güvenli ve etkili olup olmadığını belirlemeli, ancak çalışma terapötik olarak test edilebilir açık bir hedef sunuyor.
Atıf: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
Anahtar kelimeler: GNE miyopati, kas otofajisi, ekstraselüler matris, AKT mTORC1 yolu, copanlisib