Clear Sky Science · de
Defekte Autophagie bei GNE-Myopathie wird durch Hemmung nichtkanonischer Akt–mTORC1-Aktivierung in mehreren isogenen Modellen gerettet
Warum die Selbstreinigung der Muskeln wichtig ist
Unsere Muskeln bauen ständig abgenutzte Bestandteile ab und bauen sie wieder auf. Diese interne Haushaltsführung, als zelluläres Recycling bezeichnet, erhält die Kraft der Muskelfasern ein Leben lang. Bei einer seltenen erblichen Erkrankung, der sogenannten GNE-Myopathie, verlieren junge Erwachsene allmählich an Muskelkraft, doch die Abfolge der Ereignisse, die von einem einzigen fehlerhaften Gen zur Muskelatrophie führt, war bisher unklar. Diese Studie verfolgt diese Abfolge Schritt für Schritt und zeigt mithilfe von Stammzellmodellen, gentechnisch veränderten Mausmuskelzellen und miniaturisierten neuromuskulären Organoiden, wie eine gestörte Umgebung um die Muskelzelle das Recycling innerhalb der Zelle abschalten kann und wie ein bereits zugelassenes Krebsmedikament helfen könnte, es wieder einzuschalten.
Vom Genfehler zur Muskelschwäche
Die GNE-Myopathie wird durch Veränderungen in einem Gen verursacht, das normalerweise Zellen bei der Herstellung von Sialinsäure unterstützt, einem kleinen Zucker, der viele Oberflächenmoleküle schmückt. Versagt das Gen, sind Muskelfasern unterversorgt mit Sialinsäure und entwickeln schließlich randbegrenzte Vakuolen, blasenähnliche Strukturen, die in Patientenbiopsien unter dem Mikroskop zu sehen sind. Frühere Arbeiten deuteten an, dass fehlerhaftes zelluläres Recycling Teil des Problems sein könnte, doch die genaue Verkettung vom Gendefekt bis zum gestörten Recycling war unbekannt. Die Autorinnen und Autoren begannen damit, die Genaktivität in Muskelzellen zu vergleichen, die aus menschlichen Stammzellen gezüchtet wurden und sich nur darin unterschieden, ob sie eine häufige GNE-Mutation trugen. Sie beobachteten weitreichende Verschiebungen in Gen-Sets, die mit Recycling zu tun haben, was darauf hindeutet, dass die Haushaltswege in erkrankten Zellen konsistent gestört sind.
Aufbau passender Zellmodelle
Um die Mechanismen zu untersuchen, erzeugte das Team ein vereinfachtes Muskelzell-System, indem es das Gne-Gen in einer standardisierten Mausmyoblastenlinie löschte. Diese gentechnisch veränderten Zellen zeigten denselben Mangel an Sialinsäure wie die menschlichen Modelle und die Patientenzellen. Unter Routinezuchtbedingungen wirkten sie ziemlich normal, doch als Zuckerversorgung entzogen wurde, um metabolischen Stress zu simulieren, starben die Knockout-Zellen deutlich häufiger. Detaillierte Proteinmessungen und Bildgebung zeigten, dass in diesen gestressten Zellen Recyclingstrukturen, sogenannte Autophagosomen, schlecht gebildet wurden und der normale Fluss von Material in zelluläre Abfallkompartimente gebremst war. Dies bestätigte, dass ein Versagen des Recyclings eine zentrale Schwäche ist, die bei GNE-defizientem Muskel unter erhöhtem Energiebedarf zum Vorschein kommt.
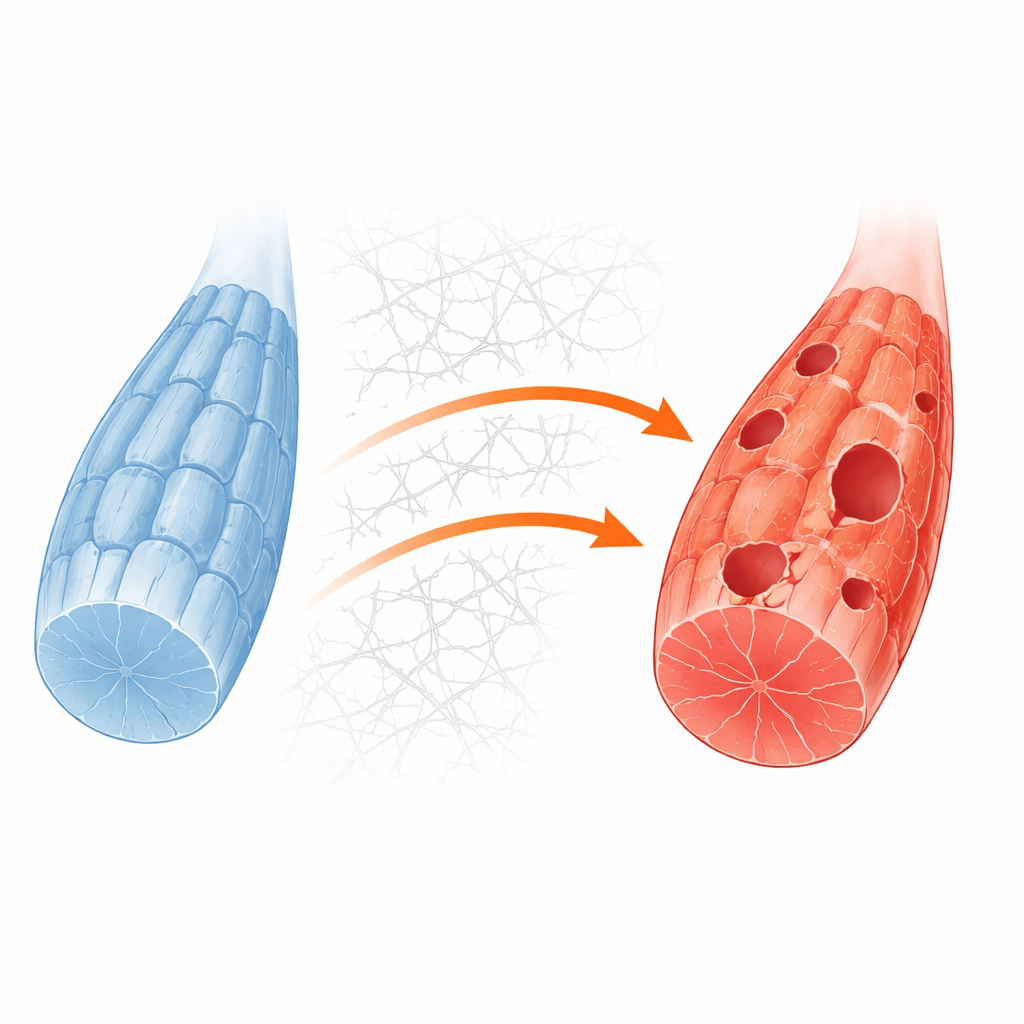
Wie das Zelläußere das Innere blockiert
Die Forscher fragten als Nächstes, was das Recycling auf molekularer Ebene blockierte. Ihre Analysen deuteten auf einen überaktiven Wachstumssteuerungsweg hin, der von Proteinen angetrieben wird, die als PI3K, AKT und mTORC1 bekannt sind und normalerweise auf Nährstoffe und Wachstumsreize reagieren. In gesundem Muskel dämpft Energiemangel diesen Weg und erlaubt einem Starterenzym namens ULK1, das Recycling zu initiieren. In GNE-defizienten Zellen blieb der Weg jedoch auch während der Nahrungsdeprivation eingeschaltet. Gleichzeitig produzierten die Zellen vermehrt Kollagen und andere Bestandteile des umgebenden Gerüsts, der extrazellulären Matrix. Dieses überschüssige Gerüst verstärkte Kontaktpunkte zwischen Zelloberfläche und Umgebung, was wiederum eine Relay-Kinase namens Focal Adhesion Kinase aktivierte und in den PI3K–AKT–mTORC1-Weg einspeiste. Das Ergebnis war ein persistentes chemisches Markierungszeichen auf ULK1, das es in einem ausgeschalteten Zustand hält und verhindert, dass das Recycling überhaupt beginnt.
Test eines Medikaments, das die Bremse löst
Mit diesem Schaltplan suchte das Team in einer großen Datenbank von durch Medikamente induzierten Genveränderungen nach Wirkstoffen, deren Effekte dem Krankheitssignaturbild entgegengesetzt sind. Viele der obersten Treffer waren Inhibitoren von PI3K oder mTOR, und sie wählten Copanlisib, einen zugelassenen intravenösen PI3K-Inhibitor, der bei bestimmten Lymphomen eingesetzt wird, für weiterführende Tests aus. In GNE-Knockout-Mausmuskelzellen reduzierte Copanlisib das überaktive Signalsystem, entfernte das inhibitorische Tag von ULK1 und stellte die Recyclingaktivität wieder her, obwohl es den ursprünglichen Sialinsäuremangel nicht reparierte. Die Autorinnen und Autoren wandten sich dann dreidimensionalen neuromuskulären Organoiden zu, die aus menschlichen Stammzellen mit der GNE-Mutation gezüchtet wurden. Diese miniaturisierten Muskel-Nerv-Einheiten reproduzierten niedrige Sialinsäurewerte, Recyclingdefekte und mTORC1-Überaktivität. Wurden die erkrankten Organoide während Nährstoffmangels mit Copanlisib behandelt, bildeten sie deutlich mehr Recycling-Punktstrukturen innerhalb der Muskelfasern, was auf eine wiederbelebte Haushaltsfunktion hindeutet.
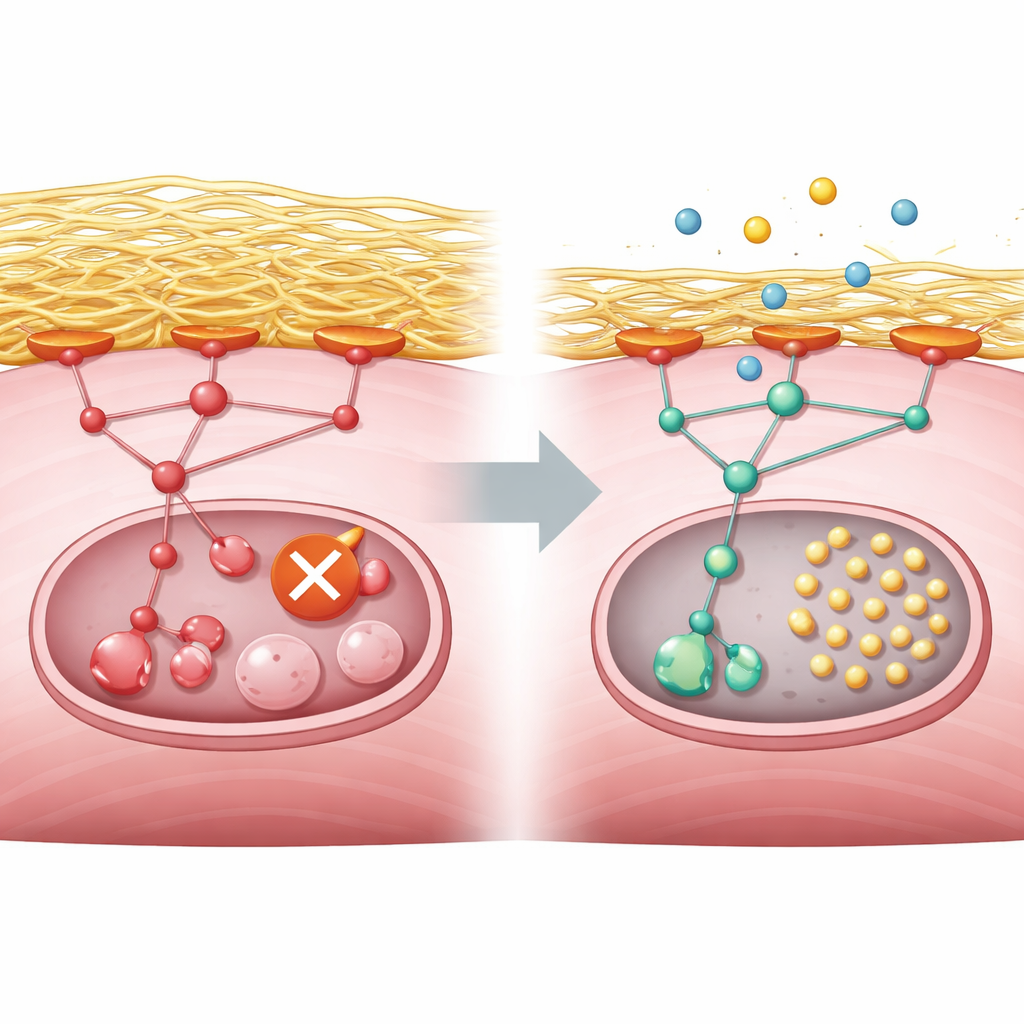
Was das für Menschen mit GNE-Myopathie bedeutet
Kurz gesagt verbindet diese Arbeit ein fehlerhaftes Zuckerherstellungsgen in Muskelzellen mit einer übermäßigen Anhäufung des umgebenden Gerüsts, das einen Wachstumssteuerungsweg überstimuliert und die zelluläre Reinigung abschaltet. Die Studie zeigt, dass dieses Muster in gentechnisch veränderten Mauszellen, aus menschlichen Stammzellen gewonnenen Muskeln und Organoiden sowie in der Genaktivität aus Patientenbiopsien auftritt. Copanlisib ist zwar noch keine Behandlung für GNE-Myopathie, die Experimente legen jedoch nahe, dass ein gezieltes Herunterfahren des PI3K–AKT–mTORC1-Wegs die Recyclingblockade lösen und den Muskelschaden möglicherweise verlangsamen könnte. Künftige klinische Studien müssen klären, ob dieser Ansatz beim Menschen sicher und wirksam ist, doch die Arbeit liefert ein klares und testbares Therapieziel.
Zitation: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
Schlüsselwörter: GNE-Myopathie, Muskelautophagie, extrazelluläre Matrix, AKT–mTORC1-Signalweg, Copanlisib