Clear Sky Science · ar
إصلاح العطب في البلعمة الذاتية بمرض GNE عبر تثبيط تنشيط AKT–mTORC1 غير الكلاسيكي عبر نماذج متماثلة وراثياً متعددة
لماذا يهم تنظيف العضلات الذاتي
تتفكك عضلاتنا باستمرار وتعيد بناء الأجزاء المتآكلة. هذا العمل الداخلي للتنظيف، الذي يسمى إعادة تدوير الخلايا، يحافظ على قوة ألياف العضلات عبر العمر. في حالة وراثية نادرة تعرف باعتلال GNE العضلي، يفقد البالغون الصغار القوة العضلية تدريجياً، ومع ذلك ظل مسار الأحداث من جين معطوب واحد إلى ضمور العضلات غير واضح. تتبع هذه الدراسة ذلك المسار خطوة بخطوة، مستخدمة نماذج من الخلايا الجذعية، وخلايا عضلية فأرية معدّلة ونماذج عصبية عضلية مصغرة لتوضيح كيف يمكن لبيئة مضطربة حول الخلية العضلية أن تطفئ آلية إعادة التدوير بداخلها، وكيف قد يساعد دواء موجود بالفعل على إعادة تشغيلها.
من تغير جيني إلى ضعف العضلات
ينجم اعتلال GNE العضلي عن تغيّرات في جين يساعد عادة الخلايا على صنع حمض السياليك، وهو سكر صغير يزين العديد من الجزيئات السطحية. عندما يتعطل الجين، تعاني ألياف العضلات نقصاً في حمض السياليك وتطور في نهاية المطاف حويصلات محيطة بالحواف، وهي هياكل شبيهة بالفقاعات تُرى تحت المجهر في خزعات المرضى. أشارت أعمال سابقة إلى أن خللاً في إعادة التدوير الخلوي قد يكون جزءاً من المشكلة، لكن التوصيل الدقيق من عطل الجين إلى فشل إعادة التدوير كان غير معلوم. بدأ المؤلفون بمقارنة نشاط الجينات في خلايا عضلية مكوّنة من خلايا جذعية بشرية اختلفت فقط بوجود طفرة شائعة في GNE. لاحظوا تغيّرات واسعة في مجموعات الجينات المتعلقة بإعادة التدوير، ما يوحي بأن مسارات التنظيف كانت مضطربة بشكل ثابت في الخلايا المريضة.
بناء نماذج خلوية مطابقة
للتعمق في الآليات، أنشأ الفريق نظام خلايا عضلية أبسط بحذف جين Gne في سلالة قياسية من خلايا الميو بلاست الفأرية. أظهرت هذه الخلايا المعدّلة نفس نقص حمض السياليك الذي لوحظ في النماذج البشرية والمرضى. تحت ظروف النمو الروتينية بدت الخلايا اعتيادية إلى حد ما، لكن عندما سُحبت الإمدادات السكرية لمحاكاة الإجهاد الأيضي، كانت الخلايا المحذوفة أكثر عرضة للموت. كشفت قياسات البروتين الدقيقة والتصوير أن هياكل إعادة التدوير المسماة الحويصلات البلعومية تشكلت بشكل ضعيف، وتدفق المواد الطبيعي إلى مقصورات النفايات الخلوية كان معطلاً. أكد ذلك أن فشل إعادة التدوير هو نقطة ضعف أساسية تتكشف عندما تُدفع العضلات الناقصة GNE بحاجات طاقية.
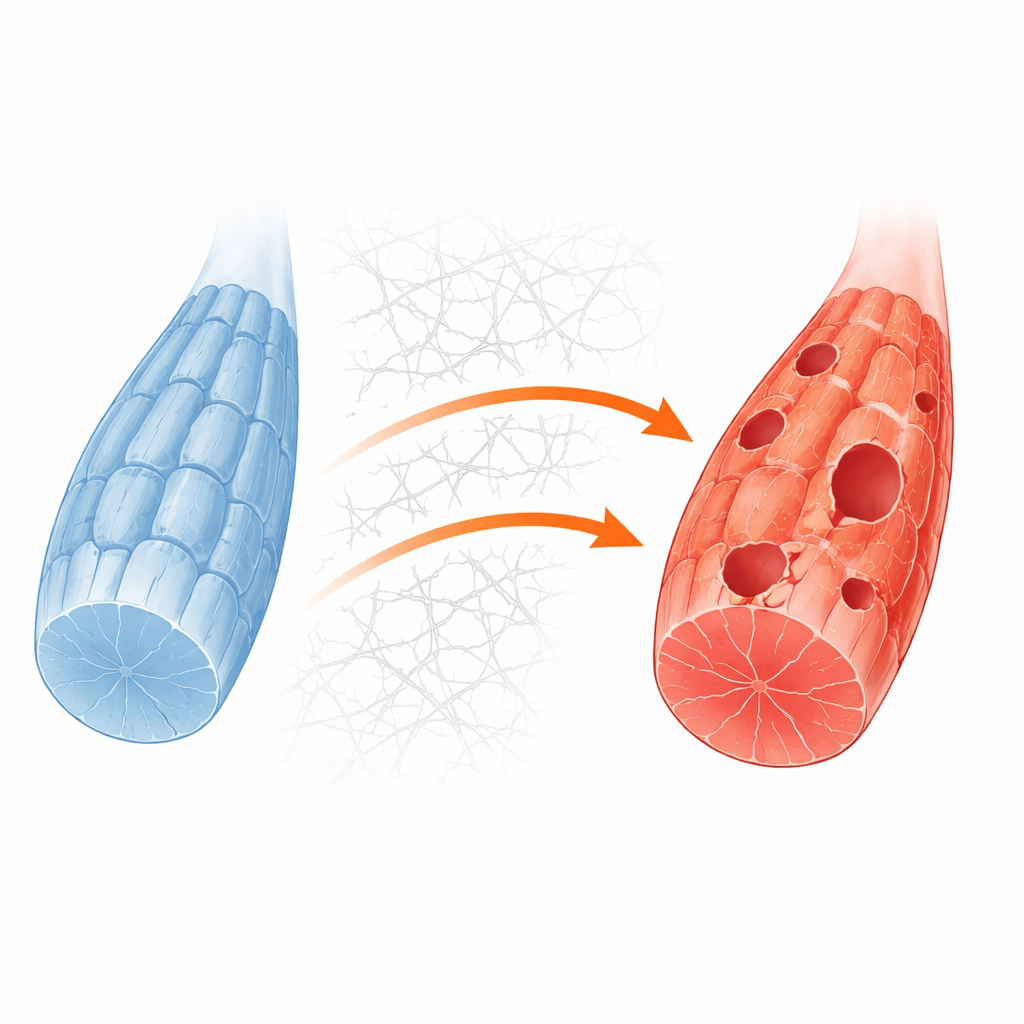
كيف تعطل البيئة الخارجية الداخل
سأل الباحثون بعد ذلك ما الذي يعيق إعادة التدوير على المستوى الجزيئي. أشارت تحليلاتهم إلى فرط نشاط في مسار التحكم بالنمو الذي يقوده بروتينات معروفة باسم PI3K وAKT وmTORC1، والتي تستجيب عادة للمغذيات وإشارات النمو. في العضلات السليمة، يؤدي نقص الطاقة إلى كبح هذا المسار ويسمح لإنزيم بادئ يسمى ULK1 بإطلاق عملية إعادة التدوير. في الخلايا الناقصة GNE، ظل المسار مفعلاً حتى أثناء الجوع. في الوقت نفسه، أنتجت الخلايا كولاجين ومكونات أخرى من السقالة المحيطة أكثر من اللازم. عززت هذه السقالة الزائدة نقاط التماس بين سطح الخلية وبيئتها، مما فعّل جزيئاً ناقلاً يُدعى كيناز الالتصاق البؤري (focal adhesion kinase) وضمّ إلى مسار PI3K–AKT–mTORC1. كانت النتيجة وسم كيميائي دائم على ULK1 يبقيه في حالة إيقاف، مانعاً بدء إعادة التدوير.
اختبار دواء يخفف المكبح
مسلحين بهذا المخطط الوصفي، بحث الفريق في قاعدة بيانات كبيرة لتغيرات الجينات المحفزة بالأدوية عن أدوية تكون آثارها معاكسة لتوقيع المرض. كان كثير من النتائج الأفضل هي مثبطات PI3K أو mTOR، فاختاروا كوبانليسيب، وهو مثبط وريدِي معتمد لـ PI3K يُستخدم في بعض أنواع اللمفوما، لاختبارات إضافية. في خلايا عضلية فأرية محذوفة GNE خفّض كوبانليسيب إشارة المسار المفرطة، أزاح الوسم المثبط من ULK1 وأعاد نشاط إعادة التدوير، رغم أنه لم يصلح نقص حمض السياليك الأصلي. انتقل المؤلفون بعد ذلك إلى أعضاء عصبية-عضلية ثلاثية الأبعاد نمت من خلايا جذعية بشرية تحمل طفرة GNE. reproduced هذه الوحدات المصغرة مستويات منخفضة من حمض السياليك، وعيوب في إعادة التدوير وفرط نشاط mTORC1. عند معالجتها بكوبانليسيب خلال الإجهاد الغذائي، شكلت العضيدات المريضة نقاط إعادة تدوير داخل ألياف العضلات أكثر بكثير، ما يشير إلى استئناف أعمال التنظيف.
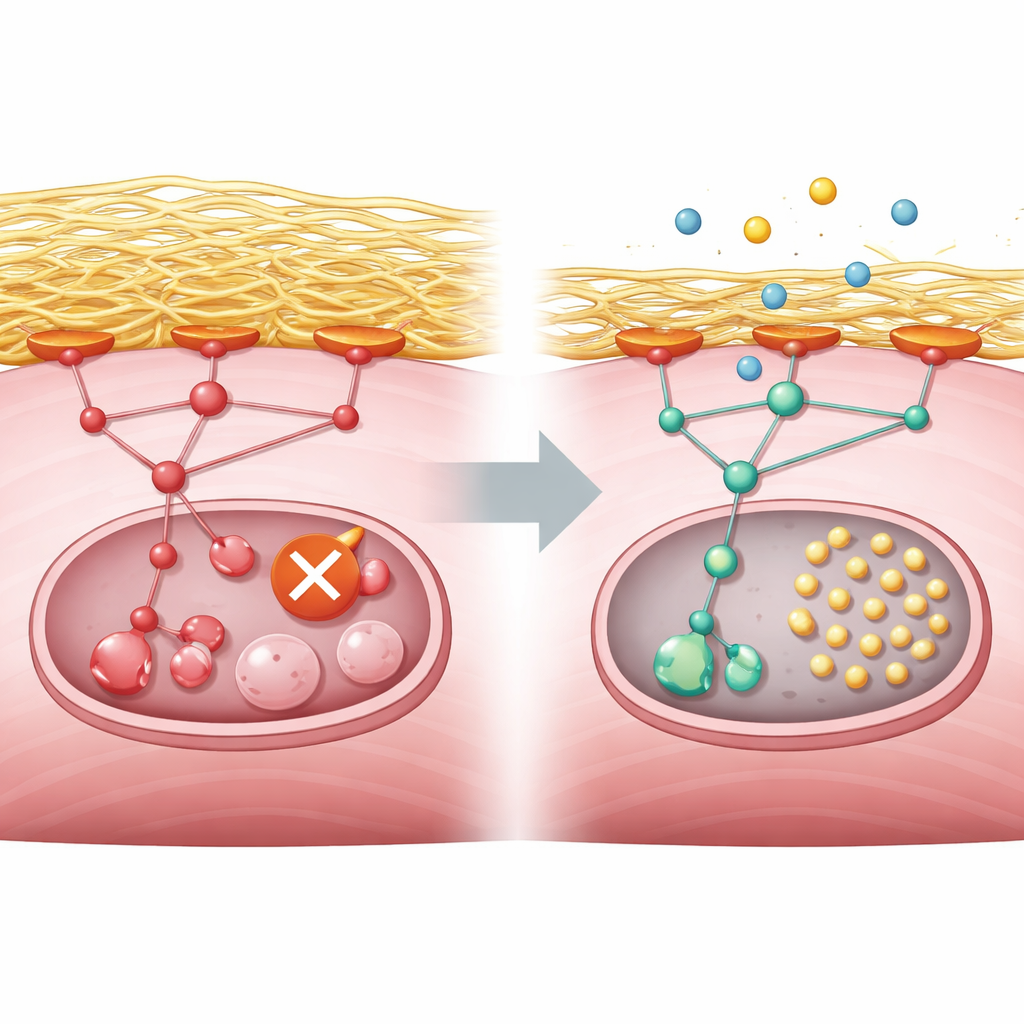
ما يعنيه هذا للأشخاص المصابين باعتلال GNE
باختصار، تربط هذه الدراسة جيناً معطوباً لصنع السكر في خلايا العضلات بتراكم مفرط للسقالة المحيطة، الذي يفرط في تنشيط مسار التحكم بالنمو ويُطفئ طاقم تنظيف الخلية. تظهر نفس الخريطة في خلايا فأرية معدّلة، وفي عضلات مشتقة من خلايا جذعية بشرية والعضيدات، وفي نشاط الجينات من خزعات المرضى. بينما لا يُعد كوبانليسيب علاجاً معتمداً لاعتلال GNE العضلي بعد، تشير التجارب إلى أن تخفيف نشاط مسار PI3K–AKT–mTORC1 بعناية قد يرفع الحاجز أمام إعادة التدوير وربما يبطئ تلف العضلات. ستحتاج الدراسات السريرية المستقبلية إلى تحديد ما إذا كانت هذه المقاربة آمنة وفعالة لدى البشر، لكن العمل يقدّم هدفاً واضحاً وقابلاً للاختبار للعلاج.
الاستشهاد: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
الكلمات المفتاحية: اعتلال عضلي GNE, البلعمة الذاتية في العضلات, المصفوفة خارج الخلوية, مسار AKT–mTORC1, كوبانليسيب