Clear Sky Science · sv
Defekt autofagi vid GNE-myopati återställs genom hämning av icke-kanonisk Akt–mTORC1-aktivering i flera isogena modeller
Varför muskelns egen städning är viktig
Våra muskler bryter ständigt ned utslitna delar och bygger upp dem igen. Denna interna städning, kallad cellulär återvinning, håller muskelfibrerna starka livet igenom. I en sällsynt ärftlig sjukdom som heter GNE-myopati förlorar unga vuxna gradvis muskelstyrka, men kedjan av händelser som leder från en enda defekt gen till muskelförtvining har varit oklar. Denna studie följer den kedjan steg för steg, med stamcellsmodeller, modifierade muskelceller från mus och små neuromuskulära organoider, för att visa hur en störd omgivning runt muskelcellen kan slå av återvinningen inne i cellen och hur ett befintligt cancerläkemedel skulle kunna hjälpa till att slå på den igen.
Från genförändring till svaga muskler
GNE-myopati orsakas av förändringar i en gen som normalt hjälper celler att tillverka sialinsyra, en liten sockerart som dekorerar många ytmolekyler. När genen sviktar blir muskelfibrerna underförsedda med sialinsyra och utvecklar så småningom rimmed vacuoler, bubbelliknande strukturer som ses i patientbiopsier. Tidigare arbete antydde att defekt cellulär återvinning kan vara en del av problemet, men den precisa kopplingen från genfel till misslyckad återvinning var okänd. Författarna började med att jämföra genaktivitet i muskelceller odlade från mänskliga stamceller som bara skilde sig åt i om de bar en vanlig GNE‑mutation. De såg breda skift i genset relaterade till återvinning, vilket tyder på att städrutiner konsekvent var störda i sjuka celler.
Bygga matchande cellmodeller
För att gå djupare i mekanismerna skapade teamet ett enklare muskelsystem genom att ta bort Gne-genen i en standardiserad musmyoblastlinje. Dessa konstruerade celler visade samma brist på sialinsyra som sågs i humana modeller och hos patienter. Under rutinmässiga odlingsförhållanden såg de ganska normala ut, men när sockertillförseln drogs ned för att efterlikna metabol stress var knock‑out‑cellerna mycket mer benägna att dö. Detaljerade proteinmätningar och avbildning visade att i dessa stressade celler bildades återvinningsstrukturer kallade autofagosomer dåligt och det normala flödet av material in i cellens avfallscompartments var bromsat. Detta bekräftade att återvinningssvikt är en grundläggande svaghet som avslöjas när GNE‑bristiga muskler pressas av energibrist.
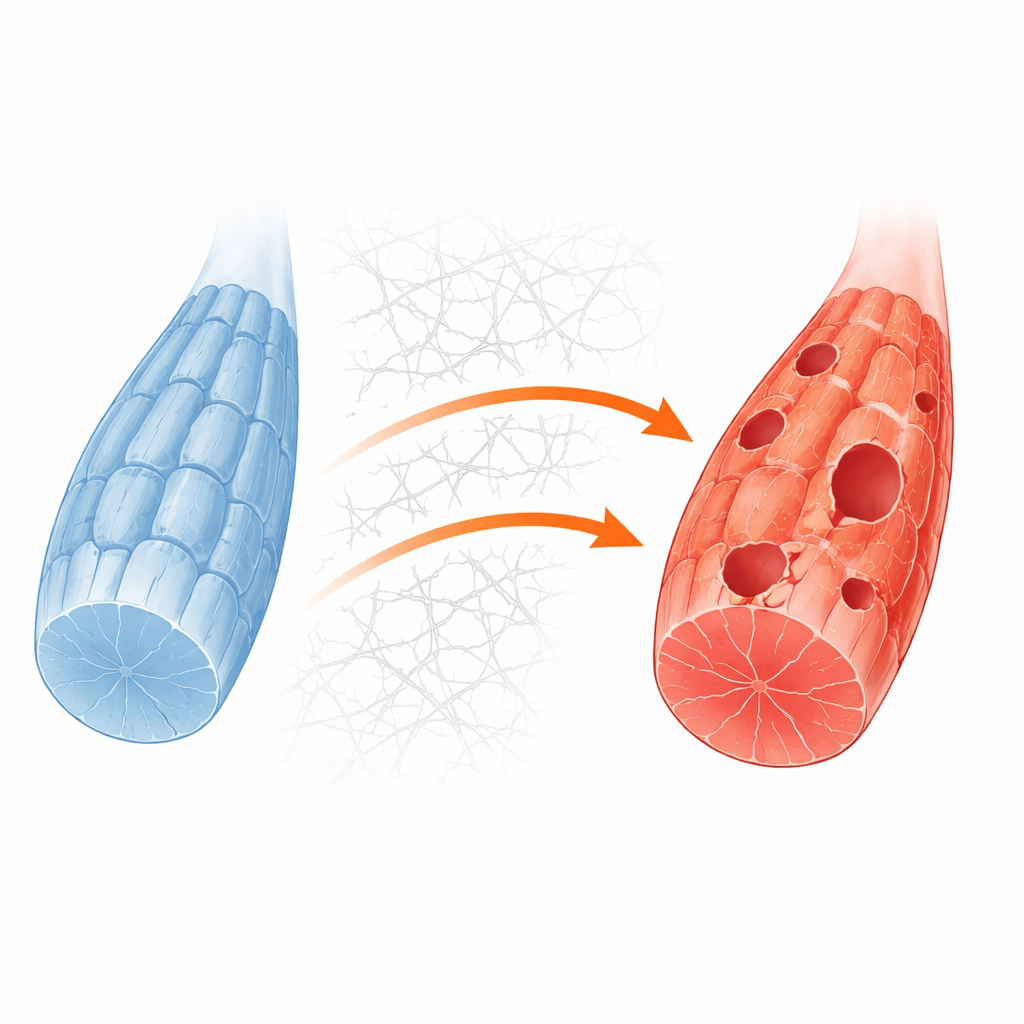
Hur cellens utsida blockerar insidan
Forskarnas nästa fråga var vad som molekylärt blockerade återvinningen. Deras analyser pekade på en överaktiv tillväxtkontrollväg driven av proteiner kända som PI3K, AKT och mTORC1, som normalt reagerar på näringsstatus och tillväxtsignaler. I frisk mus tystnar denna väg vid energibrist och tillåter ett startenzym kallat ULK1 att trigga återvinningen. I GNE‑deficienta celler förblev vägen emellertid påslagen även under svält. Samtidigt överproducerade cellerna kollagen och andra komponenter i den omgivande stödmatrixen, extracellulär matrix. Detta överskott av stödstruktur stärkte kontaktpunkterna mellan cellsytan och omgivningen, vilket i sin tur aktiverade ett relämolekyl kallad focal adhesion kinase och matade in i PI3K–AKT–mTORC1‑vägen. Resultatet blev en bestående kemisk markör på ULK1 som håller det i avstängt läge och förhindrar att återvinningen ens startar.
Test av ett läkemedel som lossar bromsen
Med denna kopplingsschema sökte teamet i en stor databas över läkemedelsinducerade genförändringar för att hitta läkemedel vars effekter gick tvärt emot sjukdomssignaturen. Många av toppkandidaterna var hämmare av PI3K eller mTOR, och de valde copanlisib, en godkänd intravenös PI3K‑hämmare som används för vissa lymfom, för vidare tester. I GNE‑knockout muskelceller minskade copanlisib den överaktiva signalsignaturen, tog bort den hämmande märkningen från ULK1 och återställde återvinningsaktiviteten, även om det inte reparerade den ursprungliga bristen på sialinsyra. Författarna gick sedan över till tredimensionella neuromuskulära organoider odlade från mänskliga stamceller med GNE‑mutationen. Dessa mini‑muskel‑nerv‑enheter reproducerade låga sialinsyranivåer, återvinningsdefekter och mTORC1‑överaktivitet. När de behandlades med copanlisib under näringsstress bildade de sjuka organoiderna många fler återvinningspunkter inne i muskelfibrerna, vilket indikerar återupplivad städning.
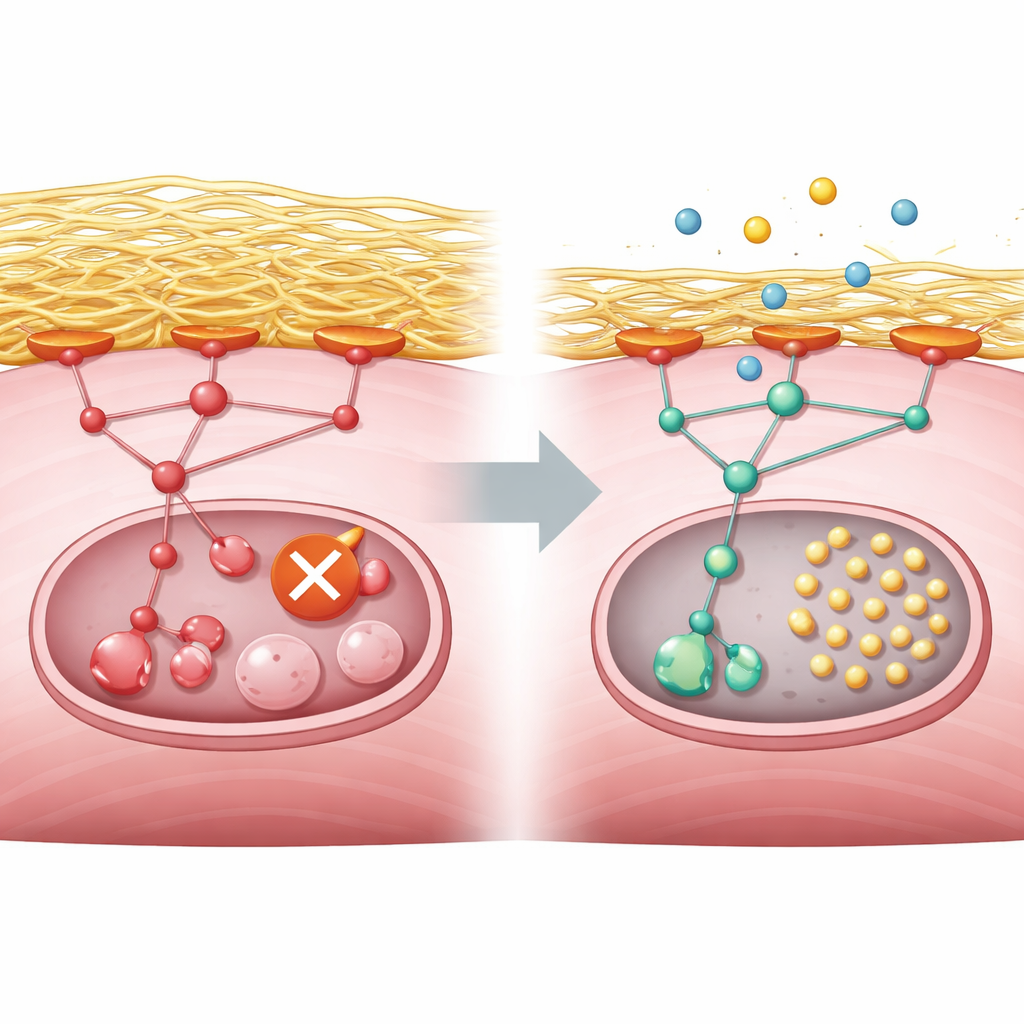
Vad detta betyder för personer med GNE‑myopati
Enkelt uttryckt kopplar detta arbete en felaktig sockertillverkande gen i muskelceller till överdriven uppbyggnad av omkringliggande stödstruktur, vilket överstimulerar en tillväxtkontrollväg och stänger av cellens städpatrull. Studien visar att detta mönster uppträder i konstruerade musceller, humana stamcells‑deriverade muskler och organoider, samt i genaktivitet från patientbiopsier. Fastän copanlisib ännu inte är en behandling för GNE‑myopati tyder experimenten på att en noggrant avvägd nedreglering av PI3K–AKT–mTORC1‑vägen skulle kunna lätta återvinningsblocket och potentiellt bromsa muskelskadan. Framtida kliniska studier måste avgöra om detta tillvägagångssätt är säkert och effektivt hos människor, men arbetet ger ett tydligt, testbart mål för terapi.
Citering: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
Nyckelord: GNE-myopati, muskelautofagi, extracellulär matrix, AKT mTORC1-väg, copanlisib