Clear Sky Science · ru
Дефектный аутофагический механизм при миопатии GNE восстанавливается ингибированием неклассической активации Akt–mTORC1 в нескольких изогенных моделях
Почему важно «самоуборка» мышц
Наши мышцы постоянно разрушают изношенные компоненты и восстанавливают их. Эта внутренняя уборка, называемая клеточной переработкой или аутофагией, поддерживает прочность мышечных волокон на протяжении жизни. При редком наследственном заболевании, известном как миопатия GNE, у молодых взрослых постепенно снижается сила мышц, однако цепочка событий от одной дефектной копии гена до атрофии мышц оставалась неясной. В этом исследовании авторы прослеживают эту цепочку шаг за шагом, используя модели на основе стволовых клеток, генетически модифицированные мышечные клетки мышей и миниатюрные нейромышечные органоиды, чтобы показать, как нарушенная внешняя среда вокруг мышечной клетки может выключать внутриклеточную переработку и как существующий препарат против рака может помочь вновь её запустить.
От изменения гена к ослабленным мышцам
Миопатия GNE вызвана изменениями в гене, который обычно помогает клеткам синтезировать сиаловую кислоту — небольшой сахар, украшающий многие молекулы на поверхности клетки. Когда ген функционирует неправильно, мышечные волокна лишаются достаточного количества сиаловой кислоты и в конечном итоге развивают ободковидные вакуоли — пузырьковидные структуры, видимые под микроскопом в биоптатах пациентов. Предыдущие работы указывали на то, что дефектная клеточная переработка может быть частью проблемы, но точная схема от генетической поломки до нарушения переработки оставалась неизвестной. Авторы начали с сравнения активности генов в мышечных клетках, полученных из человеческих стволовых клеток, различавшихся только наличием распространенной мутации GNE. Они обнаружили широкие сдвиги в наборах генов, связанных с переработкой, что указывало на системное нарушение путей «уборки» в больных клетках.
Создание сопоставимых клеточных моделей
Чтобы детально изучить механизмы, команда создала более простую модель мышечной клетки, удалив ген Gne в стандартной линии мышиных миобластов. Эти модифицированные клетки продемонстрировали тот же дефицит сиаловой кислоты, что и человеческие модели и пациенты. При обычных условиях культивирования они выглядели относительно нормально, но когда запасы сахаров были удалены для имитации метаболического стресса, клетки с нокаутом значительно чаще погибали. Детальное количественное определение белков и визуализация показали, что при таком стрессе структуры переработки — аутофагосомы — формировались плохо, и нормальный поток материала в клеточные «мусорные» компартменты был приторможен. Это подтвердило, что сбой переработки — ключевая уязвимость, проявляющаяся при повышенной энергетической нагрузке у мышц с дефицитом GNE.
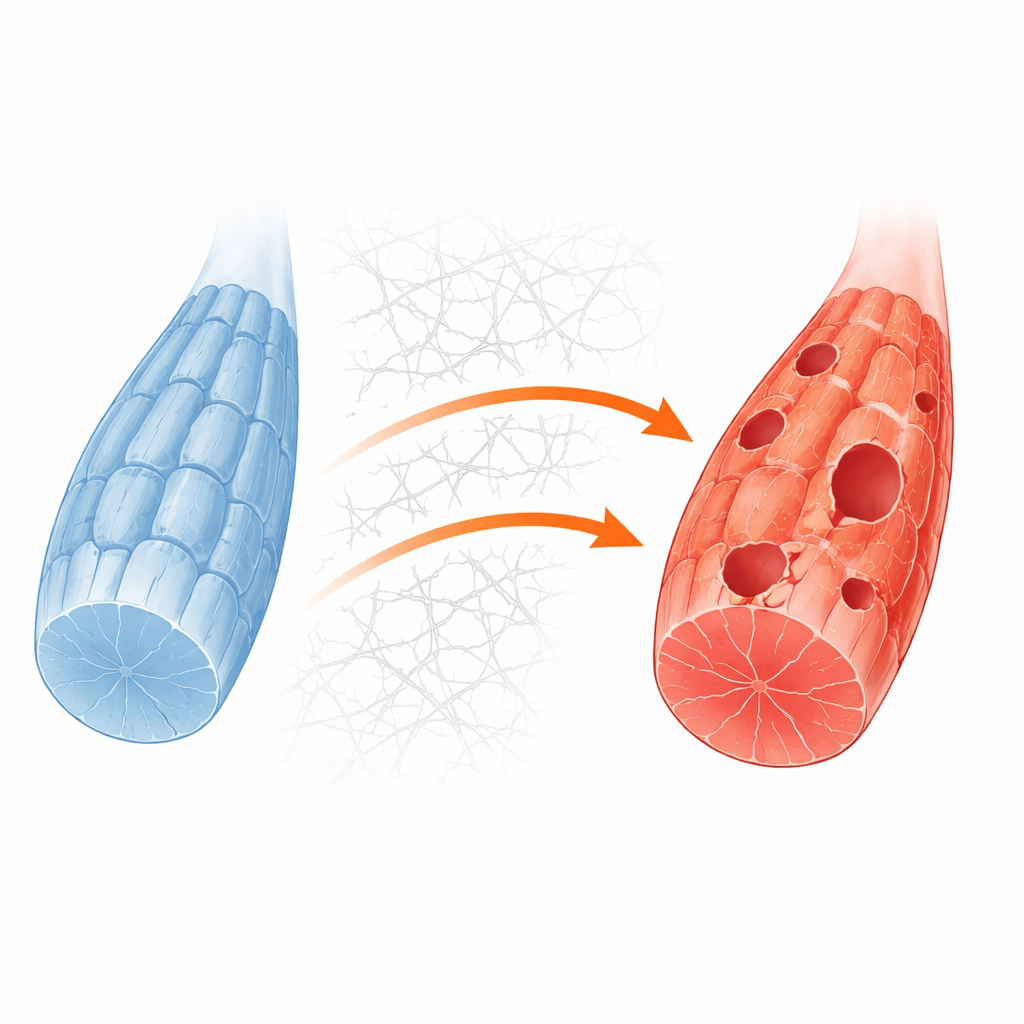
Как наружная среда клетки блокирует процессы внутри
Исследователи затем спросили, что именно молекулярно блокирует переработку. Их анализ указывал на избыточно активный путь контроля роста, управляемый белками PI3K, AKT и mTORC1, которые обычно реагируют на питательные вещества и сигналы роста. В здоровой мышце при нехватке энергии этот путь затухает, позволяя стартовому ферменту ULK1 инициировать переработку. Однако в клетках с дефицитом GNE путь оставался включенным даже во время голодания. Одновременно клетки перепроизводили коллаген и другие компоненты внеклеточного матрикса. Этот избыток «каркаса» укреплял точки контакта между клеточной поверхностью и окружающей средой, что в свою очередь активировало фактор фокальной адгезии и усиливало сигнал по пути PI3K–AKT–mTORC1. В результате на ULK1 сохранялся постоянный химический «ярлык», удерживающий его в выключенном состоянии и не позволяющий начаться процессу переработки.
Проба препарата, ослабляющего тормоз
Имея такую схему, команда просканировала большую базу данных изменений экспрессии генов под действием лекарств в поисках препаратов, чьи эффекты противоположны сигнатуре болезни. Многие из лучших кандидатов оказались ингибиторами PI3K или mTOR, и для дальнейших тестов был выбран хопанлизиб — одобренный внутривенный ингибитор PI3K, применяемый при некоторых лимфомах. В мышиных мышечных клетках с нокаутом Gne хопанлизиб снизил чрезмерный сигнальный поток, убрал ингибирующую метку с ULK1 и восстановил активность переработки, хотя сам дефицит сиаловой кислоты при этом не устранялся. Авторы затем перешли к трехмерным нейромышечным органоидам, полученным из человеческих стволовых клеток с мутацией GNE. Эти миниатюрные мышечно-нервные единицы воспроизводили низкий уровень сиаловой кислоты, дефекты переработки и гиперактивность mTORC1. При обработке хопанлизибом во время питательного стресса в больных органоидах внутри мышечных волокон образовалось значительно больше пунктов переработки, что указывает на восстановление «уборки».
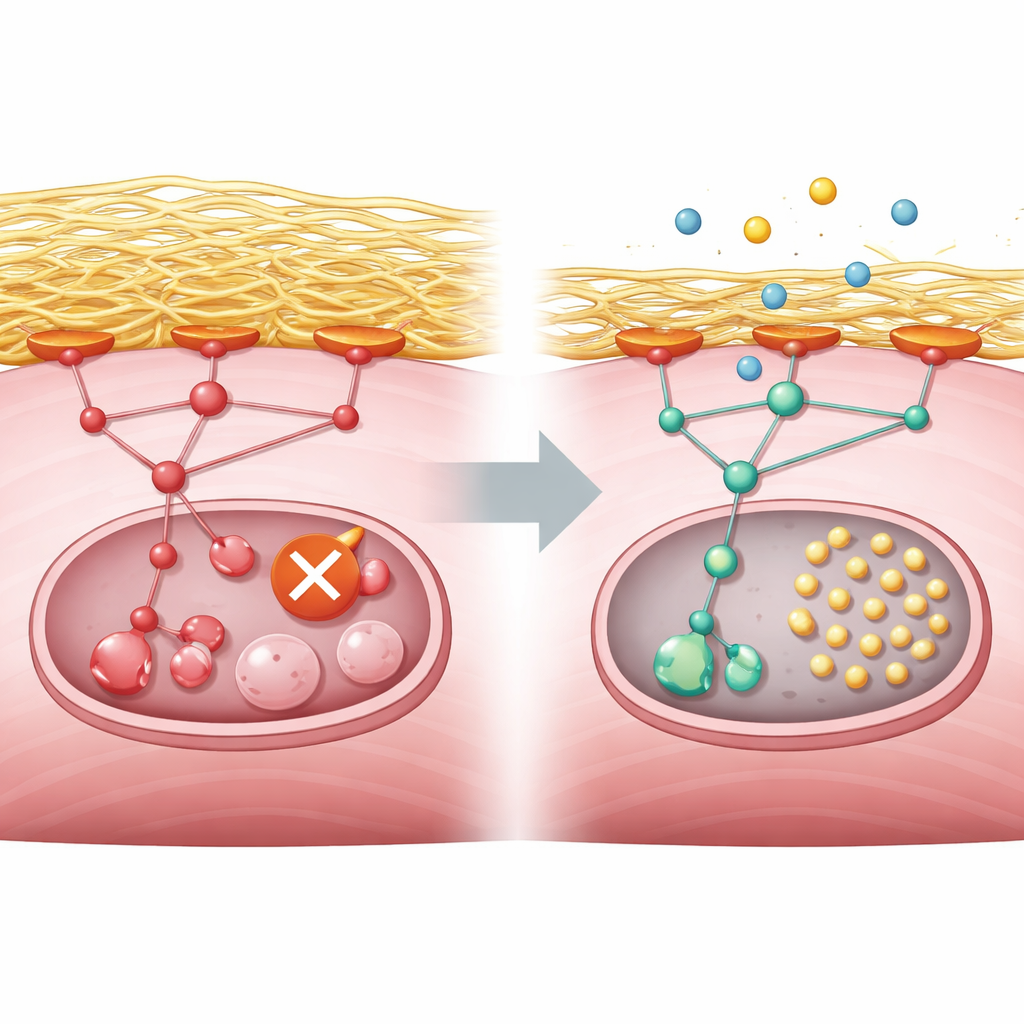
Что это означает для людей с миопатией GNE
Проще говоря, работа связывает дефектный ген синтеза сахара в мышечных клетках с чрезмерным накоплением внеклеточного матрикса, что сверхстимулирует путь контроля роста и отключает внутриклеточную «службу очистки». Исследование показывает, что этот же паттерн наблюдается в генетически модифицированных мышиных клетках, мышцах, полученных из человеческих стволовых клеток и органоидах, а также в профилях экспрессии генов из биоптатов пациентов. Хотя хопанлизиб пока не является лечением миопатии GNE, эксперименты предполагают, что аккуратно направленное подавление пути PI3K–AKT–mTORC1 может снять блок переработки и потенциально замедлить разрушение мышц. Будущие клинические исследования должны будут установить, безопасен ли и ефективен ли такой подход для людей, но работа дает ясную и проверяемую терапевтическую цель.
Цитирование: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
Ключевые слова: миопатия GNE, аутофагия в мышцах, внеклеточный матрикс, путь AKT–mTORC1, хопанлизиб