Clear Sky Science · nl
Defecte autofagie bij GNE-myopathie wordt hersteld door remming van niet‑canonische Akt–mTORC1‑activatie in meerdere isogene modellen
Waarom spier‑zelfreiniging er toe doet
Onze spieren breken voortdurend versleten onderdelen af en bouwen ze opnieuw op. Deze interne huishouding, autofagie genoemd, houdt spiervezels jarenlang sterk. Bij een zeldzame erfelijke aandoening die bekendstaat als GNE‑myopathie, verliezen jongvolwassenen geleidelijk spierkracht, maar de reeks gebeurtenissen die van één defect gen naar spierverval leiden, was onduidelijk. Deze studie volgt die keten stap voor stap, met gebruik van stamcelmodellen, gemodificeerde muisspiercellen en miniatuur neuromusculaire organoïden, en laat zien hoe een verstoorde omgeving rond de spiercel het recyclen binnenin de cel kan uitschakelen en hoe een bestaand kanker‑medicijn dat mogelijk kan herstellen.
Van genverandering naar zwakke spieren
GNE‑myopathie wordt veroorzaakt door mutaties in een gen dat normaal helpt bij de aanmaak van siaalzuur, een klein suikerrestje dat veel oppervlaktedomeinen siert. Wanneer het gen faalt, raken spiervezels ondervoorzien van siaalzuur en ontwikkelen ze uiteindelijk randvacuolen, belachtige structuren die in patiëntbiopten onder de microscoop zichtbaar zijn. Eerder werk suggereerde dat defecte cellulair recyclen een rol speelt, maar de precieze koppeling van gendefect naar mislukte autofagie was onbekend. De auteurs begonnen met het vergelijken van genexpressie in spiercellen gekweekt uit menselijke stamcellen die alleen verschilden in het dragen van een veelvoorkomende GNE‑mutatie. Ze zagen brede verschuivingen in genen die met recyclen te maken hebben, wat erop wijst dat huishoudingsroutes consequent verstoord zijn in zieke cellen.
Het bouwen van overeenkomstige celmodellen
Om de mechanismen nader te onderzoeken creëerde het team een eenvoudiger spiercelsysteem door het Gne‑gen te verwijderen in een standaard muismyoblastlijn. Deze gemodificeerde cellen toonden hetzelfde gebrek aan siaalzuur als in menselijke modellen en bij patiënten. Onder routinegroeicondities leken ze redelijk normaal, maar wanneer suikervoorraad werd teruggeschroefd om metabolische stress na te bootsen, waren de knockoutcellen veel gevoeliger voor celdood. Gedetailleerde eiwitmetingen en beeldvorming toonden dat in deze gestreste cellen de recyclingsstructuren, autophagosomen genoemd, slecht vormden en dat de normale stroom van materiaal naar de afvalcompartimenten van de cel werd afgeremd. Dit bevestigde dat falende autofagie een kernzwakte is die aan het licht komt wanneer GNE‑deficiënte spiercellen door energiebehoefte onder druk worden gezet.
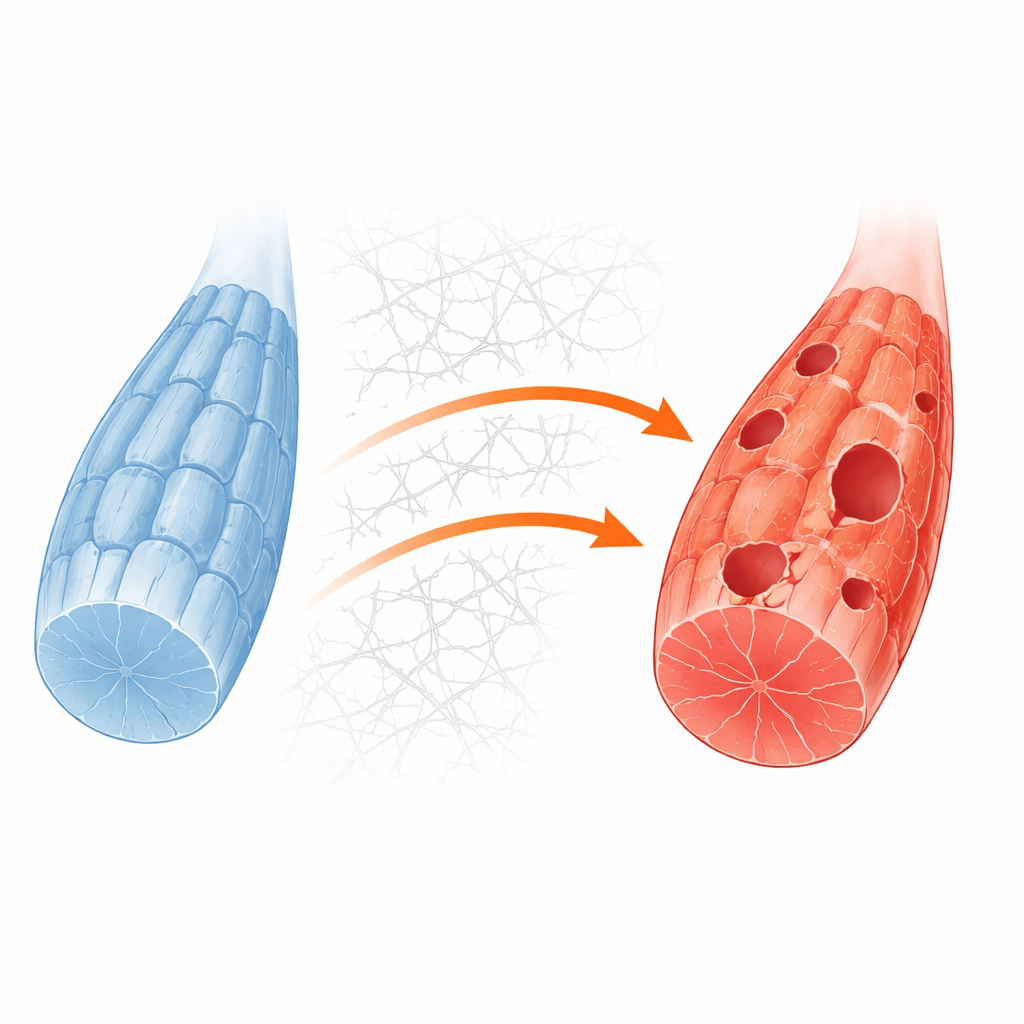
Hoe de buitenkant van de cel de binnenkant blokkeert
De onderzoekers vroegen vervolgens wat op moleculair niveau het recyclen blokkeerde. Hun analyses wezen op een overactief groeiregulerend pad gedreven door eiwitten bekend als PI3K, AKT en mTORC1, die normaal reageren op voedingsstoffen en groeisignalen. In gezonde spier dempt een energie tekort dit pad en kan een initiërend enzym, ULK1, autofagie opstarten. In GNE‑deficiënte cellen bleef het pad echter ingeschakeld, zelfs tijdens uithongering. Tegelijkertijd produceerden de cellen excessief collageen en andere componenten van het omringende skelet, de extracellulaire matrix. Deze overmaat aan matrix versterkte de contactpunten tussen celoppervlak en omgeving, wat op zijn beurt een relaismolecuul, focal adhesion kinase, activeerde en het signaal naar het PI3K–AKT–mTORC1‑pad voerde. Het gevolg was een aanhoudende chemische modificatie op ULK1 die het in een uit‑toestand houdt, waardoor autofagie niet eens kan beginnen.
Een geneesmiddel testen dat het rempedaal versoepelt
Gewapend met dit bedradingsdiagram doorzochten de onderzoekers een grote database van geneesmiddel‑geïnduceerde genveranderingen om middelen te vinden waarvan de effecten tegengesteld waren aan het ziekte‑handtekening. Veel van de topkandidaten waren remmers van PI3K of mTOR, en ze kozen copanlisib, een geregistreerde intraveneuze PI3K‑remmer die voor bepaalde lymfomen wordt gebruikt, voor nadere tests. In GNE‑knockout muisspiercellen verlaagde copanlisib het overactieve padsignaal, verwijderde de remmende modificatie van ULK1 en herstelde de recyclingactiviteit, hoewel het het oorspronkelijke gebrek aan siaalzuur niet repareerde. De auteurs gingen daarna over naar driedimensionale neuromusculaire organoïden gekweekt uit menselijke stamcellen met de GNE‑mutatie. Deze miniatuur spier‑zenuw‑eenheden reproduceerden lage siaalzuurniveaus, autofagiedefecten en mTORC1‑overactiviteit. Bij behandeling met copanlisib tijdens nutriëntstress vormden zieke organoïden veel meer autofagie‑puncta binnen spiervezels, wat wijst op heropgestarte huishouding.
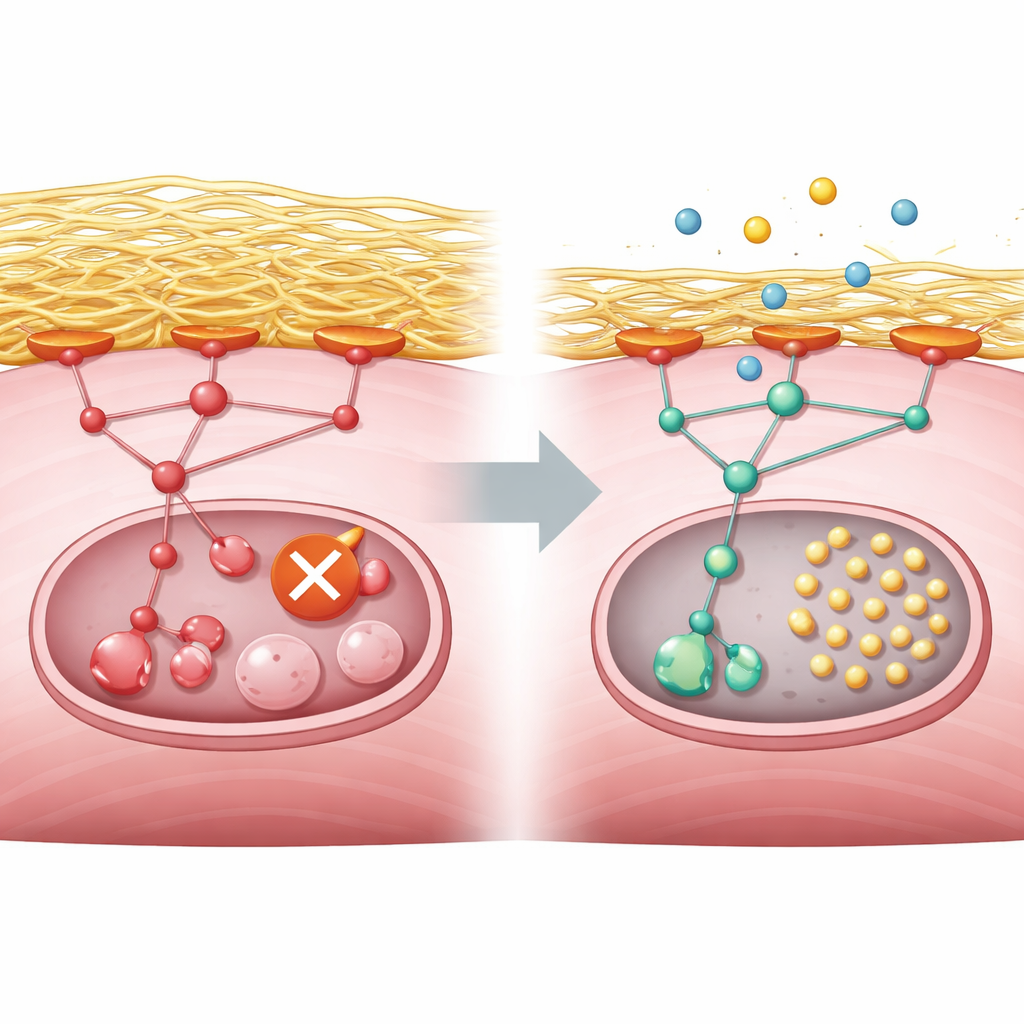
Wat dit betekent voor mensen met GNE‑myopathie
Kort gezegd koppelt dit werk een defect gen voor suikerproductie in spiercellen aan een excessieve ophoping van de omringende matrix, die een groeiregulerend pad overstimuleert en de schoonmaakploeg van de cel uitschakelt. De studie laat zien dat dit patroon verschijnt in gemodificeerde muiscellen, uit menselijke stamcellen afgeleide spiercellen en organoïden, en in genexpressiegegevens van patiëntbiopten. Hoewel copanlisib nog geen behandeling voor GNE‑myopathie is, suggereren de experimenten dat het zorgvuldig temperen van het PI3K–AKT–mTORC1‑pad de blokkade van autofagie kan opheffen en mogelijk spierbeschadiging kan vertragen. Toekomstige klinische studies moeten bepalen of deze benadering veilig en effectief is bij mensen, maar het werk levert een duidelijk, te testen therapeutisch doel op.
Bronvermelding: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
Trefwoorden: GNE‑myopathie, spierautofagie, extracellulaire matrix, AKT mTORC1‑pad, copanlisib