Clear Sky Science · ja
GNEミオパチーの異常なオートファジーは、複数の同系モデルで非正統的なAkt–mTORC1活性化を抑制することで回復する
筋肉の“自己清掃”が重要な理由
筋肉は常に摩耗した成分を分解し再構築しています。この細胞内の家事作業、すなわち細胞のリサイクルは、筋繊維を生涯にわたり強く保つ役割を果たします。GNEミオパチーと呼ばれる稀な遺伝性の病気では、若年成人がゆっくりと筋力を失いますが、単一の遺伝子変異から筋萎縮へと至る一連の過程は不明瞭でした。本研究は、幹細胞モデル、遺伝子改変マウス筋細胞、小型の神経筋オルガノイドを用いて、その連鎖を段階的にたどり、筋細胞の周囲環境の乱れがどのように細胞内のリサイクルを停止させるか、そして既存の抗がん薬がそれを再び作動させうるかを示します。
遺伝子変化から弱った筋肉へ
GNEミオパチーは、細胞がシアル酸という小さな糖を合成するのを助ける遺伝子の変化によって引き起こされます。シアル酸は多くの表面分子に付加される修飾です。この遺伝子が機能しないと、筋繊維はシアル酸が不足し、患者の生検で観察されるリム状空胞と呼ばれる泡状の構造が最終的に発生します。以前の研究は細胞のリサイクルの異常が問題の一端であることを示唆していましたが、遺伝子欠陥からリサイクル障害へ至る正確な配線は不明でした。著者らはまず、一般的なGNE変異を持つかどうかだけが異なるヒト幹細胞由来の筋細胞で遺伝子発現を比較しました。リサイクルに関連する遺伝子群に広範な変化が見られ、疾患細胞でハウスキーピング経路が一貫して乱れていることが示唆されました。
一致する細胞モデルの構築
メカニズムを詳しく調べるため、研究チームは標準的なマウス筋芽細胞株でGne遺伝子を欠失させ、より単純な筋細胞系を作成しました。これらの改変細胞はヒトモデルや患者で見られるのと同様のシアル酸欠乏を示しました。通常の増殖条件下では見かけ上は比較的正常でしたが、代謝ストレスを模倣して糖供給を断ったとき、ノックアウト細胞は著しく死にやすくなりました。詳細なタンパク質解析とイメージングにより、これらのストレス下の細胞ではオートファゴソームと呼ばれるリサイクル構造の形成が不十分であり、細胞内廃棄区画への物質の流れが鈍っていることが明らかになりました。これは、GNE欠損筋がエネルギー需要にさらされるとリサイクル障害が顕在化する主要な弱点であることを裏付けます。
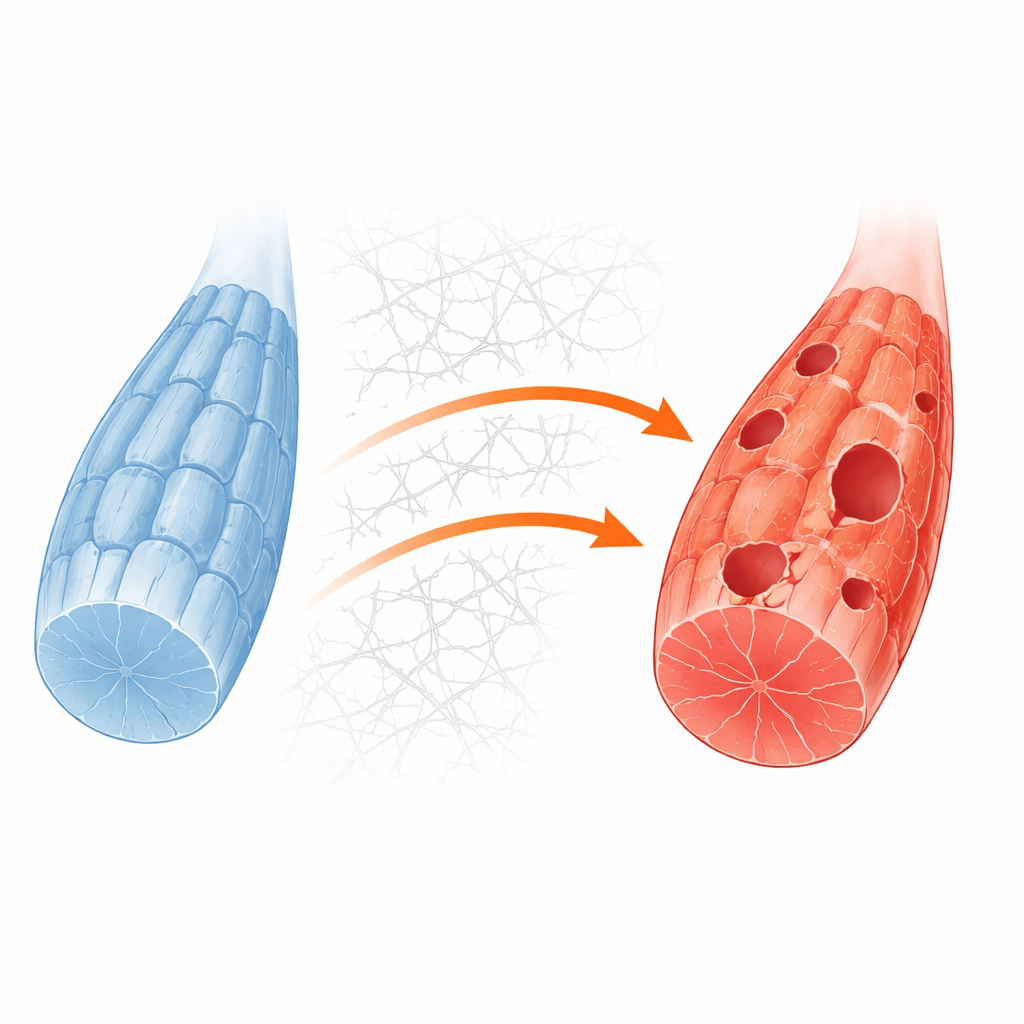
細胞外が細胞内の働きをどのように妨げるか
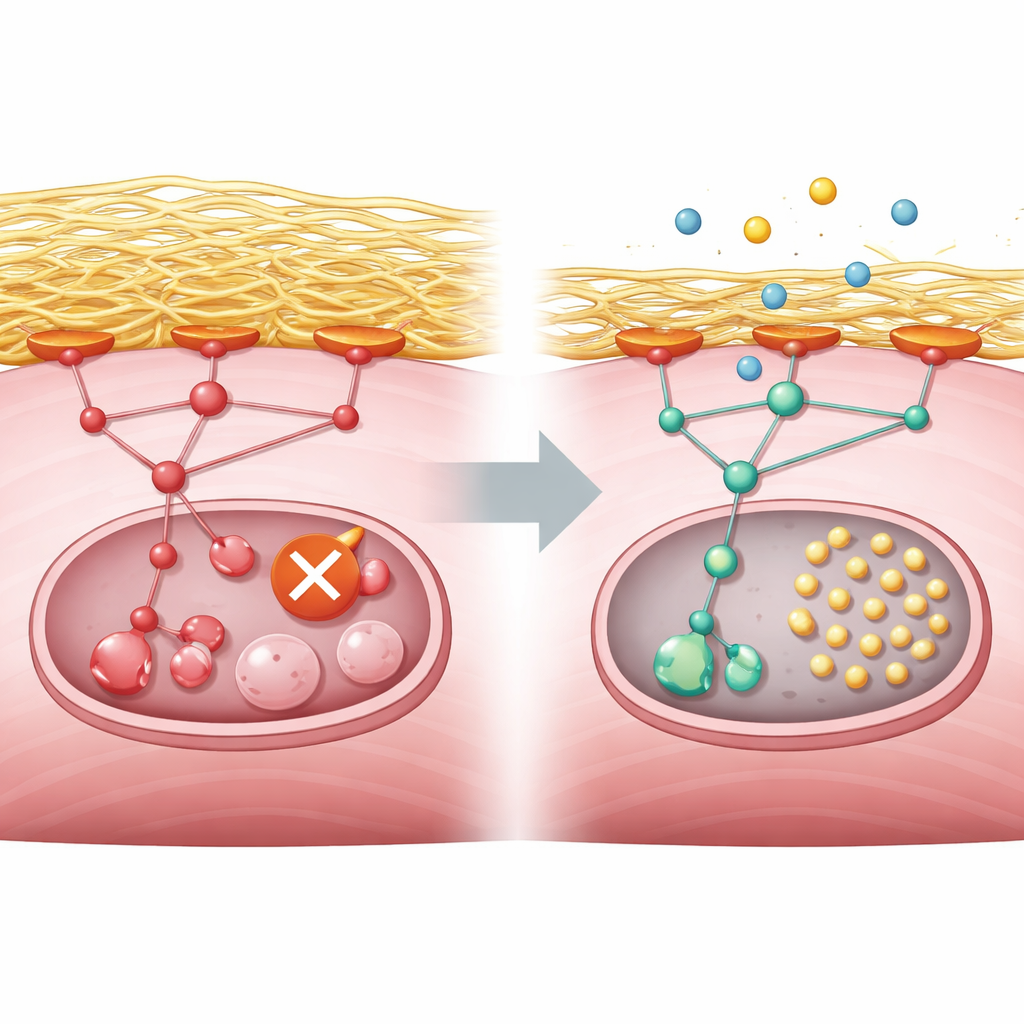
研究者らは次に、分子レベルで何がリサイクルを妨げているかを問いただしました。解析は、通常は栄養や成長シグナルに応答するPI3K、AKT、mTORC1と呼ばれるタンパク質による成長制御経路が過剰に活性化していることを示しました。健常な筋では、エネルギー不足がこの経路を抑えてULK1という起動酵素がリサイクルを開始できるようにします。しかしGNE欠損細胞では、飢餓状態でもその経路がオンのままでした。同時に、これらの細胞はコラーゲンなどの細胞外足場(細胞外マトリックス)成分を過剰に産生していました。この過剰な足場は細胞表面と周囲環境の接着点を強化し、それがフォーカルアドヒージョンキナーゼという中継分子を活性化してPI3K–AKT–mTORC1経路へとつながりました。その結果、ULK1には恒常的な抑制的化学修飾が付与され、ULK1がオフ状態に保たれることでリサイクルがそもそも開始できなくなっていました。
ブレーキを緩める薬の試験
この配線図を手に、チームは大規模な薬剤誘導遺伝子変化データベースを検索し、疾患のシグネチャと逆の効果を示す薬を探しました。上位ヒットの多くはPI3KやmTORの阻害剤であり、リンパ腫の一部に用いられる静脈内投与の承認済みPI3K阻害剤コパンリシブを追加実験の対象に選びました。GNEノックアウトのマウス筋細胞では、コパンリシブは過剰な経路シグナルを低下させ、ULK1の抑制的修飾を除去し、オリジナルのシアル酸欠乏を修復することなくリサイクル活性を回復させました。著者らは次に、GNE変異を持つヒト幹細胞から作製した三次元の神経筋オルガノイドに移りました。これらの小型ユニットは低シアル酸レベル、リサイクル障害、mTORC1の過剰活性を再現しました。栄養ストレス下でコパンリシブを処理すると、疾患性オルガノイドの筋繊維内に多くのリサイクルパンクタ(点状構造)が形成され、ハウスキーピングが回復したことを示しました。
GNEミオパチー患者への意味
簡潔に言えば、本研究は筋細胞の糖合成遺伝子の欠陥を、周囲の足場の過剰蓄積へとつなげ、その結果成長制御経路が過剰に刺激され細胞の清掃機構が停止することを示します。このパターンは、遺伝子改変マウス細胞、ヒト幹細胞由来筋、およびオルガノイド、さらに患者生検の遺伝子発現にも現れていました。コパンリシブがすぐにGNEミオパチーの治療となるわけではありませんが、PI3K–AKT–mTORC1経路を慎重に抑えることでリサイクルのブロックを解除し、筋損傷の進行を遅らせる可能性が示唆されます。今後の臨床試験でこのアプローチが人に対して安全かつ有効かを判断する必要がありますが、本研究は治療に向けた明確で検証可能な標的を提供します。
引用: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
キーワード: GNEミオパチー, 筋オートファジー, 細胞外マトリックス, AKT mTORC1経路, コパンリシブ