Clear Sky Science · he
חוסר תקינות באוטופאגיה ב-GNE מיאופתיה מטופל על ידי עיכוב הפעלת Akt–mTORC1 הלא-קנונית במגוון מודלים איזוגניים
מדוע ניקוי עצמי של השריר חשוב
השרירים שלנו מפרקים באופן מתמיד רכיבים בלויים ובונים אותם מחדש. עבודת הבית התאית הזאת, הנקראת מיחזור תאי, שומרת על חוזק סיבי השריר לאורך החיים. במחלה תורשתית נדירה הידועה כ-GNE מיאופתיה, צעירים מבוגרים מאבדים בהדרגה כוח שריר, אך הרצף שהופך פגם גנטי בודד לדלדול שרירי לא היה מובן במלואו. מחקר זה עוקב אחר אותו רצף שלבים שלב אחר שלב, בעזרת מודלים של תאי גזע, תאים שריריים עכבריים מהונדסים ואורגנואידים נוירו-שריריים מוקטנים, כדי להראות כיצד סביבה מתעתעת סביב תא השריר יכולה לכבות את המיחזור בתוך התא וכיצד תרופה קיימת בתחום האונקולוגי עשויה לסייע להדליק אותו שוב.
משינוי גנטי לשרירים חלשים
GNE מיאופתיה נגרמת על ידי שינויים בגן שעוזר בדרך כלל לתאים לייצר חומצה סיאלית, סוכר קטן שמקשט מולקולות רבות על פני השטח. כאשר הגן הכושל, סיבי השריר נותרים במצב של מחסור בחומצה סיאלית ולבסוף מפתחים ואקולות עם שפה (rimmed vacuoles), מבנים מבעבעים הנראים במיקרוסקופ בדגימות מטופלים. עבודה קודמת רמזה כי ליקוי במיחזור תאי עשוי להיות חלק מהבעיה, אך התקשורת המדויקת מהפגם הגנטי לכישלון המיחזור הייתה לא ברורה. המחברים החלו בהשוואת פעילות גנים בתאי שריר שגודלו מתאי גזע אנושיים שהשתנו רק בכך שנשאו מוטציית GNE שכיחה. הם ראו שינויים רחבים בקבוצות גנים הקשורות למיחזור, מה שמרמז כי מסלולי עבודת הבית היו מופרעים בעקביות בתאים החולים.
בניית מודלים תאיים תואמים
כדי לחקור את המנגנונים, הצוות יצר מערכת תאי שריר פשוטה יותר על ידי מחיקת הגן Gne בקו מיובלסט עכבר סטנדרטי. תאים מהונדסים אלה הוכיחו את אותו חוסר בחומצה סיאלית שנצפה במודלים אנושיים ובמטופלים. בתנאי גידול שגרתיים הם נראו די נורמליים, אך כאשר אספקת הסוכרים הוסרה כדי לדמות לחץ מטבולי, תאי הנוקאאוט היו עם סבירות גבוהה יותר למות. מדידות חלבון מפורטות והדמיה הראו שבתאים הנלחצים הללו, מבני המיחזור שנקראים אוטופגוזומים נוצרו בצורה לקויה וזרימת החומר לאברוני הפסולת התאית נחלשה. זה חיזק כי כישלון במיחזור הוא חולשה ליבתית שמתגלת כאשר שריר חסר GNE נדחף על ידי דרישת אנרגיה.
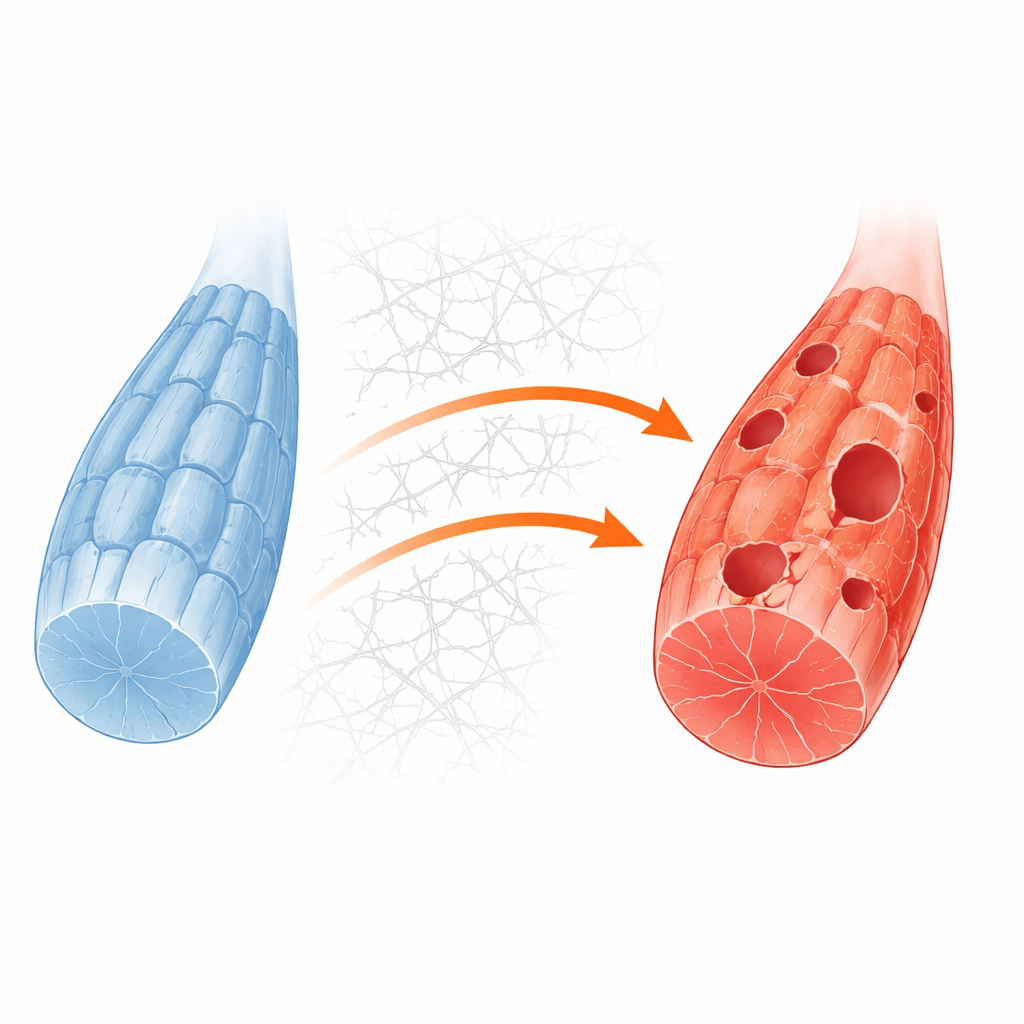
כיצד החוץ של התא חוסם את הפנים
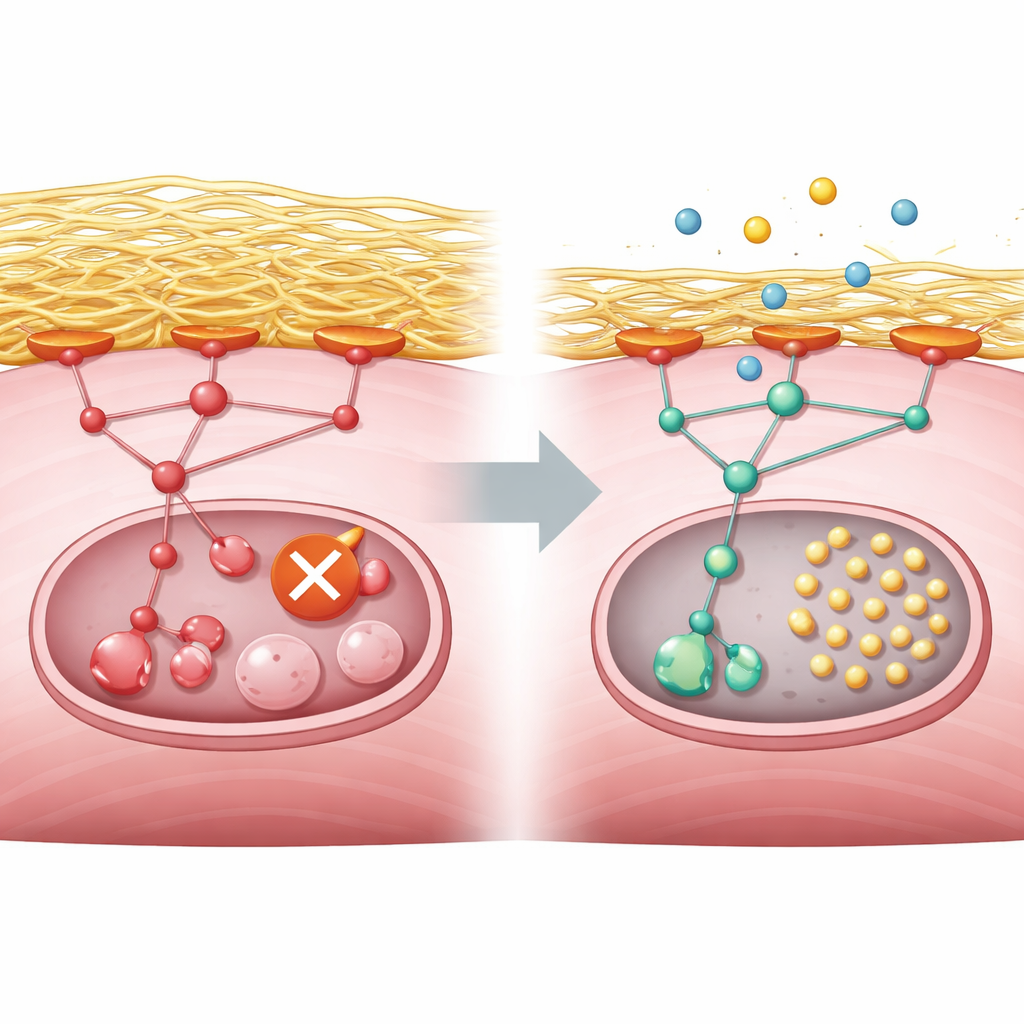
החוקרים שאלו בהמשך מה חוסם את המיחזור ברמה מולקולרית. הניתוחים שלהם הצביעו על מסלול בקרה על צמיחה פעיל יתר על המידה המונע על ידי חלבונים הידועים כ-PI3K, AKT ו-mTORC1, שבדרך כלל מגיבים להזנה ואותות גדילה. בשריר בריא, חוסר באנרגיה מרגיע את המסלול הזה ומאפשר לאנזים מעלה בשם ULK1 להפעיל את המיחזור. בתאים חסרי GNE, לעומת זאת, המסלול נשאר דלוק גם במהלך רעב. במקביל, התאים ייצרו עודף קולגן ורכיבים אחרים של המטה החיצונית, או המטריצה החוץ-תאית. המבנה החיצוני העודף הזה חיזק נקודות מגע בין פני התא לסביבה שלו, מה שהפעיל מולקולת העברה הנקראת focal adhesion kinase והזין את מסלול ה-PI3K–AKT–mTORC1. התוצאה הייתה תג כימי יציב על ULK1 ששומר אותו במצב כבוי, ומונע אפילו את תחילת המיחזור.
מבחן של תרופה המרפה את הבלם
מצוידים בתרשים החיווט הזה, הצוות חיפש בבסיס נתונים גדול של שינויים גנטיים שמעוררות תרופות כדי למצוא תרופות שהשפעתן הפוכה לחתימת המחלה. רבים מהמולטי הראשיים היו חוסמי PI3K או mTOR, והם בחרו ב-copanlisib, מעכב PI3K מאושר לווריד המשמש עבור סוגי לימפומה מסוימים, למבחנים נוספים. בתאי שריר עכבריים עם נוקאאוט של GNE, copanlisib הוריד את אות המסלול הפעיל יתר, הסיר את תג המעכב מ-ULK1 ושיחזר את פעילות המיחזור, אף על פי שלא תיקן את המחסור המקורי בחומצה הסיאלית. לאחר מכן המחברים פנו לאורגנואידים תלת־ממדיים נוירו-שריריים שגודלו מתאי גזע אנושיים הנושאים את מוטציית GNE. יחידות שריר-עצם זעירות אלה שיחזרו רמות סיאלית נמוכות, ליקויי מיחזור ופעילות יתר של mTORC1. כאשר טופלו ב-copanlisib במהלך לחץ תזונתי, האורגנואידים החולים יצרו הרבה יותר מוקדי מיחזור בתוך סיבי השריר, מה שמעיד על החייאת עבודת הבית התאית.
מה משמעות הדבר עבור אנשים עם GNE מיאופתיה
פשוטו כמשמעו, עבודה זו מחברת בין גן פגום לייצור סוכר בשריר לבין הצטברות עודפת של המטריצה החוץ-תאית, שממריצה יתר על המידה מסלול בקרה על הצמיחה וכובשת את צוות הניקיון של התא. המחקר מראה כי אותו דפוס מופיע בתאי עכבר מהונדסים, בתאי שריר שמקורם מתאי גזע אנושיים ובאורגנואידים, וכמו כן בפעילות גנים מתוך דגימות מטופלים. אף ש-copanlisib אינו עדיין טיפול ל-GNE מיאופתיה, הניסויים מציעים כי כיבוי מבוקר של מסלול ה-PI3K–AKT–mTORC1 עשוי לשחרר את החסימה במיחזור ואולי להאט את נזקי השריר. מחקרים קליניים עתידיים יצטרכו לקבוע האם גישה זו בטוחה ויעילה באדם, אך העבודה מספקת מטרה ברורה ובוחנת לטיפול.
ציטוט: Kim, DW., Kwon, EJ., Kwon, H. et al. Defective autophagy in GNE myopathy is rescued by inhibition of noncanonical Akt–mTORC1 activation across multiple isogenic models. Exp Mol Med 58, 1187–1202 (2026). https://doi.org/10.1038/s12276-026-01701-7
מילות מפתח: GNE מיאופתיה, אוטופאגיה בשריר, המטריצה החוץ-תאית, מסלול AKT–mTORC1, copanlisib