Clear Sky Science · he
ארכיטקטורת רשת עצבית גרפית בעלת שני סניפים לחיזוי עלות קשירה בין תרופה למטרה חלבונית
דרכים מהירות יותר לתרופות טובות יותר
פיתוח תרופה חדשה בדרך כלל אורך יותר מעשור ועולה מיליארדי דולרים, ורק חלק קטן מהמועמדים מגיע בסופו של דבר לחולים. מחקר זה בוחן כיצד סוג חדש של בינה מלאכותית, שנבנה כדי להבין מולקולות כרשתות של אטומים מקושרים, יכול להאיץ את חיפוש התרופות ואפילו למצוא שימושים חדשים לתרופות קיימות. על ידי חיזוי עד כמה בחוזקה תרופה תיצמד לחלבון מטרה בגוף, הגישה שואפת לצמצם אלפי אפשרויות לרשימה קצרה איכותית שניתנת לניהול.
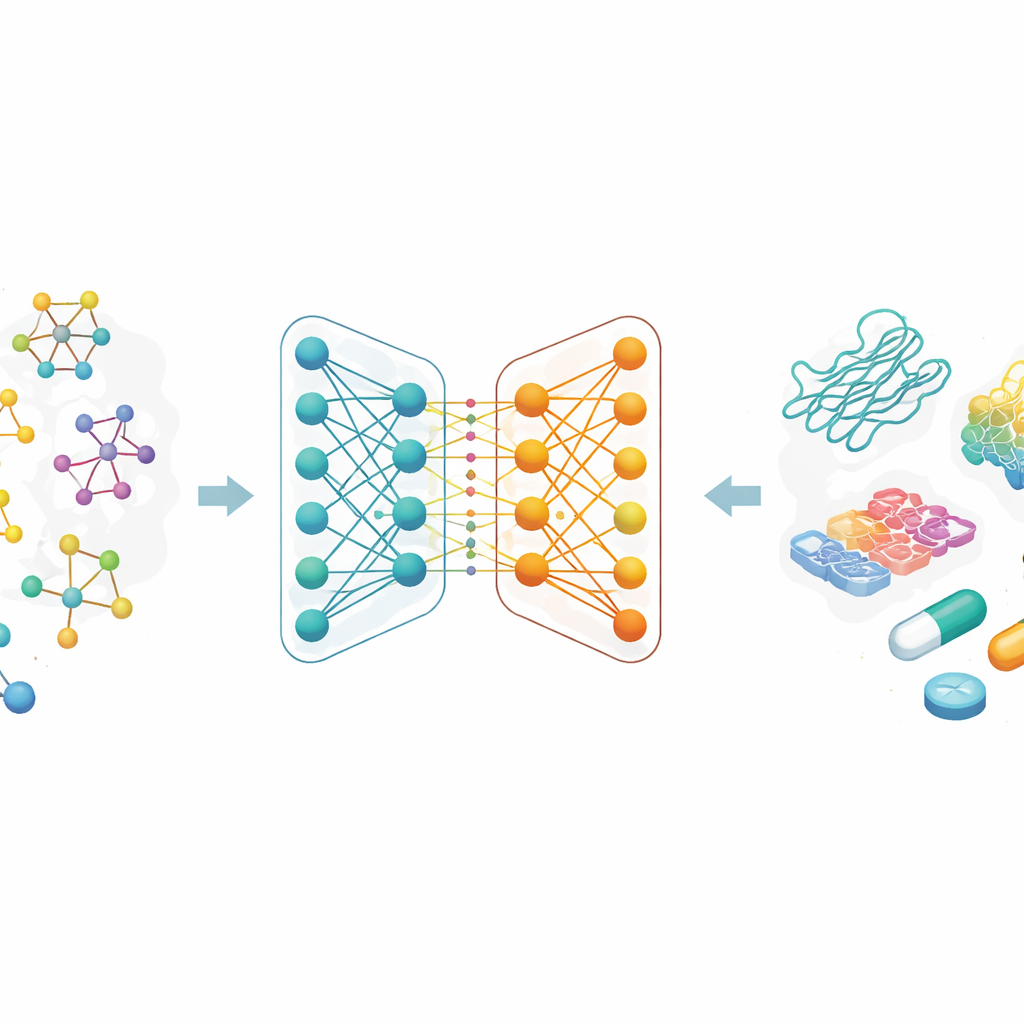
מדוע חיזוי «הדבקות» חשוב
רוב התרופות המודרניות פועלות על ידי התקשרות לחלבונים ספציפיים ושינוי ההתנהגות שלהם. עוצמת האחיזה הזו, הנקראת עלות קשירה, קשורה באופן הדוק לכך האם תרופה תעבוד ובאיזה מינון. באופן מסורתי, מדידת עלות קשירה דורשת ניסויים מעבדתיים מייגעים וספריות גדולות של תרכובות כימיות. המחברים מתמקדים בהחלפת חלק מתהליך הניסיון והטעייה הזה בחישוב: אם מודל מחשבתי יכול לחזות באופן מהימן אילו זוגות תרופה–חלבון צפויים להיקשר בחוזקה, חוקרים יכולים לבדוק פחות תרכובות במעבדה, לחסוך זמן וכסף ולפתוח דלת לרעיונות טיפוליים חדשים.
להסתכל על מולקולות כמפות מקושרות
במקום לתאר מולקולות כמחרוזות של אותיות או כרשימות ארוכות של מאפיינים מעוצבים בעבודה ידנית, החוקרים מתייחסים לכל תרופה כאל גרף: אטומים הם נקודות וקשרים כימיים הם קווים ביניהם. משפחה של שיטות בינה מלאכותית הנקראות רשתות עצביות גרפיות מצטיינת בלמידה ממפות כאלה, כי היא מעבירה מידע לאורך החיבורים בצורה חוזרת, ותופסת גם פרטים מקומיים וגם מבנה גלובלי. בעבודה זו, כל תרופה מתחילה מקוד דמוי-טקסט נפוץ בכימיה, שמומר לאחר מכן לגרף מולקולרי. הצוות גם משתמש בקידודים עשירים למטרות חלבוניות, שנועדו ללכוד דפוסים ברצפי חומצות האמינו ותת-מבנים בעלי משמעות כימית.
שני סניפי בינה מלאכותית שעובדים יחד
ליבת המאמר היא רשת עצבית גרפית חדשה בעלת שני סניפים לייצוג תרופות. סניף אחד משתמש ברשת קונבולוציה גרפית, שממזגת מידע מן האטומים השכנים באופן מבוקר. הסניף השני משתמש בשיטה הנקראת GraphSAGE, שלומדת כיצד לסכם את שכונת כל אטום מתוך הנתונים. מודול "ידע קופצני" (jumping knowledge) משלב בצורה גמישה מידע מעומקים שונים של הרשת, כך שהייצוג הסופי של התרופה משקף גם דפוסים רדודים ומקומיים וגם דפוסים עמוקים וגלובליים יותר. קידוד דו-סניפי זה מזווג עם מקודד חלבון חזק, והתכונות המשולבות של תרופה–חלבון מוזנות למודול חיזוי שמפיק הערכת עוצמת קשירה.
מה מידת הביצועים של המודל
כדי לבחון את התכנון שלהם, המחברים משווים אותו מול 45 צירופים שונים של מקודדי תרופות וחלבונים קיימים בשני אוספי ביקורת נפוצים: מערכי Davis ו-KIBA, שמקטלגים כיצד מגוון מולקולות קטנות מתקשרות עם קינאזות חלבוניות, מעמד חשוב של מטרות תרופתיות. לאורך מספר מדדים סטנדרטיים של דיוק ואיכות דירוג, המודל הדו-סניפי החדש מתייצב בקביעות בראש או קרוב אליו. במיוחד במערך Davis הוא מספק שגיאת חיזוי נמוכה יותר וסידור טוב יותר של זוגות תרופה–מטרה מאשר שיטות גרפיות מתחרות, מה שמרמז כי התצפית העשירה שלו על מבנה מולקולרי לוכדת הבדלים עדינים שמודלים פשוטים יותר מפספסים. במערך KIBA, הגדול והרעשי יותר, השיפורים קטנים יותר אך יציבים, מה שמצביע על הכללה טובה.
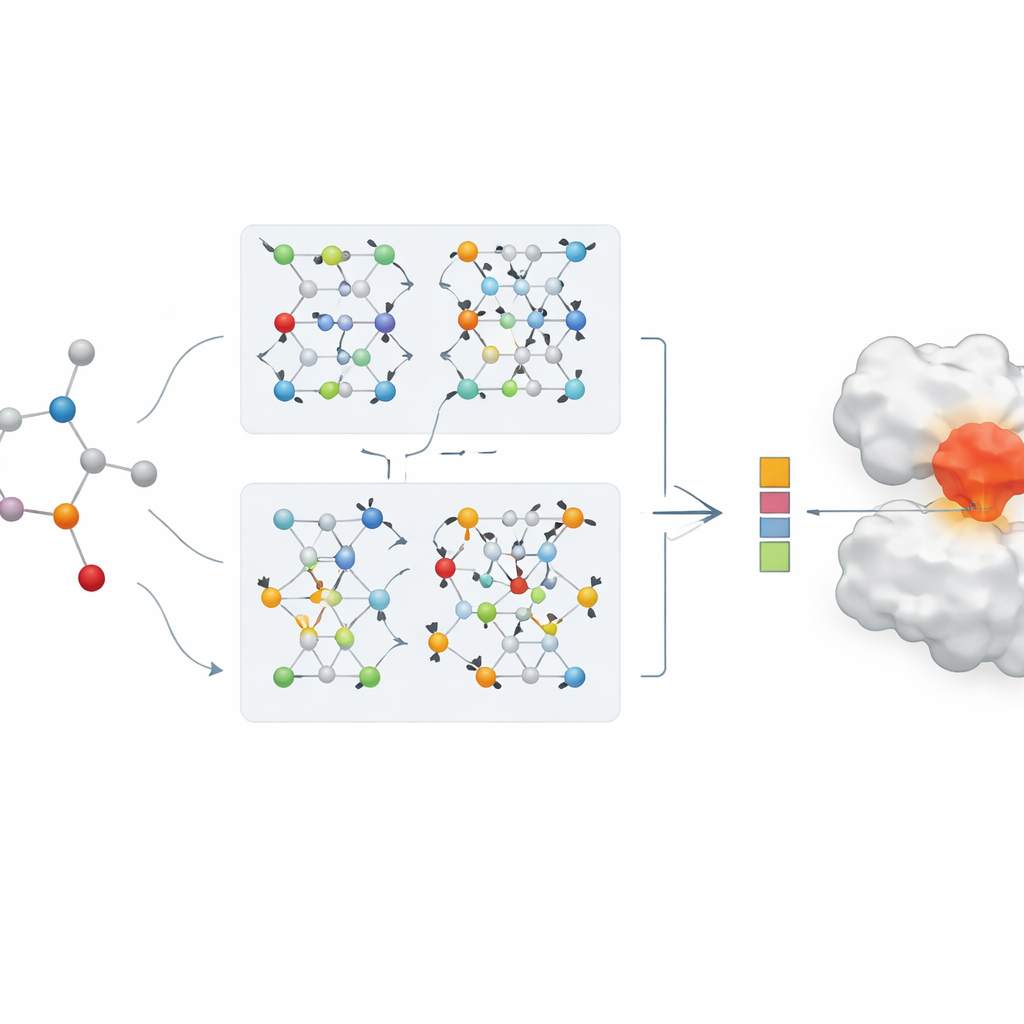
ממספרים למקרי מחלה אמיתיים
כדי להדגים ערך בעולם האמיתי, הצוות מיישם את המודל שלהם בעירוי שימוש מחדש בתרופות עבור COVID-19, עם מיקוד באנזים הוויראלי הראשי שאליו שואפות רבות מהטיפולים לנטרול. הבינה המלאכותית מדרגת תרופות אנטי-ויראליות וקבוצות קשורות על פי עוצמת הקשירה החזויה לאנזים זה. מספר מועמדים ידועים, כולל רמדסיביר וחלק ממעכבי הפרוטאז, מופיעים בראש הרשימה, בהתאמה לממצאים ניסויים שדווחו על ידי קבוצות אחרות. כאשר דירוגי המודל מושווים לניקוד דוקינג חישובי מסורתי, ישנה התאמה חזקה, והמערכת מצטיינת במיוחד בהדחקת המועמדים הסבירים אל ראש הרשימה. זה מצביע על כך שמודלים כאלה יכולים לשמש כמסננים חזקים כדי לתעדף תרכובות למבחנים ניסיוניים במהלך משברי בריאות מהירים.
מה המשמעות הזו לגילוי תרופות בעתיד
בסך הכול, המחקר מראה כי בינה מבוססת-גרף שתוכננה בקפידה יכולה לספק טביעות אצבע אינפורמטיביות יותר של מולקולות תרופות וחיזויים מהימנים יותר של האינטראקציה שלהן עם מטרות חלבוניות. עבור קהל שאינו מומחה, המסר המרכזי הוא שייצוגים דיגיטליים חכמים יותר של הכימיה יכולים להפוך סינון וירטואלי ליותר מדויק ובעל יכולת יישום, במיוחד כשזמן ומשאבים מוגבלים. למרות שהגישה עדיין מתמודדת עם אתגרים — כולל עלות חישובית ורגישות לבחירות עיצוב — היא מייצגת צעד משמעותי نحو מערכות בינה מלאכותית שעוזרות למדענים להשתמש מחדש בתרופות קיימות ולעצב תרופות חדשות באופן יעיל ובטוח יותר.
ציטוט: Abbas, K., Hao, C., Dong, S. et al. A dual-branch graph neural network architecture for drug-target binding affinity prediction. Sci Rep 16, 13864 (2026). https://doi.org/10.1038/s41598-026-43782-4
מילות מפתח: רשתות עצביות גרפיות, גילוי תרופות, חיזוי עלות קשירה, שימוש מחודש בתרופות, פרמקולוגיה חישובית