Clear Sky Science · ar
معمارية شبكة عصبية بيانية ذات فرعين للتنبؤ بشدة ارتباط الدواء بالهدف البروتيني
طرق أسرع لأدوية أفضل
عادةً ما يستغرق تطوير دواء جديد أكثر من عقد من الزمن ويكلف مليارات الدولارات، مع وصول نسبة صغيرة فقط من المرشحين إلى المرضى في النهاية. تستكشف هذه الدراسة كيف يمكن لنوع جديد من الذكاء الاصطناعي، المصمم لفهم الجزيئات كشبكات من الذرات المترابطة، أن يسرع عملية البحث عن أدوية بل ويكشف استخدامات جديدة لأدوية موجودة. من خلال التنبؤ بمدى قوة تعلق الدواء ببروتين الهدف في الجسم، تهدف هذه المقاربة إلى تضييق الآلاف من الاحتمالات إلى قائمة مختصرة وعالية الجودة يمكن إدارتها.
لماذا يهم تنبؤ مدى الالتصاق
تعمل معظم الأدوية الحديثة عن طريق الالتحام ببروتينات محددة وتغيير سلوكها. تُعد قوة ذلك الالتصاق، المسماة شدة الارتباط، مرتبطة ارتباطًا وثيقًا بما إذا كان الدواء سينجح وبالجرعة المطلوبة. تقليديًا، يتطلب قياس شدة الارتباط تجارب مخبرية مرهقة ومجموعات كبيرة من المركبات الكيميائية. يركز المؤلفون على استبدال جزء من هذا النهج التجريبي بالحوسبة: إذا تمكن نموذج حاسوبي من التنبؤ بشكل موثوق بأزواج الدواء–البروتين التي من المرجح أن ترتبط بإحكام، فيمكن للباحثين اختبار عدد أقل بكثير من المركبات في المختبر، مما يوفر الوقت والمال ويفتح الباب أمام أفكار علاجية جديدة.
رؤية الجزيئات كخرائط مترابطة
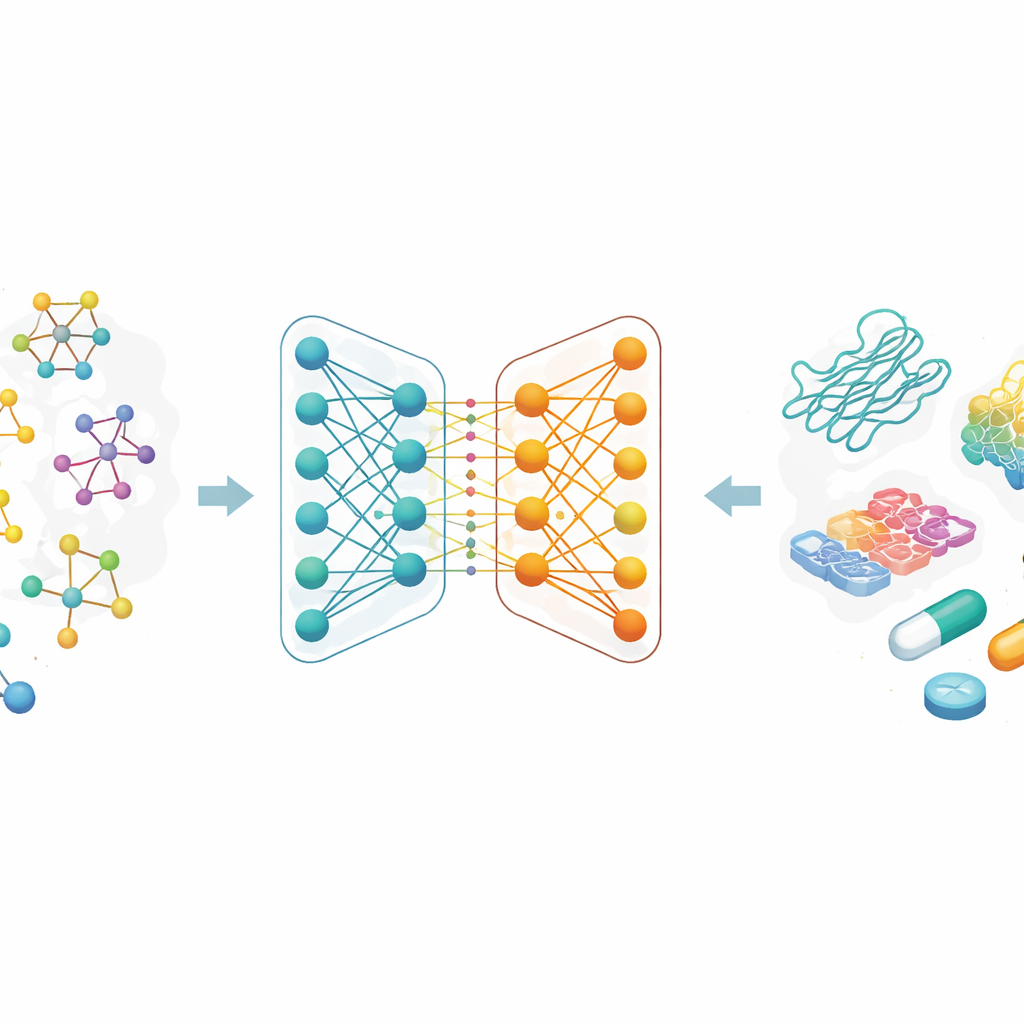
بدلًا من وصف الجزيئات كسلاسل من الحروف أو قوائم طويلة من الميزات المصممة يدويًا، يتعامل الباحثون مع كل دواء كرسمة بيانية: الذرات نقاط والروابط الكيميائية خطوط بينها. عائلة من أساليب الذكاء الاصطناعي تسمى الشبكات العصبية البيانية بارعة بشكل خاص في التعلم من هذه الخرائط، لأنها تنقل المعلومات عبر الاتصالات مرارًا وتكرارًا، ملتقطةً التفاصيل المحلية والبنية الكلية على حد سواء. في هذا العمل، يبدأ كل دواء من رمز شائع يشبه النص مستخدم في الكيمياء، ثم يُحوَّل إلى رسم بياني جزيئي. كما يستخدم الفريق ترميزات غنية لأهداف البروتين، صُممت لالتقاط أنماط تسلسل الأحماض الأمينية والمرتكزات الكيميائية ذات الدلالة.
فرعا ذكاء اصطناعي يعملان معًا
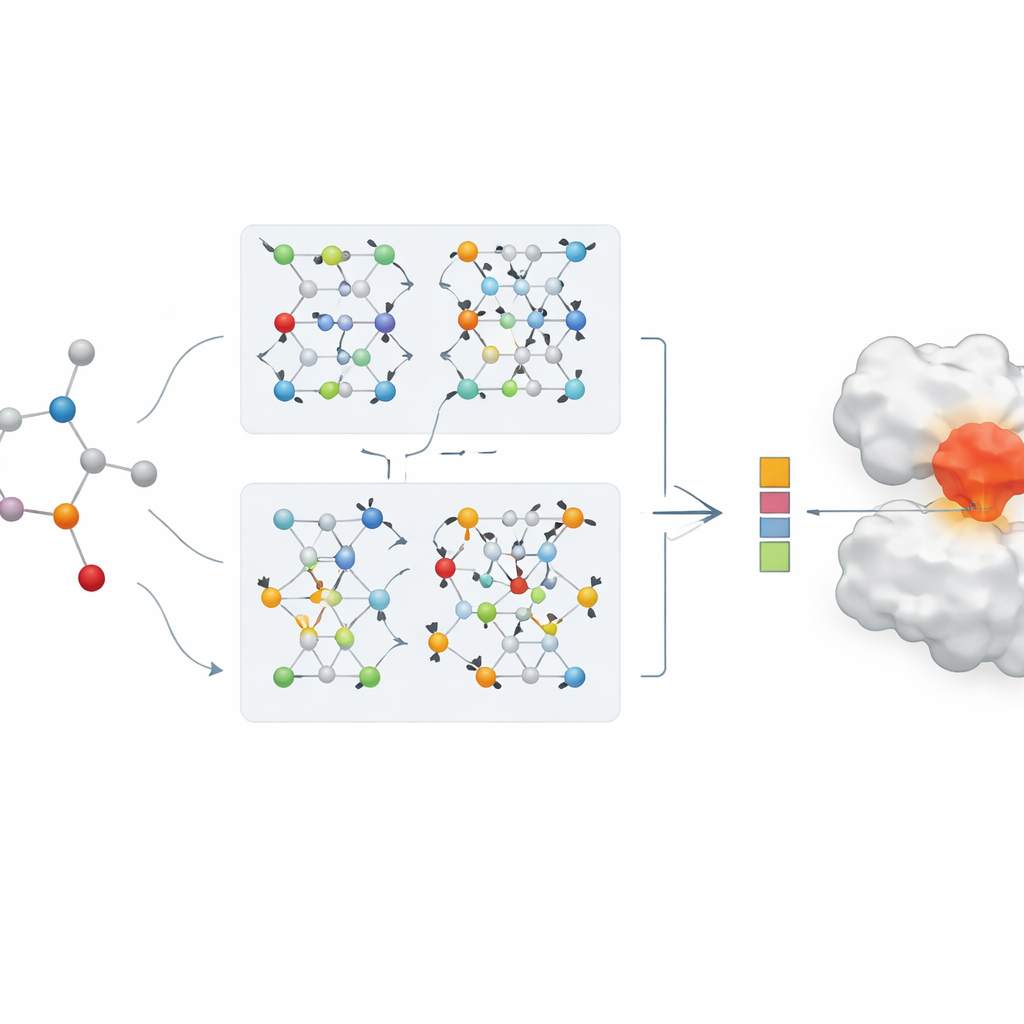
جوهر الورقة هو شبكة عصبية بيانية جديدة ذات فرعين لتمثيل الأدوية. يستخدم فرع واحد شبكة التفاف بيانية تمزج المعلومات من الذرات المجاورة بطريقة محكومة. أما الفرع الآخر فيستخدم طريقة تُدعى GraphSAGE، التي تتعلم كيفية تلخيص حيّز كل ذرة من البيانات نفسها. ثم يجمع وحدة "المعرفة القافزة" المعلومات بمرونة من أعماق مختلفة للشبكة، بحيث يعكس التمثيل النهائي للدواء الأنماط السطحية المحلية والأعمق والأكثر شمولاً على حد سواء. يقترن هذا الترميز ثنائي الفرع مع مشفّر بروتين قوي، وتُدخَل ميزات الدواء–البروتين المجمعة في وحدة للتنبؤ تُنتج تقديرًا لشدة الارتباط.
مدى أداء النموذج
لاختبار تصميمهم، يقارنه المؤلفون مع 45 توليفة مختلفة من مشفرات الدواء والبروتين القائمة على مجموعتين مرجعيتين مستخدمتين على نطاق واسع: مجموعتا بيانات Davis وKIBA، اللتان توثّقان كيفية تفاعل مجموعة من الجزيئات الصغيرة مع كينازات البروتين، وهي فئة مهمة من أهداف الأدوية. عبر عدة مقاييس معيارية للدقة وجودة الترتيب، يجلس النموذج ثنائي الفرع الجديد باستمرار في القمة أو بالقرب منها. على مجموعة بيانات Davis بشكل خاص، يحقق خطأ تنبؤ أقل وترتيبًا أفضل لأزواج الدواء–الهدف مقارنة بالطرق البيانية المنافسة، مما يشير إلى أن رؤيته الأغنى للبنية الجزيئية تلتقط فروقًا دقيقة تفوتها النماذج الأبسط. على مجموعة KIBA الأكبر والأكثر ضوضاءً، تكون التحسينات أصغر لكنها لا تزال قوية، مما يدل على عمومية جيدة.
من الأرقام إلى حالات مرضية حقيقية
لإظهار القيمة العملية، يطبّق الفريق نموذجهم على دراسة حالة لإعادة توظيف الأدوية لمرض كوفيد-19، مع التركيز على الإنزيم الفيروسي الرئيسي الذي تهدف إليه العديد من العلاجات لتعطيله. يصنف الذكاء الاصطناعي الأدوية المضادة للفيروسات والأدوية ذات الصلة حسب شدة الارتباط المتوقعة بهذا الإنزيم. يظهر عدد من المرشحين المعروفين، بما في ذلك ريمديسيفير ومثبطات البروتياز الأخرى، قريبين من قمة القائمة، متوافقين مع نتائج تجريبية أبلغت عنها مجموعات أخرى. عند مقارنة تصنيفات النموذج مع درجات الاعتصاف التقليدية بالحوسبة، هناك توافق قوي، ويظهر الذكاء الاصطناعي قوة خاصة في دفع الضربات المحتملة إلى الأعلى. يشير هذا إلى أن مثل هذه النماذج قد تعمل كمرشحات فعالة لإعطاء الأولوية للمركبات للاختبار التجريبي خلال أزمات صحية سريعة التطور.
ما الذي يعنيه هذا لمستقبل اكتشاف الأدوية
بصفة عامة، تُظهر الدراسة أن التصميم الدقيق القائم على الرسوم البيانية يمكن أن يوفر بصمات أكثر إفادة لجزيئات الدواء وتنبؤات أكثر موثوقية لكيفية تفاعلها مع أهداف البروتين. بالنسبة لغير المتخصصين، الرسالة الأساسية هي أن التمثيلات الرقمية الأذكى للكيمياء يمكن أن تجعل الفحص الافتراضي أكثر دقة وقابلية للتطبيق، خاصة عند محدودية الوقت والموارد. وبينما لا تزال الطريقة تواجه تحديات — بما في ذلك التكلفة الحاسوبية والحساسية لخيارات التصميم — فإنها تمثل خطوة مهمة نحو أنظمة ذكاء اصطناعي تساعد العلماء على إعادة توظيف الأدوية الموجودة وتصميم أدوية جديدة بكفاءة وسلامة أكبر.
الاستشهاد: Abbas, K., Hao, C., Dong, S. et al. A dual-branch graph neural network architecture for drug-target binding affinity prediction. Sci Rep 16, 13864 (2026). https://doi.org/10.1038/s41598-026-43782-4
الكلمات المفتاحية: الشبكات العصبية البيانية, اكتشاف الأدوية, تنبؤ شدة الارتباط, إعادة توظيف الأدوية, الصيدلة الحاسوبية