Clear Sky Science · zh
使用整合组学方法揭示化疗诱发的外周神经病变(CIPN)机制
为什么癌症治疗会伤害神经
化疗能挽救生命,但对许多人而言也伴随着令人难受的代价:手脚灼痛、刺痛或麻木,可能持续数月甚至数年。这种被称为化疗诱发的外周神经病变的状况,会让行走、睡眠甚至扣衣扣变得困难,有时迫使医生降低剂量或停止本来有效的抗癌药物。被综述的文章说明,能够同时扫描数千种分子的前沿“组学”工具正在开始揭示治疗期间神经发生了哪些异常——以及这些知识如何为更早的预警信号和更温和、个体化的癌症治疗铺路。
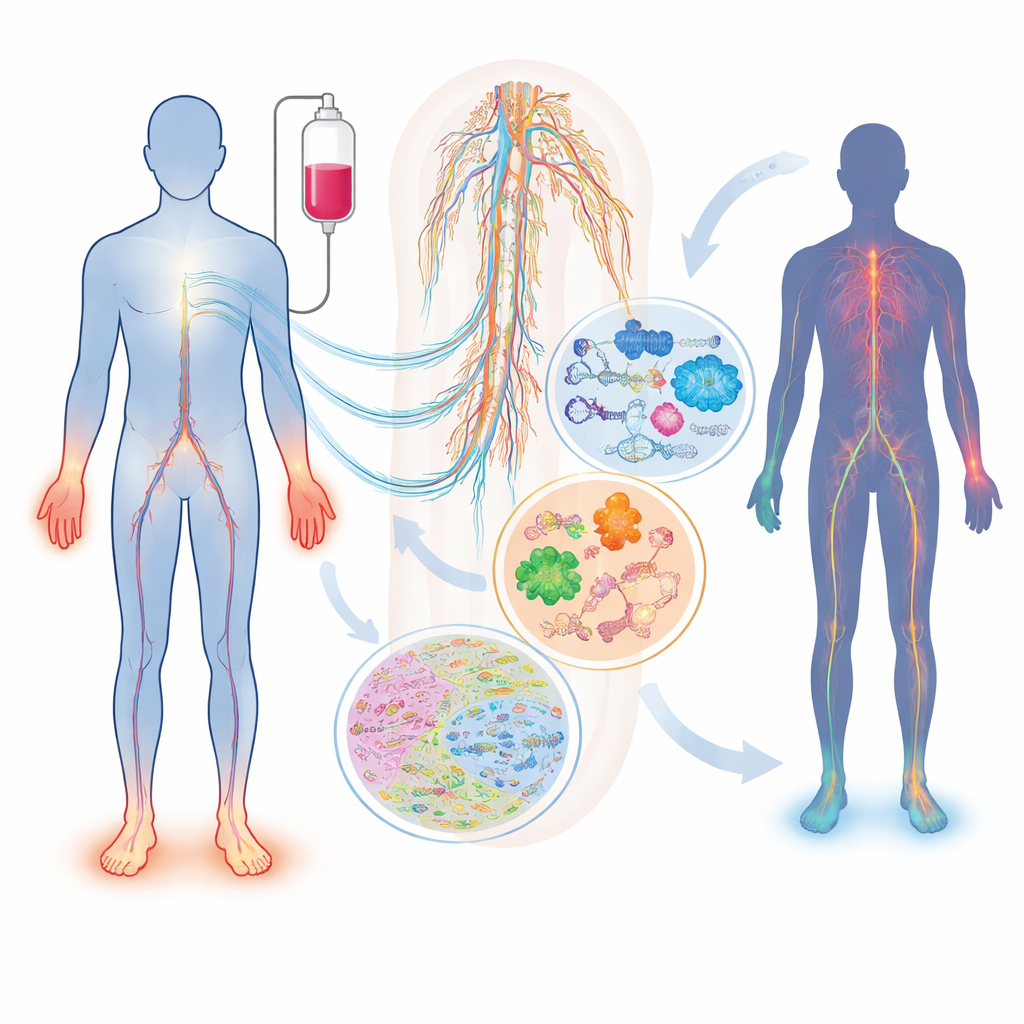
化疗期间神经发生了什么
并非所有接受相同药物和剂量的患者都会出现神经损伤,出现损伤的患者症状也可能迥异。综述描述了常用药物——如紫杉类(紫杉醇、多西紫杉醇)、铂类化合物(顺铂、奥沙利铂)和蛋白酶体抑制剂(硼替佐米、卡非佐米)——如何以不同方式损伤感觉、运动和自主神经。年龄、糖尿病、维生素缺乏、肾或甲状腺问题,以及控制药物代谢或神经结构的遗传差异等因素,都会改变个体风险。一个简单的血液标志物——神经丝轻链,已经可以追踪动物和患者的轴突损伤,但单靠它无法捕捉该病症的全部复杂性,也无法解释为何病情会发生。
组学如何提供受损神经的分子“X光”
作者展示了转录组学(RNA 分型)、蛋白质组学(大规模蛋白分析)和代谢组学(小分子系统研究)如何分别从不同角度揭示神经损伤。现代单细胞 RNA 测序可以区分脊神经节(靠近脊柱的神经细胞体簇)中许多亚型的感觉神经元及其支持细胞,并跟踪每种类型对不同化疗药物的反应。例如,特定的触觉敏感纤维在接受紫杉醇后显示出强烈的基因改变,而与神经老化和细胞衰老相关的一些基因在顺铂处理后被激活。蛋白质组学揭示了维持细胞骨架、能量工厂和应激反应的蛋白质在早期发生变化,往往早于动物出现疼痛行为数天。代谢组学则突出显示脂质、氨基酸和胆汁酸的重大紊乱,指向能量利用、膜稳定性和炎症方面的问题,这些变化可因药物、年龄甚至肠道微生物而异。
观察组织内损伤发生的具体部位
除了登记哪些分子发生变化,更先进的“空间”质谱方法可以显示这些变化在组织中的精确位置。成像质谱细胞术和质谱成像可以在神经切片和脊髓切片上直接绘制蛋白质、脂质、代谢物甚至化疗药物本身的分布,保留神经元、神经胶质细胞与周围组织的结构。早期研究利用这些工具定位与疼痛相关的神经肽,并描绘神经损伤后脂质在特定区域的变化。它们还追踪到奥沙利铂在皮肤中的长期铂沉积,这提示滞留在非肿瘤组织的药物分子可能维持慢性症状。尽管目前专门在化疗处理的神经中进行的此类研究还很少,但该技术有望澄清哪些细胞类型与微区域最先、最严重、或持续时间最长地受损。
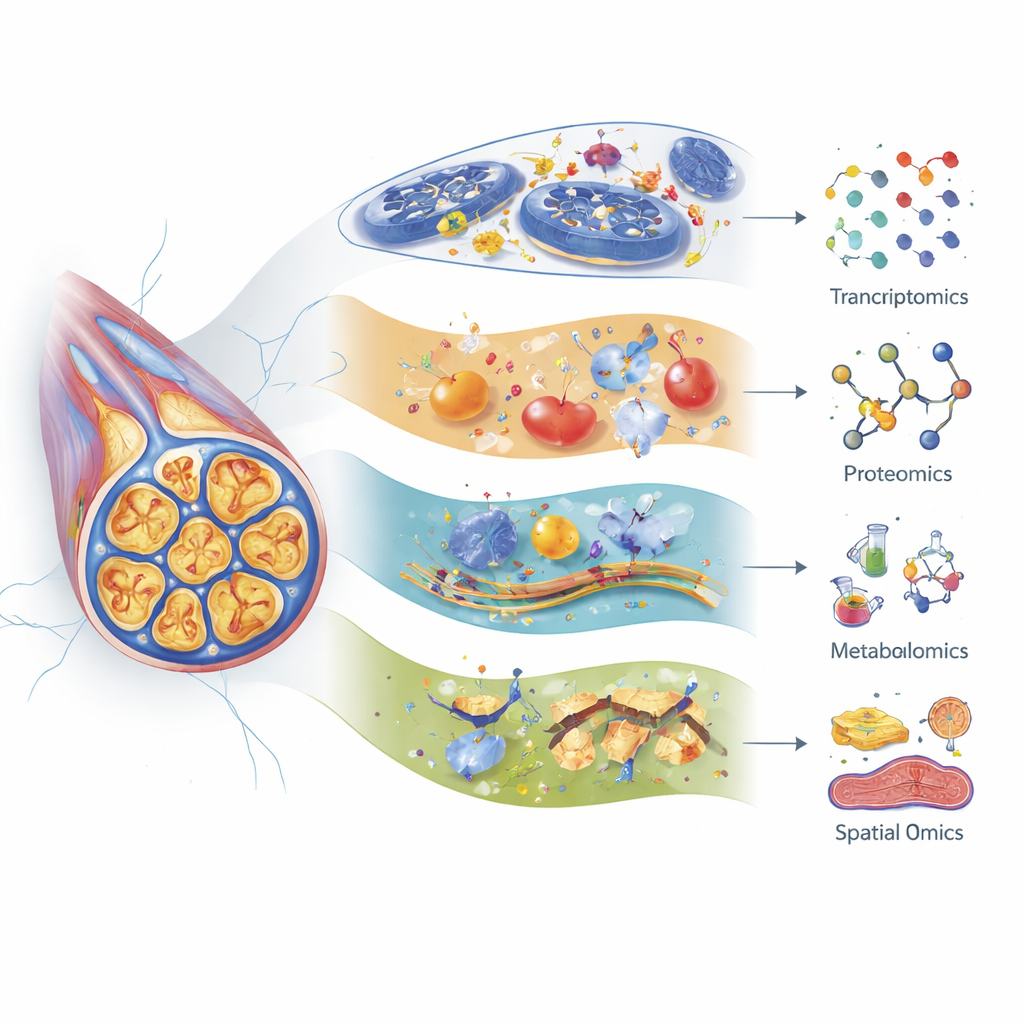
把所有分子线索拼接在一起
没有任何单一类型的组学能完全解释为什么部分患者会发展成严重的神经病变而其他人不会。综述主张采用整合的、多层次的方法,结合遗传变异、RNA 变化、蛋白网络、代谢物变化、空间图谱、神经功能检测和患者报告的症状。早期的多组学研究已将脂质信号、炎症通路、线粒体应激和调节神经的系统(如内源性大麻素和阿片信号)中的协调变化联系起来。其他研究将特定脂质介质和肠道来源的胆汁酸与疼痛相关联,提示了新的药物靶点,例如鞘脂受体或趋化因子受体,可能在不削弱抗癌疗效的情况下减轻神经损伤。将实验室数据与临床模式对齐的大型、精心设计的人体研究,对把这些见解转化为实用工具至关重要。
这对未来癌症护理的意义
对普通读者而言,核心信息是充满希望的:通过读取血液、神经组织甚至粪便中留下的分子指纹,科学家们开始能够预测谁更易发生神经损伤、理解不同药物如何损害神经系统,并识别可被保护的脆弱环节。作者总结道,整合组学,尤其是在随时间对人类样本进行分析时,最终可能指导医生选择符合个体生物学特征的癌症药物和剂量,同时指向能够保护神经的新药物。随着时间推移,这种系统层面的视角或可在保持强效化疗益处的同时,大幅减少随之而来的长期疼痛和残疾。
引用: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
关键词: 化疗诱发的外周神经病变, 多组学, 神经损伤, 癌症治疗副作用, 生物标志物