Clear Sky Science · nl
Het gebruik van een geïntegreerde omics-aanpak om de mechanismen achter chemotherapie-geïnduceerde perifere neuropathie (CIPN) te achterhalen
Waarom kankerbehandeling de zenuwen kan schaden
Chemotherapie redt levens, maar voor veel mensen gaat dat gepaard met een indringende prijs: brandende pijn, tintelingen of gevoelloosheid in handen en voeten die maanden of jaren kan aanhouden. Deze aandoening, chemotherapie-geïnduceerde perifere neuropathie genoemd, kan lopen, slapen en zelfs het dichtknopen van een overhemd bemoeilijken, en dwingt artsen soms om anderszins effectieve kanker geneesmiddelen te verlagen of te stoppen. Het besproken overzichtsartikel legt uit hoe geavanceerde “omics”-gereedschappen die duizenden moleculen tegelijk scannen beginnen te onthullen wat er misgaat in zenuwen tijdens de behandeling — en hoe deze kennis kan leiden tot eerdere waarschuwingssignalen en zachtere, meer gepersonaliseerde kankerzorg.
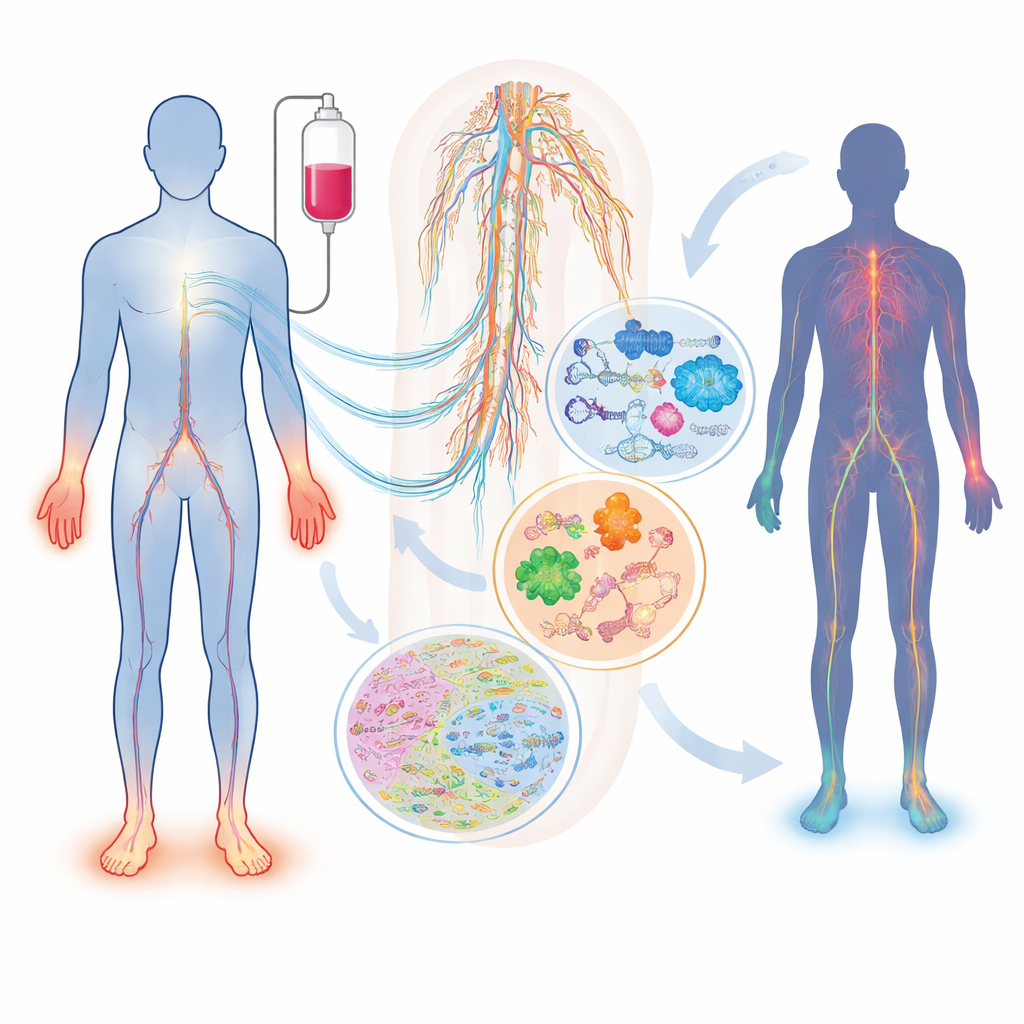
Wat er met zenuwen gebeurt tijdens chemotherapie
Niet alle patiënten die aan hetzelfde middel en dezelfde dosis worden blootgesteld ontwikkelen zenuwbeschadiging, en degenen die dat wel doen kunnen zeer verschillende symptomen ervaren. Het overzicht beschrijft hoe veelgebruikte middelen — zoals taxanen (paclitaxel, docetaxel), platinumverbindingen (cisplatine, oxaliplatine) en proteasoomremmers (bortezomib, carfilzomib) — zintuiglijke, motorische en autonome zenuwen op verschillende manieren kunnen beschadigen. Factoren zoals leeftijd, diabetes, vitaminetekorten, nier- of schildklierproblemen en erfelijke verschillen in genen die het geneesmiddeltransport of de zenuwstructuur regelen, beïnvloeden iemands risico. Eén eenvoudige bloedmarker, neurofilament light chain, kan al axonale schade volgen bij zowel proefdieren als patiënten, maar op zichzelf kan deze marker niet de volledige complexiteit van de aandoening vatten of verklaren waarom deze zich in de eerste plaats ontwikkelt.
Hoe omics een moleculaire röntgenfoto van beschadigde zenuwen geven
De auteurs laten zien hoe transcriptomics (RNA-profielen), proteomics (grootschalige eiwitanalyse) en metabolomics (systematische studie van kleine moleculen) elk een ander perspectief bieden op zenuwbeschadiging. Moderne single-cell RNA-sequencing kan veel subtypes van sensorische neuronen en ondersteunende cellen in de dorsale ganglia — clusters van cellichamen dicht bij de wervelkolom — onderscheiden en volgen hoe elk type reageert op verschillende chemotherapeutica. Zo vertonen specifieke aanraking-gevoelige vezels sterke genveranderingen na paclitaxel, en worden sommige genen die verband houden met zenuwearing en senescentie geactiveerd na cisplatine. Proteomics heeft vroege verschuivingen in eiwitten blootgelegd die het cytoskelet, de energiecentrales en stressreacties onderhouden, vaak dagen voordat dieren pijngedrag vertonen. Metabolomics benadrukt ingrijpende verstoringen in lipiden, aminozuren en galzuren, wat wijst op problemen met energiegebruik, membraanstabiliteit en ontsteking die kunnen variëren per middel, leeftijd en zelfs darmmicrobioom.
Zien waar schade zich in weefsels voordoet
Verder dan het inventariseren welke moleculen veranderen, kunnen nieuwere “ruimtelijke” massaspectrometriemethoden precies laten zien waar in het weefsel die veranderingen plaatsvinden. Imaging mass cytometry en mass spectrometry imaging brengen eiwitten, lipiden, metabolieten en zelfs de chemotherapiemiddelen zelf in kaart direct op zenuwdoorsneden en ruggenmergplakjes, waarbij de architectuur van neuronen, gliacellen en omliggend weefsel behouden blijft. Vroege studies hebben deze instrumenten gebruikt om pijn-gerelateerde neuropeptiden te lokaliseren en te schetsen hoe lipiden in precieze regio’s verschuiven na zenuwbeschadiging. Ze hebben ook langdurige afzettingen van platinum van oxaliplatine in de huid gevolgd, wat suggereert dat geneesmiddeldeeltjes die achterblijven in niet-kankergeweefsels chronische symptomen kunnen in stand houden. Hoewel slechts enkele van dergelijke studies specifiek in chemotherapie-behandelde zenuwen zijn uitgevoerd, staat de technologie klaar om te verhelderen welke celtypen en microregio’s het eerst, het sterkst en het langst worden getroffen.
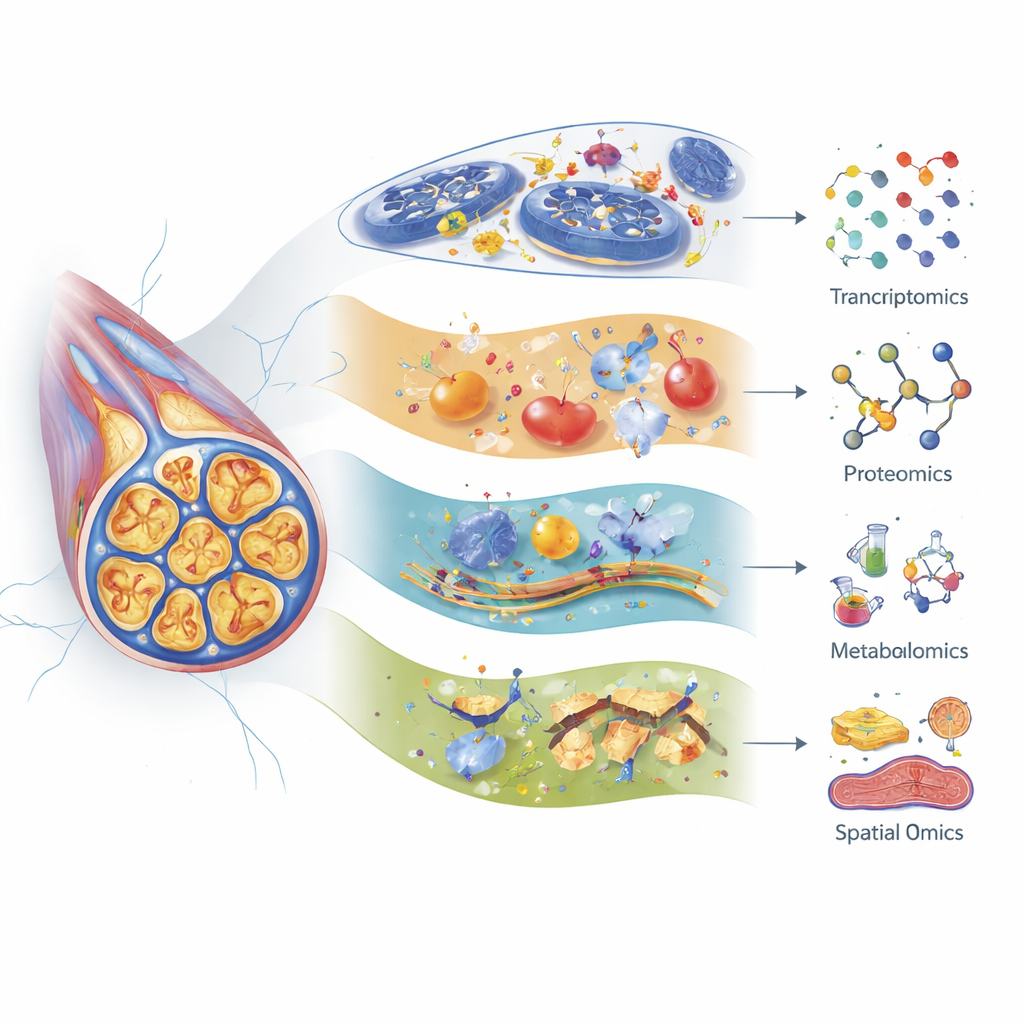
Alle moleculaire stukjes samenbrengen
Geen enkel type omics kan volledig verklaren waarom sommige patiënten ernstige neuropathie ontwikkelen en anderen niet. Het overzicht pleit voor geïntegreerde, multi-laags benaderingen die genetische variatie, RNA-veranderingen, eiwitnetwerken, metabolietverschuivingen, ruimtelijke kaarten, zenuwfunctietests en door patiënten gerapporteerde symptomen combineren. Vroege multi-omics-studies koppelen al gecoördineerde veranderingen in lipidesignalering, ontstekingsroutes, mitochondriale stress en zenuw-modulerende systemen zoals endocannabinoïden en opioïde signalering. Andere studies verbinden specifieke lipidemediateurs en darm-afgeleide galzuren aan pijn, wat nieuwe medicijndoelen suggereert zoals sphingolipide-receptoren of chemokinereseptoren die zenuwbeschadiging kunnen dempen zonder de anti-kankereffecten te verzwakken. Grote, zorgvuldig ontworpen humane onderzoeken die laboratoriumgegevens afstemmen op klinische patronen zullen cruciaal zijn om deze inzichten om te zetten in praktische instrumenten.
Wat dit betekent voor toekomstige kankerzorg
Voor de niet-specialistische lezer is de kernboodschap hoopgevend: door de moleculaire vingerafdrukken in bloed, zenuwweefsel en zelfs ontlasting te lezen, beginnen wetenschappers te voorspellen wie het meest risico loopt op zenuwbeschadiging, te begrijpen hoe verschillende middelen het zenuwstelsel schaden en kwetsbare schakels in die routes te identificeren die beschermd kunnen worden. De auteurs concluderen dat geïntegreerde omics, vooral wanneer toegepast op humane monsters over de tijd, uiteindelijk artsen zou kunnen helpen bij het kiezen van kankergeneesmiddelen en doses die passen bij iemands biologische profiel, en tegelijkertijd wijzen op nieuwe medicijnen die zenuwen tegen schade beschermen. Naarmate dit systeemniveau‑perspectief vordert, kan het mogelijk worden om de voordelen van krachtige chemotherapieën te behouden terwijl de langdurige pijn en invaliditeit die vaak volgen sterk verminderen.
Bronvermelding: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Trefwoorden: chemotherapie-geïnduceerde perifere neuropathie, multi-omics, zenuwbeschadiging, bijwerkingen van kankerbehandeling, biomarkers