Clear Sky Science · it
Utilizzare un approccio omico integrato per scoprire i meccanismi alla base della neuropatia periferica indotta dalla chemioterapia (CIPN)
Perché i trattamenti contro il cancro possono danneggiare i nervi
La chemioterapia salva vite, ma per molte persone comporta un costo scomodo: bruciore, formicolio o intorpidimento a mani e piedi che possono durare mesi o anni. Questa condizione, chiamata neuropatia periferica indotta dalla chemioterapia, può rendere difficili camminare, dormire o anche abbottonare una camicia, e talvolta costringe i medici a ridurre o interrompere farmaci antitumorali altrimenti efficaci. L’articolo recensito spiega come strumenti omici all’avanguardia che analizzano migliaia di molecole contemporaneamente stiano cominciando a rivelare cosa non va nei nervi durante il trattamento — e come queste conoscenze potrebbero portare a segnali di allarme precoci e a cure oncologiche più delicate e personalizzate.
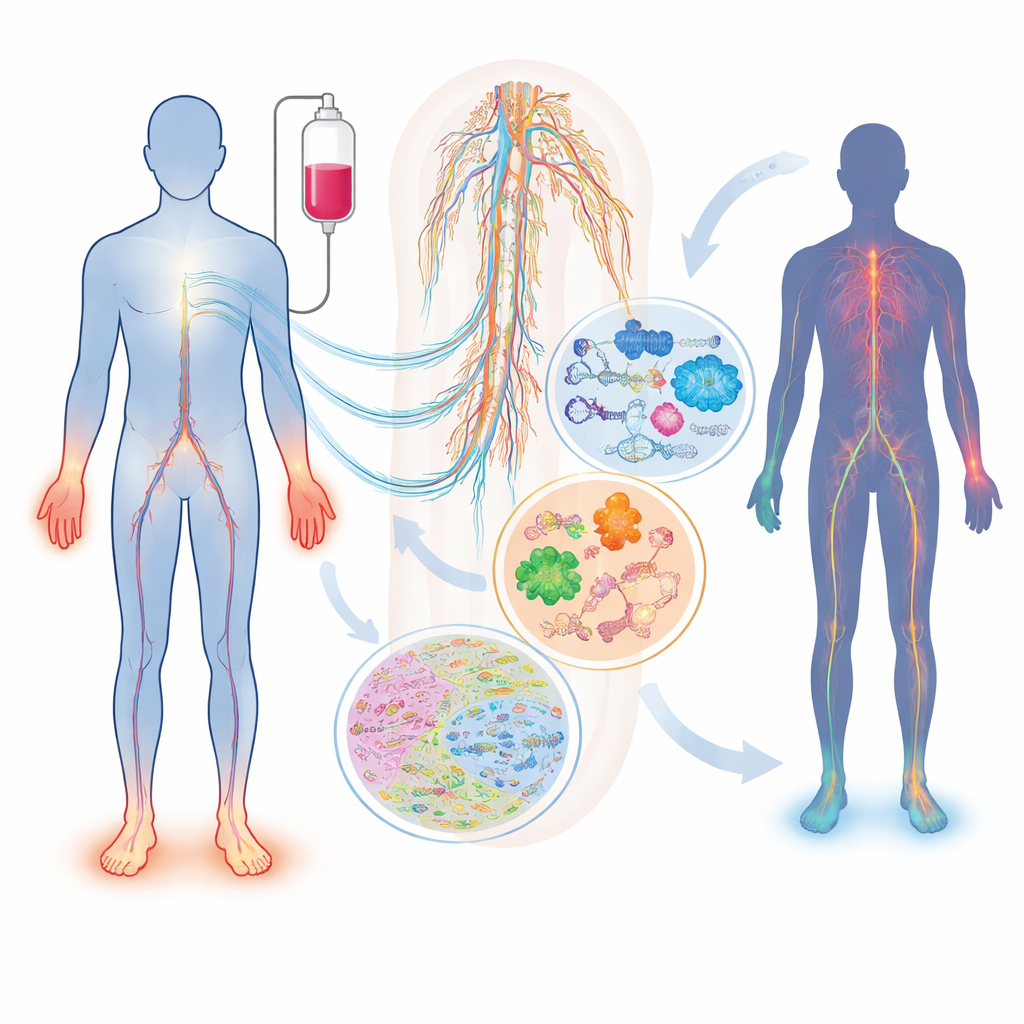
Cosa succede ai nervi durante la chemioterapia
Non tutti i pazienti esposti allo stesso farmaco e alla stessa dose sviluppano danno nervoso, e chi lo sviluppa può presentare sintomi molto diversi. La recensione descrive come farmaci ampiamente usati — come i taxani (paclitaxel, docetaxel), i composti a base di platino (cisplatino, oxaliplatino) e gli inibitori del proteasoma (bortezomib, carfilzomib) — possano lesionare in modi distinti i nervi sensitivi, motori e autonomi. Fattori come età, diabete, carenze vitaminiche, problemi renali o tiroidei e differenze ereditarie nei geni che regolano l’eliminazione dei farmaci o la struttura nervosa influenzano il rischio individuale. Un semplice marcatore ematico, la catena leggera dei neurofilamenti, può già monitorare il danno assonale sia negli animali sia nei pazienti, ma da solo non riesce a catturare la complessità della condizione né a spiegare perché si sviluppi.
Come le omiche forniscono una radiografia molecolare dei nervi danneggiati
Gli autori mostrano come la trascrittomica (profiling dell’RNA), la proteomica (analisi su larga scala delle proteine) e la metabolomica (studio sistematico delle piccole molecole) offrano ciascuna una lente diversa sul danno nervoso. L’attuale sequenziamento dell’RNA a singola cellula può distinguere molti sottotipi di neuroni sensoriali e cellule di supporto nei gangli della radice dorsale — ammassi di corpi cellulari nervosi vicino alla colonna vertebrale — e tracciare come ogni tipo risponde a diversi farmaci chemioterapici. Per esempio, fibre sensibili al tatto specifiche mostrano forti cambiamenti genici dopo paclitaxel, e alcuni geni legati all’invecchiamento nervoso e alla senescenza sono attivati dopo cisplatino. La proteomica ha rivelato spostamenti precoci in proteine che mantengono il citoscheletro, le centrali energetiche e le risposte allo stress, spesso giorni prima che gli animali manifestino comportamenti associati al dolore. La metabolomica mette in luce grandi alterazioni nei lipidi, negli amminoacidi e negli acidi biliari, indicando problemi nell’uso energetico, nella stabilità delle membrane e nell’infiammazione che possono variare a seconda del farmaco, dell’età e persino dei microbi intestinali.
Vedere dove avvengono i danni nei tessuti
Oltre a catalogare quali molecole cambiano, metodi più recenti di spettrometria di massa “spaziale” possono mostrare esattamente dove nel tessuto avvengono tali cambiamenti. L’imaging con citometria di massa e l’imaging con spettrometria di massa mappano proteine, lipidi, metaboliti e persino i composti chemioterapici stessi direttamente su sezioni nervose e fette di midollo spinale, preservando l’architettura di neuroni, cellule gliali e tessuto circostante. Lavori precoci hanno utilizzato questi strumenti per localizzare neuropeptidi legati al dolore e per tracciare come i lipidi si spostano in regioni precise dopo il danno nervoso. Hanno anche seguito depositi di platino a lunga durata derivanti dall’oxaliplatino nella pelle, suggerendo che molecole farmacologiche che permangono nei tessuti non tumorali possono contribuire a mantenere sintomi cronici. Sebbene solo pochi studi di questo tipo siano stati condotti specificamente sui nervi trattati con chemioterapia, la tecnologia è pronta a chiarire quali tipi cellulari e micro-regioni sono colpiti per primi, più gravemente e più a lungo.
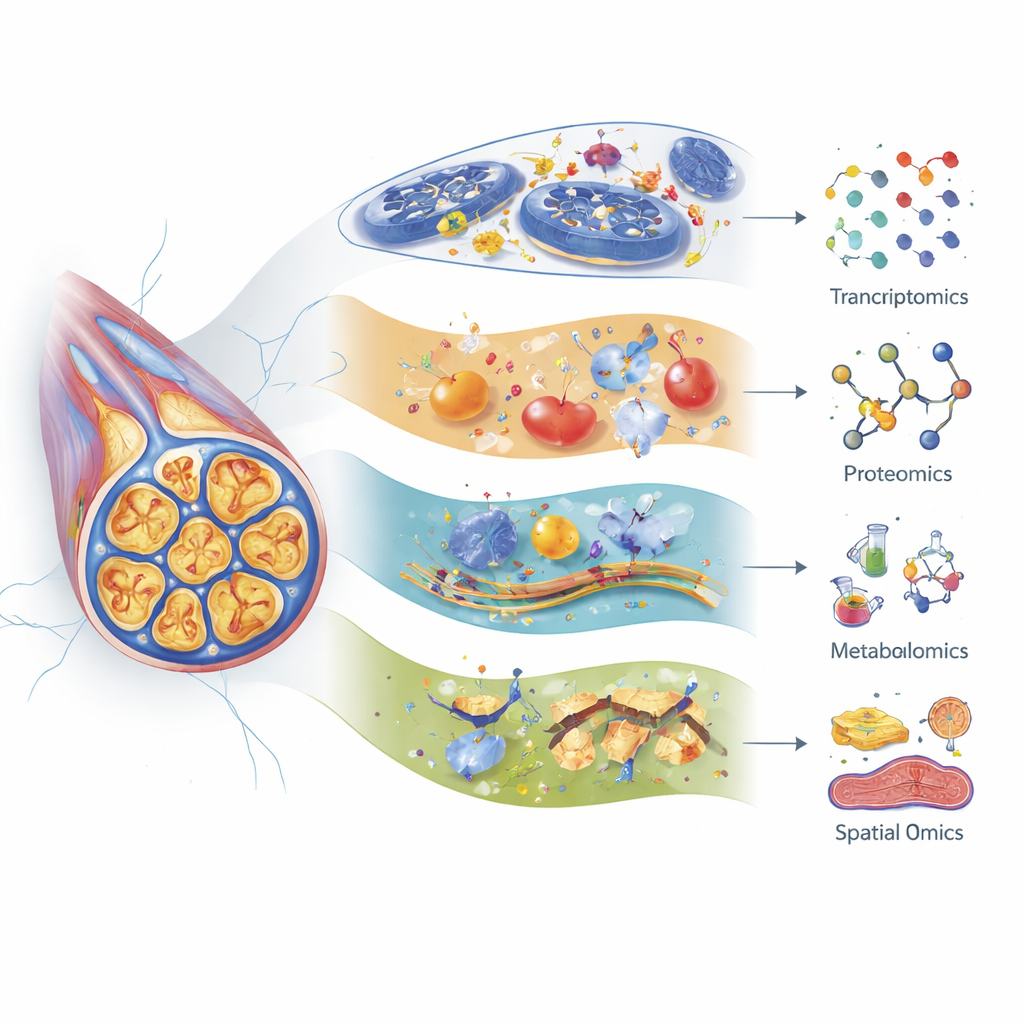
Mettere insieme tutti i pezzi molecolari
Nessun singolo tipo di omica può spiegare completamente perché alcuni pazienti sviluppano neuropatia grave e altri no. La recensione sostiene approcci integrati e multilivello che combinino variazioni genetiche, cambiamenti dell’RNA, reti proteiche, spostamenti metabolici, mappe spaziali, test di funzionalità nervosa e sintomi riferiti dai pazienti. Studi multi-omici precoci collegano già cambiamenti coordinati nella segnalazione lipidica, nelle vie infiammatorie, nello stress mitocondriale e in sistemi che modulano i nervi come gli endocannabinoidi e la segnalazione oppioide. Altri studi associano specifici messaggeri lipidici e acidi biliari derivati dall’intestino al dolore, suggerendo nuovi target farmacologici come recettori degli sfingolipidi o recettori delle chemochine che potrebbero attenuare il danno nervoso senza indebolire gli effetti antitumorali. Grandi studi umani progettati con cura che allineino i dati di laboratorio con i modelli clinici saranno cruciali per trasformare queste intuizioni in strumenti pratici.
Che implicazioni ha per la cura del cancro in futuro
Per un lettore non specialista, il messaggio centrale è incoraggiante: leggendo le impronte molecolari lasciate nel sangue, nel tessuto nervoso e persino nelle feci, gli scienziati cominciano a prevedere chi è più a rischio di danno nervoso, a capire come diversi farmaci danneggiano il sistema nervoso e a individuare punti deboli in quei percorsi che potrebbero essere protetti. Gli autori concludono che le omiche integrate, specialmente se applicate a campioni umani nel tempo, potrebbero a lungo termine guidare i medici nella scelta di farmaci e dosi oncologiche aderenti alla biologia di ciascuna persona, oltre a indicare nuove medicine che proteggano i nervi. Col tempo, questa visione a livello di sistema potrebbe permettere di mantenere i benefici delle potenti chemioterapie riducendo notevolmente il dolore e la disabilità persistenti che così spesso seguono.
Citazione: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Parole chiave: neuropatia periferica indotta dalla chemioterapia, multi-omica, danno ai nervi, effetti collaterali dei trattamenti oncologici, biomarcatori