Clear Sky Science · pl
Wykorzystanie zintegrowanego podejścia omicznego do odkrywania mechanizmów neuropatii obwodowej wywołanej chemioterapią (CIPN)
Dlaczego leczenie raka może uszkadzać nerwy
Chemioterapia ratuje życie, ale dla wielu pacjentów wiąże się z bolesnym kosztem: pieczeniem, mrowieniem lub drętwieniem rąk i stóp, które może utrzymywać się miesiącami lub latami. Ten stan, nazywany neuropatią obwodową wywołaną chemioterapią, może utrudniać chodzenie, sen, a nawet zapinanie guzika, i czasem zmusza lekarzy do zmniejszenia dawki lub przerwania skutecznych leków przeciwnowotworowych. Przeglądowy artykuł wyjaśnia, jak nowoczesne narzędzia „omiczne”, skanujące jednocześnie tysiące cząsteczek, zaczynają ujawniać, co idzie nie tak w nerwach podczas leczenia — i jak ta wiedza może doprowadzić do wcześniejszych sygnałów ostrzegawczych oraz delikatniejszej, bardziej spersonalizowanej opieki onkologicznej.
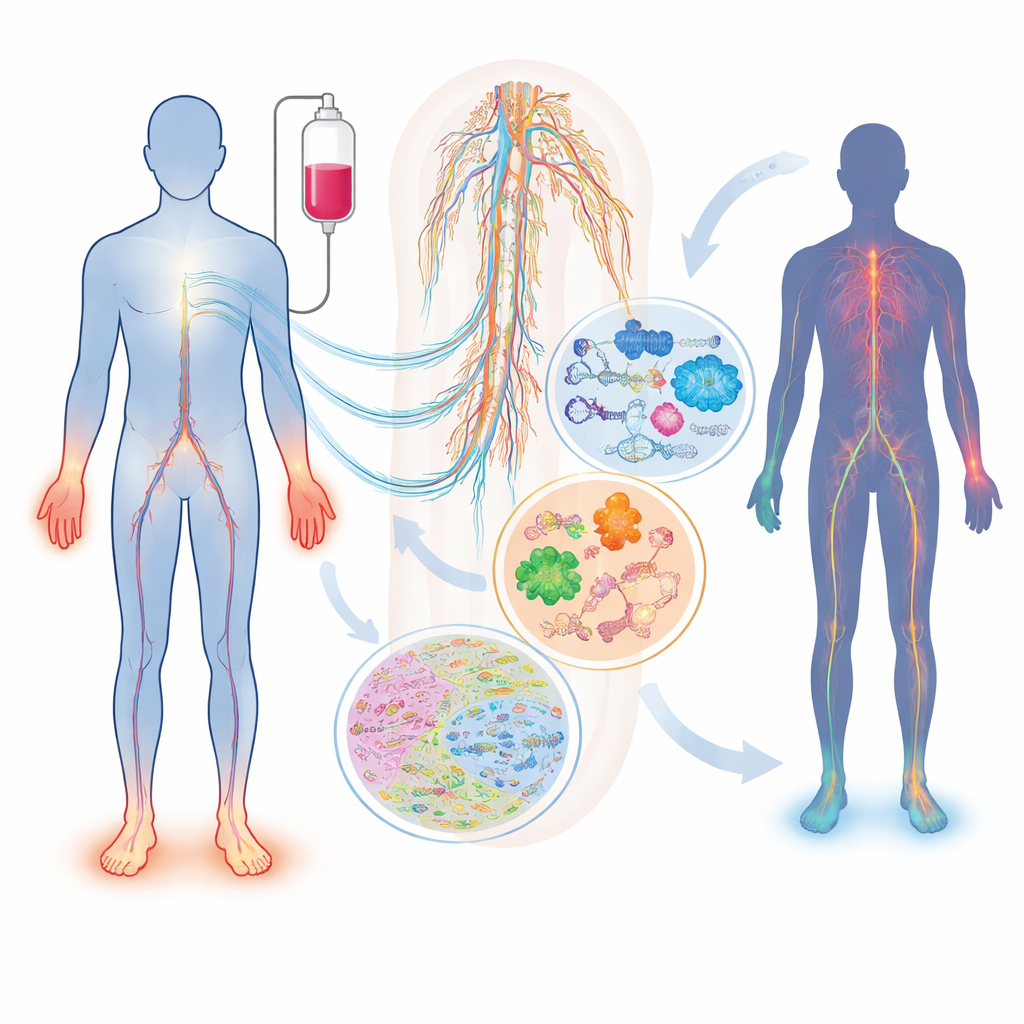
Co się dzieje z nerwami podczas chemioterapii
Nie wszyscy pacjenci otrzymujący ten sam lek i dawkę rozwijają uszkodzenie nerwów, a ci, którzy je doświadczają, mogą mieć bardzo różne objawy. Przegląd opisuje, jak powszechnie stosowane leki — takie jak taksany (paklitaksel, docetaksel), związki platyny (cisplatyna, oksaliplatyna) oraz inhibitory proteasomu (bortezomib, karfilzomib) — mogą uszkadzać nerwy czuciowe, ruchowe i autonomiczne na różne sposoby. Czynniki takie jak wiek, cukrzyca, niedobory witamin, problemy z nerkami lub tarczycą oraz dziedziczne różnice w genach kontrolujących metabolizm leków lub strukturę nerwów wpływają na indywidualne ryzyko. Jeden prosty marker we krwi, lekka podjednostka neurofilamentów, może już śledzić uszkodzenia aksonów u zwierząt i pacjentów, ale sam w sobie nie oddaje pełnej złożoności stanu ani nie tłumaczy, dlaczego się rozwija.
Jak omiki dają molekularne „rentgenowskie” spojrzenie na uszkodzone nerwy
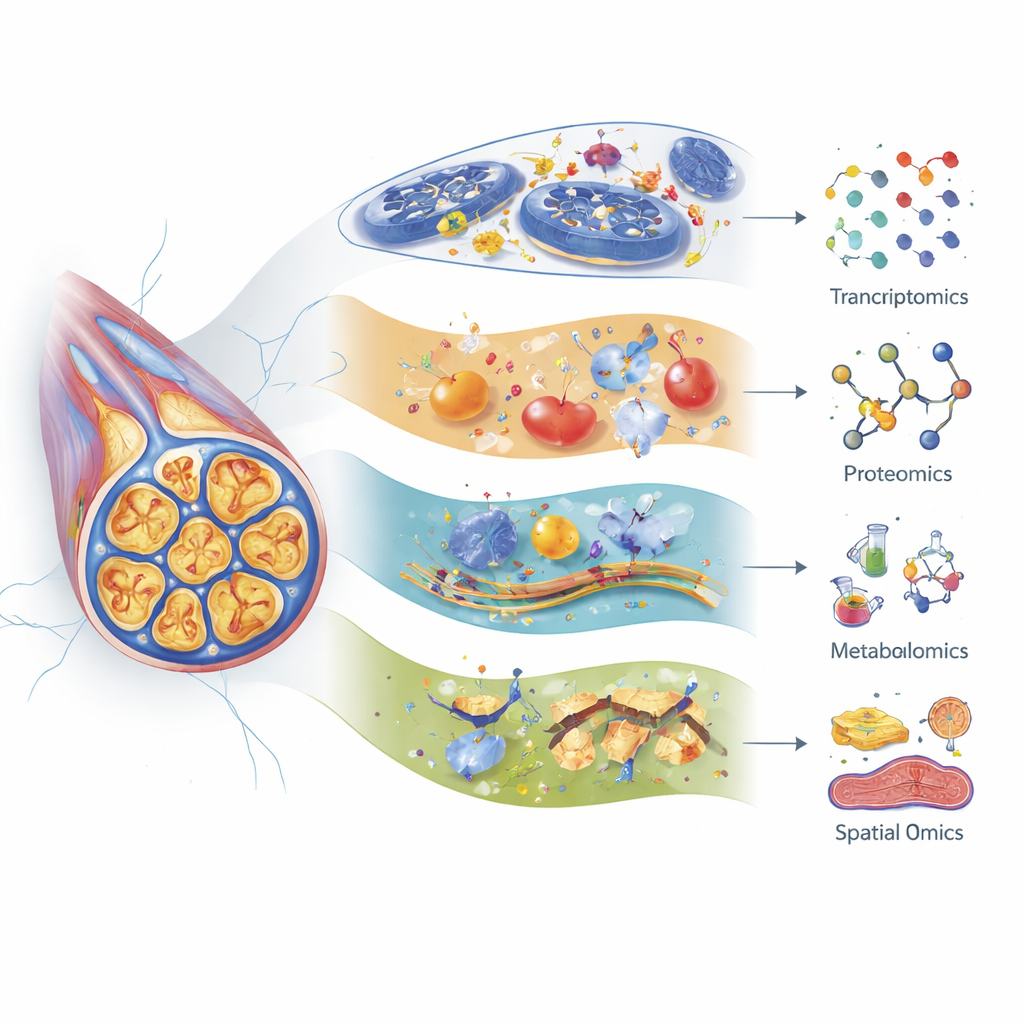
Autorzy pokazują, jak transkryptomika (profilowanie RNA), proteomika (analiza białek na dużą skalę) i metabolomika (systematyczne badanie małych cząsteczek) każda daje inną perspektywę na uszkodzenie nerwu. Nowoczesne sekwencjonowanie pojedynczych komórek RNA potrafi rozróżnić wiele podtypów neuronów czuciowych i komórek wspierających w zwojach rdzeniowych — skupiskach ciał komórek nerwowych blisko kręgosłupa — oraz śledzić, jak każdy typ reaguje na różne leki chemioterapeutyczne. Na przykład specyficzne włókna wrażliwe na dotyk wykazują silne zmiany genowe po podaniu paklitakselu, a niektóre geny powiązane ze starzeniem i senescencją nerwów aktywują się po cisplatynie. Proteomika ujawniła wczesne przesunięcia w białkach utrzymujących cytoszkielet, „fabryki energii” i odpowiedzi na stres, często na dni przed pojawieniem się u zwierząt zachowań wskazujących na ból. Metabolomika podkreśla duże zaburzenia w lipidach, aminokwasach i kwasach żółciowych, wskazując na problemy z wykorzystaniem energii, stabilnością błon i zapaleniem, które mogą się różnić w zależności od leku, wieku, a nawet mikrobiomu jelitowego.
Widzenie, gdzie występuje uszkodzenie w tkankach
Powyżej katalogowania, które cząsteczki się zmieniają, nowsze „przestrzenne” metody spektrometrii mas mogą pokazać dokładnie, gdzie w tkance te zmiany zachodzą. Obrazowanie cytometrii masowej i obrazowanie przy użyciu spektrometrii mas mapują białka, lipidy, metabolity, a nawet same związki chemioterapeutyczne bezpośrednio na przekrojach nerwów i fragmentach rdzenia kręgowego, zachowując architekturę neuronów, komórek glejowych i otaczających tkanek. Wczesne prace wykorzystały te narzędzia do lokalizacji neuropeptydów związanych z bólem oraz do odwzorowania, jak lipidy zmieniają się w precyzyjnych obszarach po uszkodzeniu nerwu. Śledzono też długo utrzymujące się złogi platyny po oksaliplatynie w skórze, sugerując, że cząsteczki leku zalegające w tkankach niebędących nowotworem mogą podtrzymywać przewlekłe objawy. Chociaż tylko kilka takich badań wykonano konkretnie na nerwach leczonych chemioterapią, technologia ta ma potencjał wyjaśnić, które typy komórek i mikroobszary są uderzane najpierw, najmocniej i najdłużej.
Składanie wszystkich molekularnych elementów w całość
Żaden pojedynczy rodzaj omików nie może w pełni wyjaśnić, dlaczego niektórzy pacjenci rozwijają ciężką neuropatię, a inni nie. Przegląd argumentuje za zintegrowanymi, wielowarstwowymi podejściami, które łączą zmienność genetyczną, zmiany RNA, sieci białkowe, przesunięcia metabolitów, mapy przestrzenne, testy funkcji nerwów i objawy zgłaszane przez pacjentów. Wczesne badania multi-omics już łączą skoordynowane zmiany w sygnalizacji lipidowej, szlakach zapalnych, stresie mitochondrialnym oraz systemach modulujących nerwy, takich jak endokannabinoidy i sygnalizacja opioidowa. Inne powiązały konkretne przekaźniki lipidowe i pochodne z jelit kwasy żółciowe z bólem, sugerując nowe cele lekowe, takie jak receptory sfingolipidowe czy receptory chemokin, które mogłyby osłabić uszkodzenie nerwów bez osłabiania efektu przeciwnowotworowego. Duże, starannie zaprojektowane badania u ludzi, które wyrównają dane laboratoryjne z wzorcami klinicznymi, będą kluczowe, aby przekształcić te wnioski w praktyczne narzędzia.
Co to oznacza dla przyszłej opieki onkologicznej
Dla czytelnika nieprofesjonalnego główne przesłanie jest nadziejne: czytając molekularne odciski palców pozostawione we krwi, tkance nerwowej, a nawet stolcu, naukowcy zaczynają przewidywać, kto jest najbardziej narażony na uszkodzenie nerwów, rozumieć, jak różne leki uszkadzają układ nerwowy, i identyfikować słabe punkty tych ścieżek, które można chronić. Autorzy konkludują, że zintegrowane omiki, zwłaszcza stosowane do próbek ludzkich w czasie, mogą ostatecznie pomagać lekarzom w wybieraniu leków przeciwnowotworowych i dawek dopasowanych do biologii konkretnej osoby, a także wskazywać nowe leki chroniące nerwy przed uszkodzeniem. Z czasem to systemowe spojrzenie może umożliwić zachowanie korzyści potężnych chemioterapii przy jednoczesnym znacznym zmniejszeniu długotrwałego bólu i niepełnosprawności, które tak często następują.
Cytowanie: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Słowa kluczowe: neuropatia obwodowa wywołana chemioterapią, multi-omics, uszkodzenie nerwów, efekty uboczne leczenia raka, biomarkery