Clear Sky Science · ru
Использование интегрированного омics‑подхода для выявления механизмов химиотерапией-индуцируемой периферической невропатии (CIPN)
Почему лечение рака может вредить нервам
Химиотерапия спасает жизни, но для многих она связана с неприятной расплатой: жжением, покалыванием или онемением в руках и ногах, которые могут сохраняться месяцы или годы. Это состояние, называемое химиотерапией‑индуцируемой периферической невропатией, затрудняет ходьбу, сон и даже застёгивание рубашки, а иногда вынуждает врачей снижать дозы или прекращать приёмы эффективных противоопухолевых препаратов. Рассматриваемая статья объясняет, как современные инструменты «омики», сканирующие тысячи молекул одновременно, начинают показывать, что идёт не так в нервах во время лечения — и как эти знания могут привести к ранним признакам риска и более щадящей, персонализированной онкологической помощи.
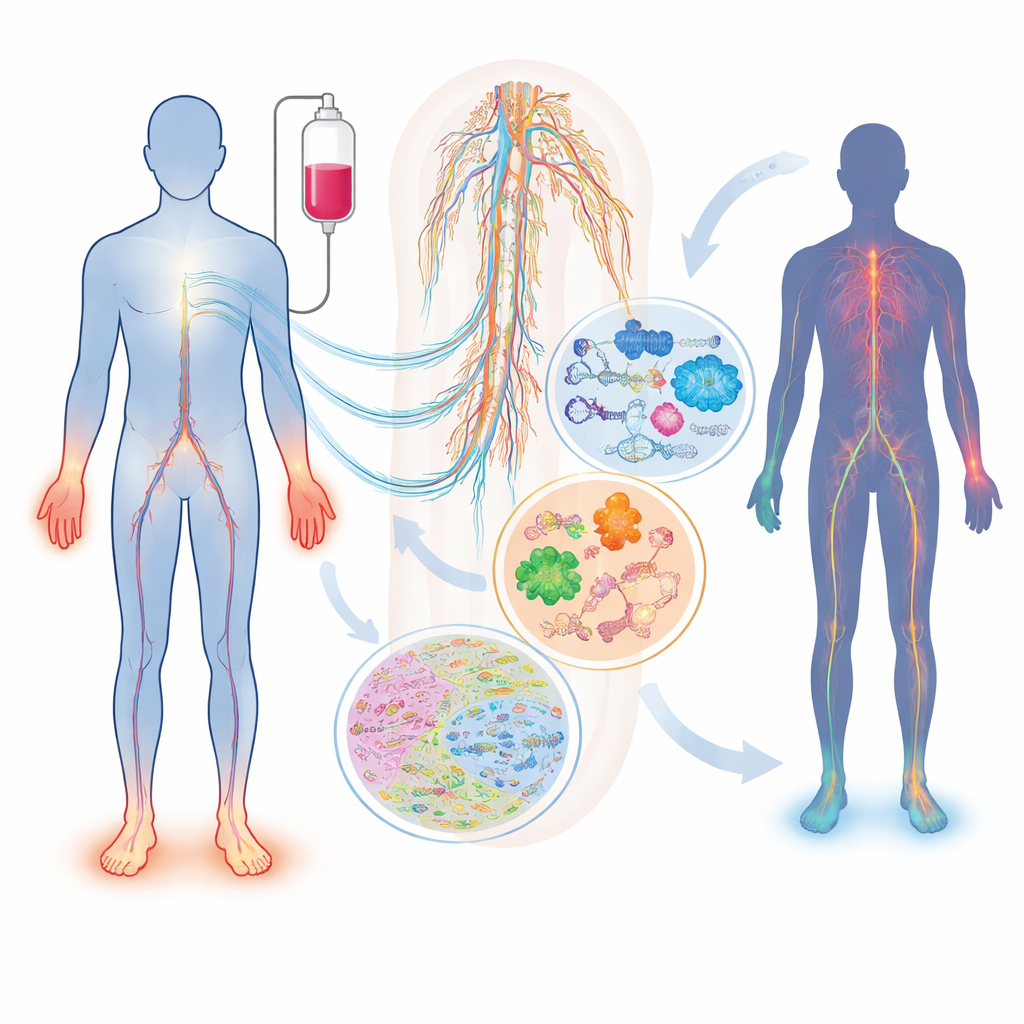
Что происходит с нервами во время химиотерапии
Не все пациенты, получающие один и тот же препарат и дозу, развивают повреждение нервов, а у тех, кто его испытывает, симптомы могут сильно различаться. В обзоре описано, как широко применяемые препараты — такие как таксаны (паклитаксел, доцетаксел), соединения платины (цисплатин, оксалиплатин) и ингибиторы протеасомы (бортезомиб, карфилзомиб) — по‑разному повреждают сенсорные, моторные и вегетативные нервы. Такие факторы, как возраст, диабет, дефицит витаминов, нарушения функции почек или щитовидной железы, а также наследственные варианты в генах, контролирующих метаболизм препаратов или структуру нервов, меняют индивидуальный риск. Один простой маркер в крови — лёгкая цепь нейрофиламента — уже может отслеживать аксональное повреждение у животных и пациентов, но сам по себе он не захватывает всю сложность состояния и не объясняет, почему оно развивается.
Как омics дают молекулярный «рентген» повреждённых нервов
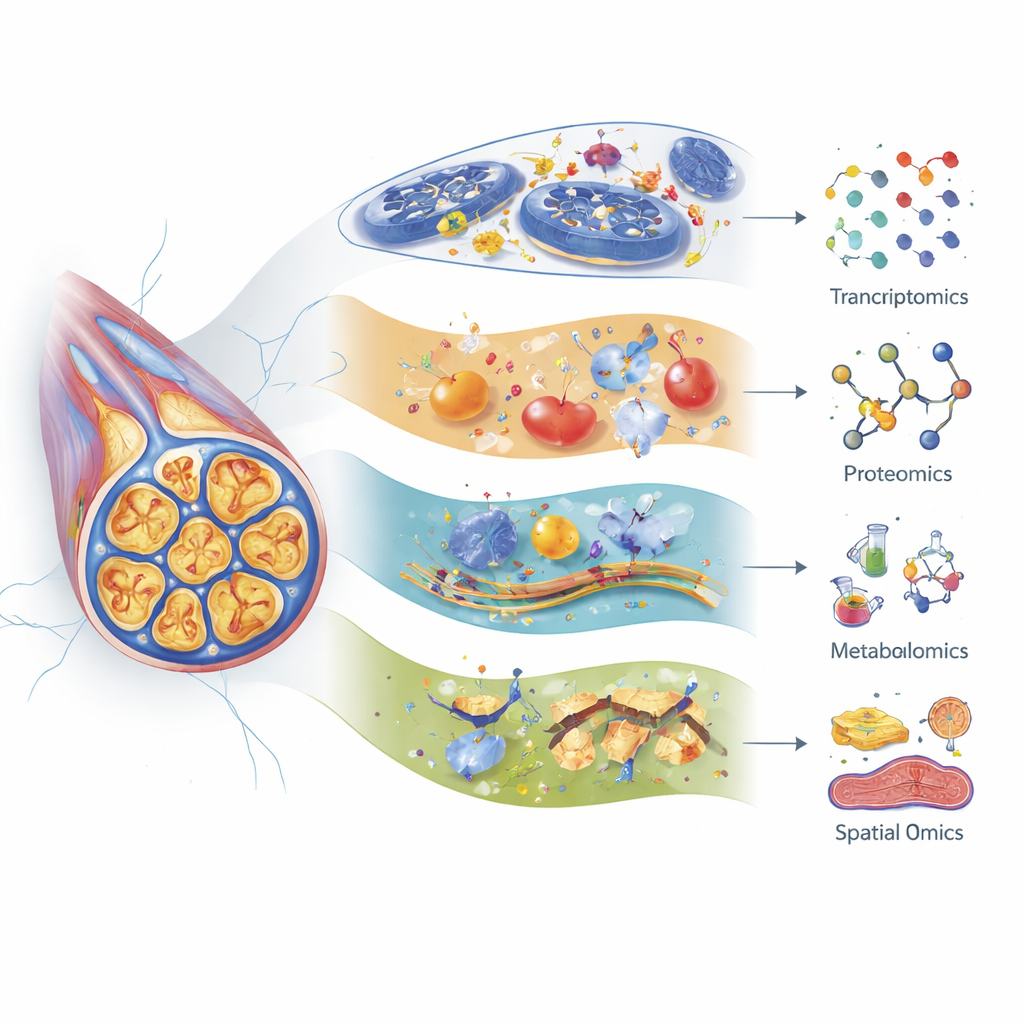
Авторы показывают, как транскриптомика (профилирование РНК), протеомика (масштабный анализ белков) и метаболомика (системное изучение малых молекул) дают разные ракурсы на повреждение нервов. Современные методы секвенирования РНК по одиночным клеткам позволяют различать многие подтипы сенсорных нейронов и вспомогательных клеток в дорсальных корешковых ганглиях — скоплениях тел нейронов у позвоночника — и отслеживать, как каждый тип реагирует на разные химиопрепараты. Так, определённые волокна, чувствительные к прикосновению, демонстрируют сильные изменения экспрессии генов после паклитаксела, а некоторые гены, связанные со старением нервов и сенесценцией, активируются после цисплатина. Протеомика выявила ранние сдвиги в белках, поддерживающих цитоскелет, энергетические фермы и реакции на стресс, часто за дни до появления у животных поведенческих признаков боли. Метаболомика подчёркивает серьёзные нарушения в липидах, аминокислотах и желчных кислотах, указывая на проблемы с энергетическим обменом, стабильностью мембран и воспалением, которые могут различаться в зависимости от препарата, возраста и даже микробиоты кишечника.
Видеть, где именно происходят повреждения в тканях
Помимо каталогизации изменяющихся молекул, новые «пространственные» методы масс-спектрометрии могут показать, где именно в ткани происходят эти изменения. Имеджинговая масс‑цитометрия и визуализация с помощью масс‑спектрометрии наносят карты белков, липидов, метаболитов и даже самих химиопрепаратов прямо на разрезы нервной ткани и срезы спинного мозга, сохраняя архитектуру нейронов, глиальных клеток и окружающей ткани. Ранние исследования использовали эти инструменты для локализации нейропептидов, связанных с болью, и для картирования смещений липидов в точных регионах после повреждения нерва. Они также отслеживали долгоживущие отложения платины от оксалиплатина в коже, что наводит на мысль, что молекулы препарата, остающиеся в неонкологических тканях, могут поддерживать хронические симптомы. Несмотря на то, что подобных исследований специально в нервах, обработанных химиотерапией, пока немного, технология готова прояснить, какие типы клеток и микро‑регионы поражаются первыми, сильнее всего и надолго.
Собирая все молекулярные фрагменты воедино
Ни один отдельный тип омics не может полностью объяснить, почему у одних пациентов развивается тяжёлая невропатия, а у других — нет. В обзоре обосновывается необходимость интегрированных многоуровневых подходов, объединяющих генетические вариации, изменения РНК, сети белков, сдвиги метаболитов, пространственные карты, тесты функции нервов и симптомы, сообщаемые пациентами. Ранние мультиомные исследования уже связывают координированные изменения в липидной сигнализации, воспалительных путях, митохондриальном стрессе и системах, модулирующих нервную функцию, таких как эндоканнабиноиды и опиоидная сигнализация. Другие работы связывают конкретные липидные посредники и желчные кислоты, происходящие из кишечника, с болью, предлагая новые лекарственные мишени, например рецепторы сфинголипидов или хемокиновые рецепторы, которые могли бы ослабить повреждение нервов, не снижая противоракового эффекта. Для превращения этих идей в практические инструменты будут критически важны крупные, тщательно спланированные исследования на людях, согласующие лабораторные данные с клиническими моделями.
Что это значит для будущей онкологической помощи
Для неспециалиста главный вывод обнадёживающий: читая молекулярные отпечатки, остающиеся в крови, нервной ткани и даже стуле, учёные начинают предсказывать, кто наиболее подвержен риску повреждения нервов, понимать, как разные препараты повреждают нервную систему, и выявлять уязвимые звенья в этих путях, которые можно защитить. Авторы делают вывод, что интегрированная омика, особенно при применении к образцам людей в динамике, в конечном итоге может помочь врачам выбирать препараты и дозы, соответствующие биологии каждого пациента, а также указать на новые лекарства, защищающие нервы от вреда. Со временем такой системный взгляд может позволить сохранить преимущества мощной химиотерапии, существенно снижая продолжительную боль и инвалидность, которые так часто за ней следуют.
Цитирование: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Ключевые слова: химиотерапией-индуцируемая периферическая невропатия, мультиомика, повреждение нервов, побочные эффекты лечения рака, биомаркеры