Clear Sky Science · es
Uso de un enfoque ómico integrado para descubrir los mecanismos subyacentes de la neuropatía periférica inducida por quimioterapia (CIPN)
Por qué el tratamiento del cáncer puede dañar los nervios
La quimioterapia salva vidas, pero para muchas personas tiene un coste preocupante: ardor, hormigueo o entumecimiento en manos y pies que puede durar meses o años. Esta condición, llamada neuropatía periférica inducida por quimioterapia, puede dificultar caminar, dormir e incluso abrocharse una camisa, y a veces obliga a los médicos a reducir o suspender fármacos contra el cáncer que de otro modo serían efectivos. El artículo revisado explica cómo las herramientas ómicas de vanguardia, que analizan miles de moléculas a la vez, comienzan a revelar qué falla en los nervios durante el tratamiento y cómo ese conocimiento podría conducir a señales de alarma tempranas y a una atención oncológica más suave y personalizada.
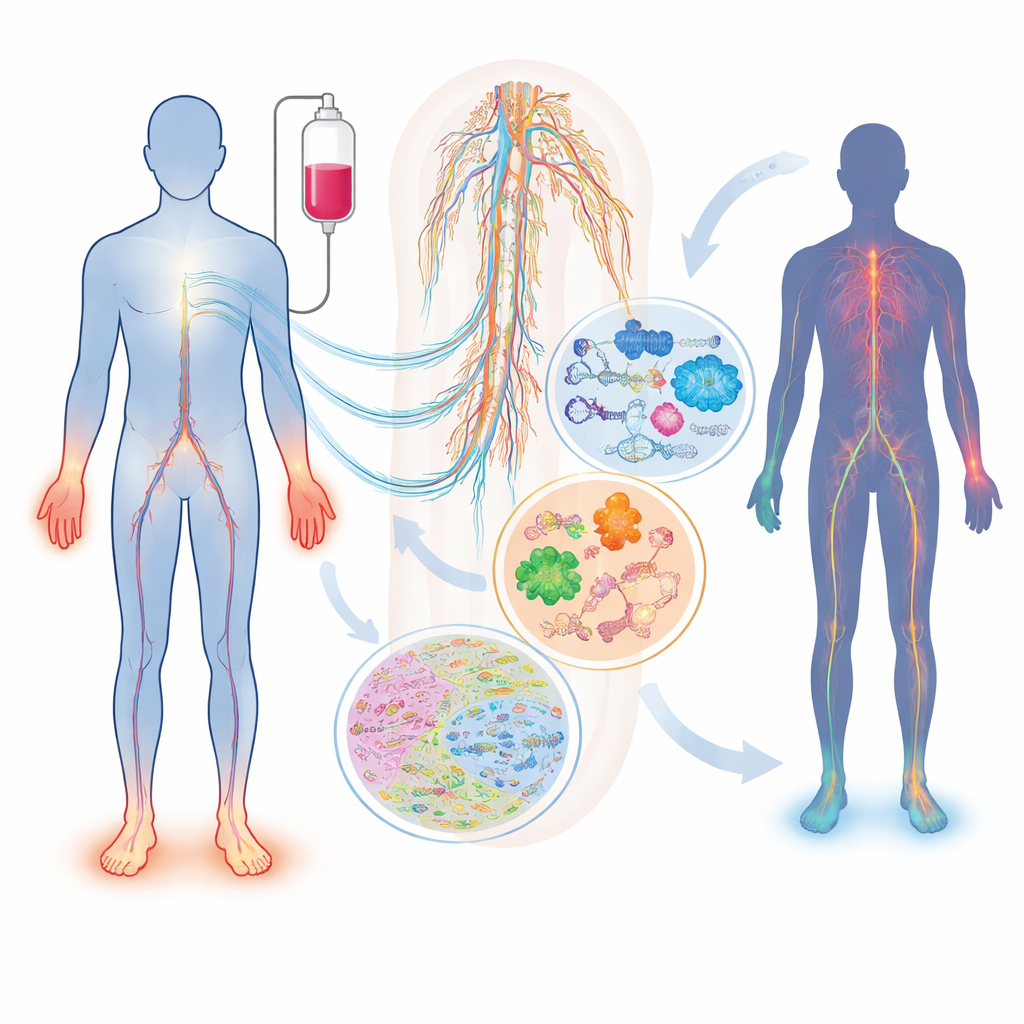
Qué les sucede a los nervios durante la quimioterapia
No todos los pacientes expuestos al mismo fármaco y dosis desarrollan daño nervioso, y quienes sí lo hacen pueden experimentar síntomas muy distintos. La revisión describe cómo fármacos de uso habitual —como los taxanos (paclitaxel, docetaxel), los compuestos de platino (cisplatino, oxaliplatino) y los inhibidores del proteasoma (bortezomib, carfilzomib)— pueden lesionar nervios sensoriales, motores y autónomos de maneras diferentes. Factores como la edad, la diabetes, deficiencias vitamínicas, problemas renales o tiroideos y diferencias hereditarias en genes que regulan el manejo del fármaco o la estructura nerviosa modifican el riesgo individual. Un marcador sanguíneo sencillo, la cadena ligera de neurofilamento, ya puede seguir el daño axonal en animales y pacientes, pero por sí solo no captura la complejidad completa de la condición ni explica por qué se desarrolla en primer lugar.
Cómo las ómicas ofrecen una radiografía molecular de los nervios lesionados
Los autores muestran cómo la transcriptómica (perfilado de ARN), la proteómica (análisis a gran escala de proteínas) y la metabolómica (estudio sistemático de pequeñas moléculas) ofrecen cada una una lente distinta sobre la lesión nerviosa. La secuenciación de ARN de célula única moderna puede distinguir muchos subtipos de neuronas sensoriales y células de soporte en los ganglios de la raíz dorsal —acúmulos de cuerpos celulares nerviosos cerca de la médula— y seguir cómo responde cada tipo a distintos fármacos quimioterápicos. Por ejemplo, fibras específicas sensibles al tacto muestran cambios génicos intensos tras paclitaxel, y algunos genes vinculados al envejecimiento nervioso y la senescencia se activan tras cisplatino. La proteómica ha revelado cambios tempranos en proteínas que mantienen el citoesqueleto celular, las fábricas de energía y las respuestas al estrés, con frecuencia días antes de que los animales muestren comportamientos indicativos de dolor. La metabolómica destaca alteraciones importantes en lípidos, aminoácidos y ácidos biliares, apuntando a problemas en el uso de energía, la estabilidad de membranas y la inflamación que pueden diferir según el fármaco, la edad e incluso los microbios intestinales.
Ver dónde ocurre el daño dentro de los tejidos
Más allá de catalogar qué moléculas cambian, los métodos más recientes de espectrometría de masas «espacial» pueden mostrar exactamente dónde en el tejido se producen esos cambios. La citometría de masas de imagen y la imagen por espectrometría de masas cartografían proteínas, lípidos, metabolitos e incluso los propios compuestos quimioterápicos directamente en secciones nerviosas y cortes de la médula espinal, preservando la arquitectura de las neuronas, las células gliales y el tejido circundante. Trabajos iniciales han utilizado estas herramientas para localizar neuropéptidos relacionados con el dolor y trazar cómo los lípidos se desplazan en regiones precisas tras la lesión nerviosa. También han seguido depósitos duraderos de platino procedentes del oxaliplatino en la piel, lo que sugiere que moléculas del fármaco que persisten en tejidos no cancerosos podrían ayudar a mantener los síntomas crónicos. Aunque solo se han realizado unos pocos estudios de este tipo específicamente en nervios tratados con quimioterapia, la tecnología está lista para aclarar qué tipos celulares y microregiones son los primeros, los más afectados y los más duraderos.
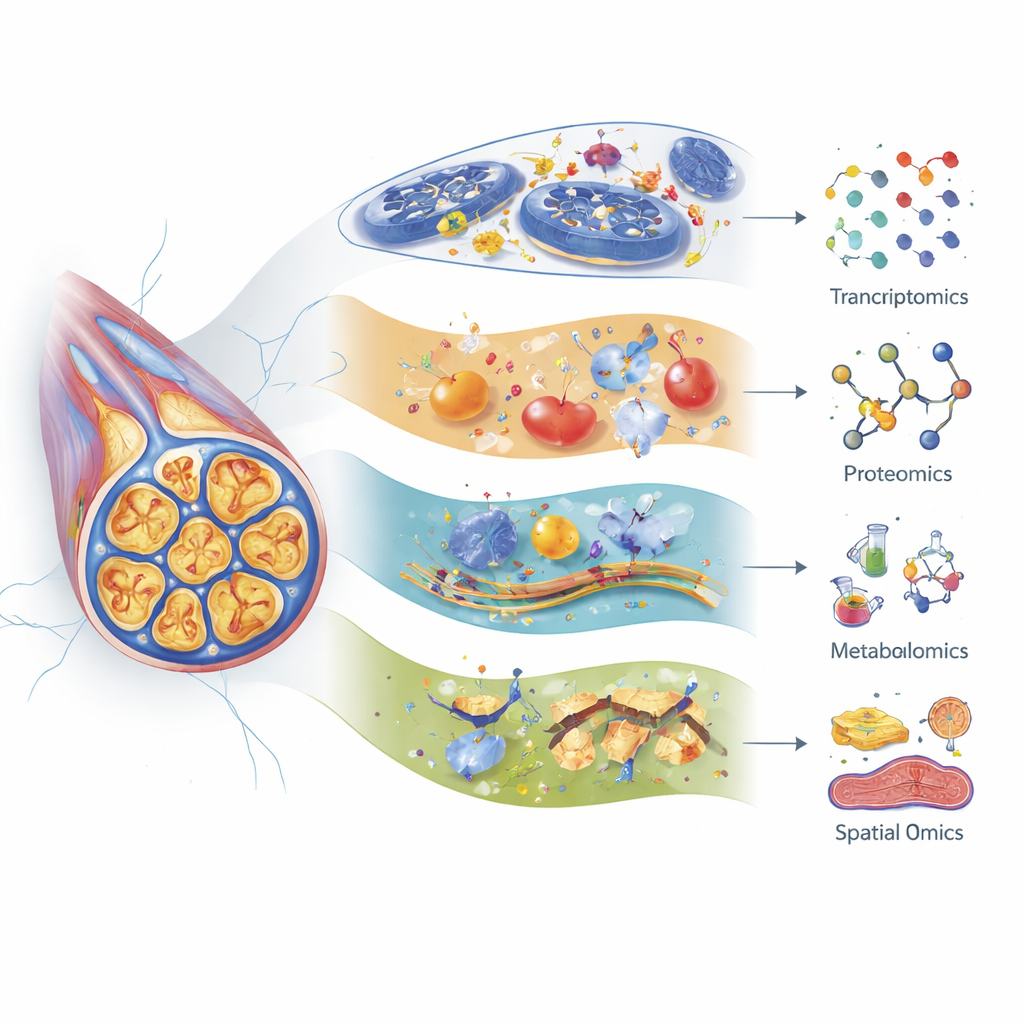
Integrando todas las piezas moleculares
Ningún tipo de ómica por sí sola puede explicar completamente por qué algunos pacientes desarrollan neuropatía severa y otros no. La revisión aboga por enfoques integrados y multicapa que combinen variación genética, cambios en ARN, redes de proteínas, alteraciones metabólicas, mapas espaciales, pruebas de función nerviosa y síntomas reportados por los pacientes. Estudios multi-ómicos tempranos ya vinculan cambios coordinados en la señalización lipídica, vías inflamatorias, estrés mitocondrial y sistemas que modulan el nervio, como los endocannabinoides y la señalización opiácea. Otros asocian mensajeros lipídicos específicos y ácidos biliares de origen intestinal con el dolor, lo que sugiere nuevos objetivos farmacológicos como receptores de esfingolípidos o receptores de quimiocinas que podrían mitigar la lesión nerviosa sin debilitar los efectos anticancerígenos. Serán cruciales estudios humanos grandes y cuidadosamente diseñados que alineen los datos de laboratorio con los patrones clínicos para convertir estos hallazgos en herramientas prácticas.
Qué significa esto para la atención del cáncer en el futuro
Para un lector no especialista, el mensaje central es esperanzador: al leer las huellas moleculares dejadas en sangre, tejido nervioso e incluso heces, los científicos comienzan a predecir quién tiene más riesgo de daño nervioso, entender cómo distintos fármacos lesionan el sistema nervioso e identificar puntos débiles en esas vías que podrían protegerse. Los autores concluyen que las ómicas integradas, especialmente cuando se aplican a muestras humanas a lo largo del tiempo, podrían eventualmente guiar a los médicos a escoger fármacos y dosis que se ajusten a la biología de cada persona, al tiempo que señalen nuevos medicamentos que protejan los nervios del daño. Con el tiempo, esta visión a nivel de sistemas podría posibilitar conservar los beneficios de las quimioterapias potentes reduciendo en gran medida el dolor y la discapacidad duraderos que tan a menudo siguen a estos tratamientos.
Cita: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Palabras clave: neuropatía periférica inducida por quimioterapia, multi-ómica, daño nervioso, efectos secundarios del tratamiento del cáncer, biomarcadores