Clear Sky Science · ja
化学療法誘発末梢神経障害(CIPN)の基礎メカニズムを明らかにするための統合オミクスアプローチの活用
なぜがん治療が神経を傷めるのか
化学療法は命を救いますが、多くの人にとって代償が伴います。手足の焼けるような痛み、しびれ、または感覚の喪失が数か月から数年続くことがあり、これを化学療法誘発末梢神経障害(CIPN)と呼びます。歩行、睡眠、シャツのボタンを留めるといった日常動作が困難になり、場合によっては有効ながん薬を減量したり中止せざるを得ないこともあります。レビュー論文は、数千もの分子を同時に解析する最先端の“オミクス”ツールが、治療中に神経で何が起きているかをどのように明らかにしつつあるか、そしてその知見が早期警告やより穏やかで個別化されたがん医療につながる可能性を説明しています。
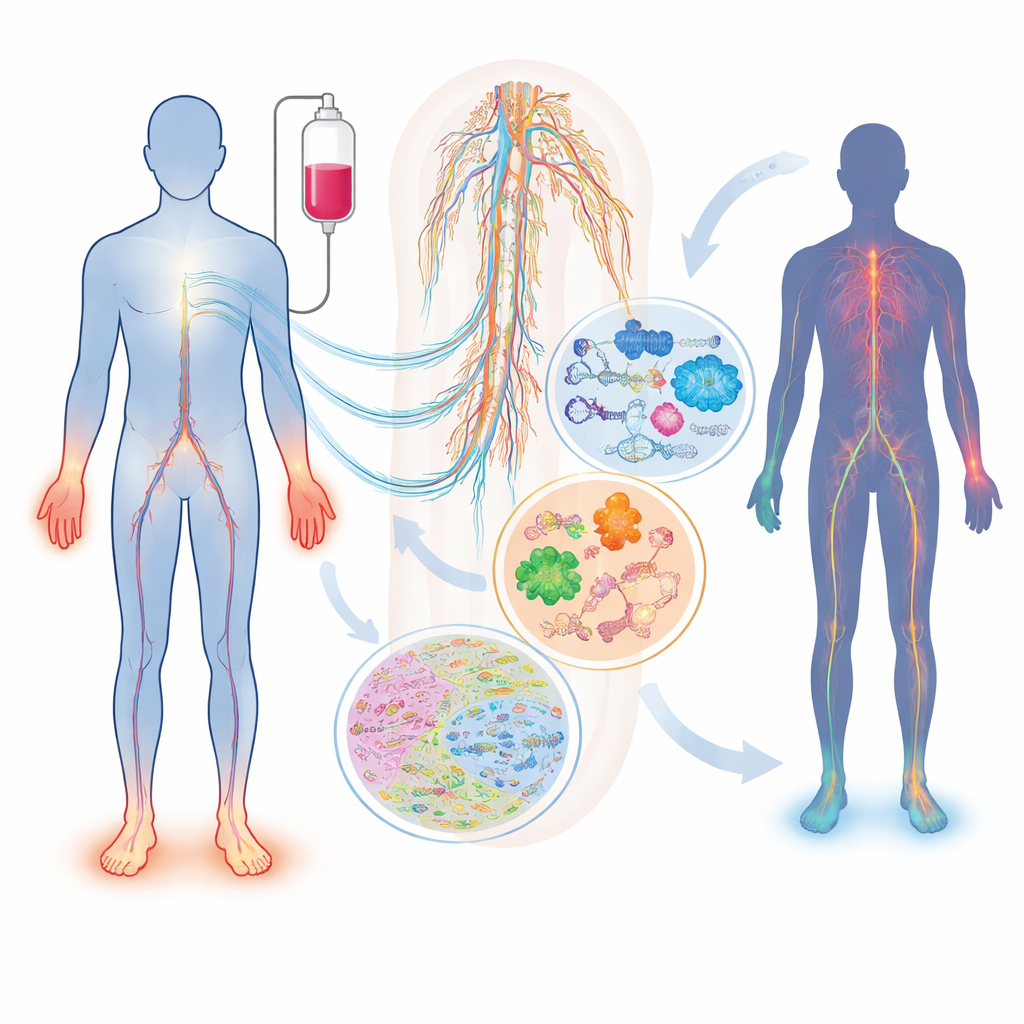
化学療法中に神経で起きること
同じ薬と同じ用量に曝されたすべての患者が神経障害を発症するわけではなく、発症した患者でも症状は大きく異なり得ます。レビューは、タキサン(パクリタキセル、ドセタキセル)、プラチナ製剤(シスプラチン、オキサリプラチン)、プロテアソーム阻害剤(ボルテゾミブ、カルフィルゾミブ)など広く使われる薬剤が、感覚神経、運動神経、自律神経をそれぞれ異なる方法で傷害し得ることを示しています。年齢、糖尿病、ビタミン欠乏、腎機能や甲状腺の問題、薬物動態や神経構造を制御する遺伝的差異などは、個人のリスクを変動させます。血液中の単純なマーカーであるニューロフィラメントライトチェーンは、動物と患者の両方で軸索損傷を追跡できますが、それだけでは状態の複雑さを完全に捉えたり、なぜ発症するのかを説明することはできません。
オミクスが損傷した神経の分子“X線”を与える方法
著者らは、トランスクリプトミクス(RNAプロファイリング)、プロテオミクス(大規模タンパク質解析)、メタボロミクス(小分子の体系的研究)がそれぞれ神経損傷を異なる角度から映し出すことを示します。最新の単一細胞RNAシーケンシングは、脊髄近くにある神経細胞体の集まりである背根神経節(DRG)内の多くの感覚ニューロン亜型や支持細胞を識別し、各タイプが異なる化学療法薬にどう反応するかを追跡できます。例えば、特定の触覚感受性線維はパクリタキセル後に強い遺伝子変化を示し、シスプラチン後には神経の老化や細胞老化に関連する遺伝子が活性化されることがあります。プロテオミクスは、細胞骨格、エネルギー産生装置、ストレス応答を維持するタンパク質の初期変動を明らかにしており、しばしば動物が疼痛行動を示すよりも数日前に検出されます。メタボロミクスは脂質、アミノ酸、胆汁酸の大きな乱れを強調し、薬剤、年齢、さらには腸内微生物によって異なるエネルギー利用、膜安定性、炎症の問題を示唆します。
組織内で損傷が起きる場所を可視化する
どの分子が変化するかを列挙するだけでなく、新しい“空間的”質量分析法は、それらの変化が組織のどこで起きているかを正確に示すことができます。イメージング質量サイトメトリーや質量顕微鏡法は、タンパク質、脂質、代謝物、さらには化学療法薬自体を神経切片や脊髄薄片上に直接マッピングし、ニューロン、グリア細胞、周辺組織の構造を保存します。初期の研究では、これらのツールを用いて痛みに関連するニューロペプチドの局在化や、神経損傷後の特定領域での脂質変動の図式化が行われてきました。また、オキサリプラチン由来のプラチナが皮膚に長期間蓄積する様子も追跡され、がん組織以外に薬剤分子が残留することが慢性症状を持続させる一因になり得ることが示唆されています。化学療法処置を受けた神経で具体的に行われた研究はまだ少数ですが、この技術はどの細胞型と微小領域が最初に、最も強く、最も長く影響を受けるかを明らかにする可能性を秘めています。
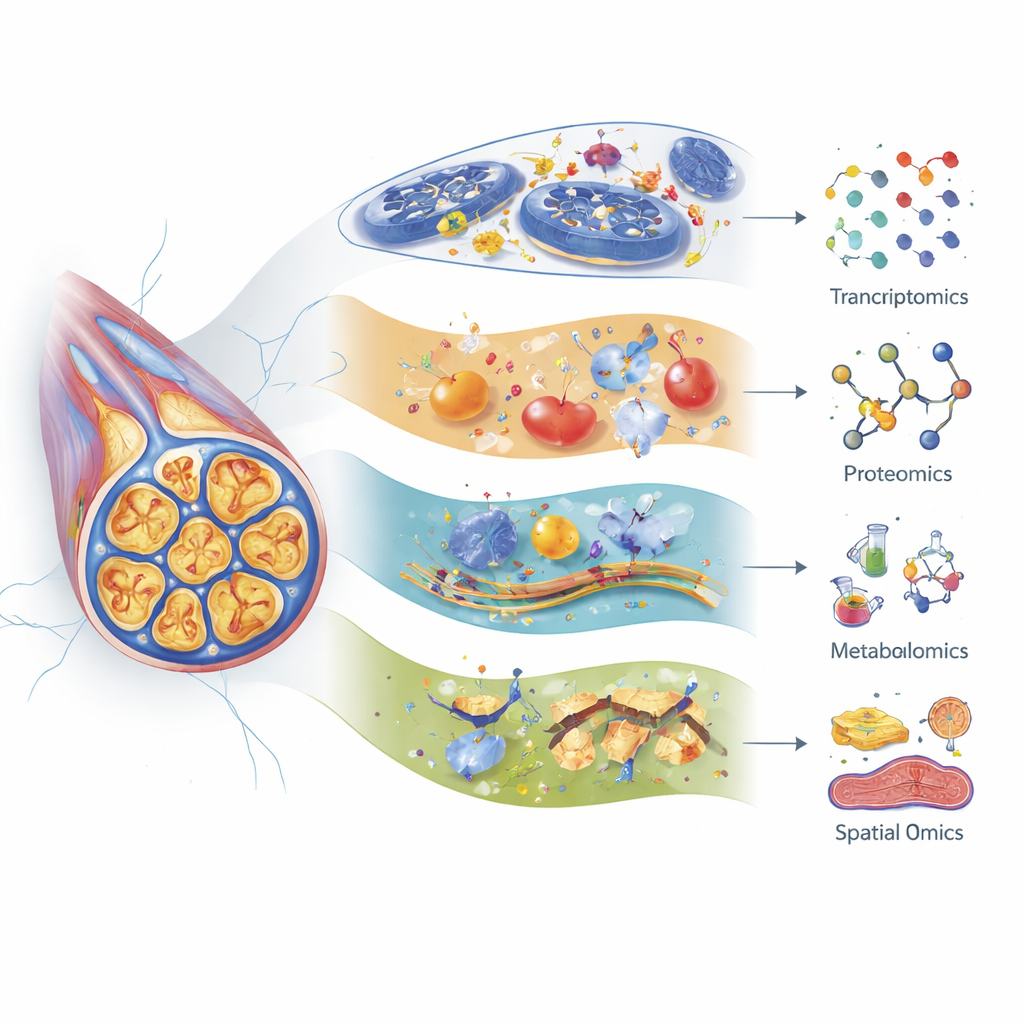
すべての分子情報を統合する
単一のオミクスだけでは、なぜ一部の患者が重度の神経障害を発症し、他は発症しないのかを完全には説明できません。レビューは、遺伝的変異、RNAの変化、タンパク質ネットワーク、代謝物の変動、空間マップ、神経機能検査、患者報告症状を組み合わせた統合的なマルチレイヤーアプローチを主張しています。初期のマルチオミクス研究は、脂質シグナル、炎症経路、ミトコンドリアストレス、エンドカンナビノイドやオピオイドのような神経調節系における協調的変化を既に結びつけています。ほかには、特定の脂質メッセンジャーや腸由来の胆汁酸を疼痛と結びつけ、スフィンゴ脂質受容体やケモカイン受容体など、がん治療効果を損なわずに神経損傷を和らげ得る新たな薬剤標的を示唆する研究もあります。臨床パターンと研究データを整合させる大規模で注意深く設計されたヒト研究が、これらの知見を実用的なツールに変えるうえで重要になるでしょう。
将来のがん医療にとっての意味
一般読者への核心的メッセージは希望的です。血液、神経組織、さらには便に残された分子の指紋を読み取ることで、誰が神経損傷のリスクが高いかを予測し、異なる薬剤が神経系にどのように損傷を与えるかを理解し、その経路の弱点を保護する方法を見つけ始めているのです。著者らは、特にヒトサンプルに対して時間を追って適用される統合オミクスが、最終的には医師が個々人の生物学に合わせた薬剤や用量を選ぶ際の指針になり得ると結論づけています。同時に神経を保護する新薬の開発にもつながる可能性があります。やがて、このシステムレベルの見方により、強力な化学療法の利益を維持しつつ、それに続く長期の痛みや障害を大幅に減らすことが可能になるかもしれません。
引用: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
キーワード: 化学療法誘発末梢神経障害, マルチオミクス, 神経損傷, がん治療の副作用, バイオマーカー