Clear Sky Science · sv
Användning av en integrerad omikstillämpning för att avslöja mekanismerna bakom kemoterapi‑inducerad perifer neuropati (CIPN)
Varför cancerbehandling kan skada nerverna
Kemoterapi räddar liv, men för många kommer den till ett bekymmersamt pris: brännande känsla, stickningar eller domningar i händer och fötter som kan vara i månader eller år. Detta tillstånd, kallat kemoterapi‑inducerad perifer neuropati, kan göra det svårt att gå, sova och till och med knäppa en skjorta, och tvingar ibland läkare att sänka doser eller avbryta annars effektiva cancerläkemedel. Den granskade artikeln förklarar hur moderna ”omik”‑verktyg som skannar tusentals molekyler på en gång börjar avslöja vad som går fel i nerverna under behandlingen — och hur denna kunskap kan leda till tidigare varningssignaler och skonsammare, mer individualiserad cancervård.
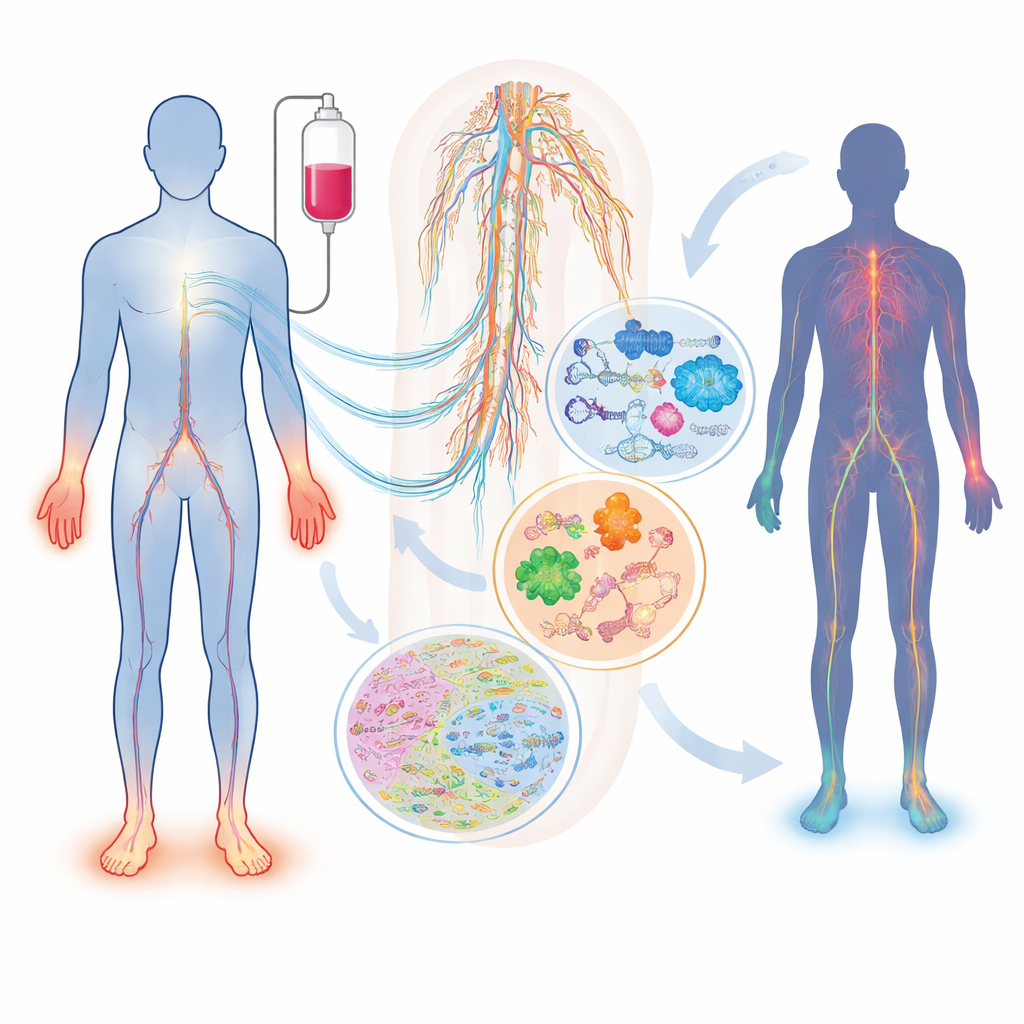
Vad som händer med nerverna under kemoterapi
Alla patienter som utsätts för samma läkemedel och dos utvecklar inte nervskador, och de som gör kan få mycket olika symtom. Översikten beskriver hur vanliga läkemedel — såsom taxaner (paklitaxel, docetaxel), platinumföreningar (cisplatin, oxaliplatin) och proteasomhämmare (bortezomib, karfilzomib) — kan skada sensoriska, motoriska och autonoma nerver på olika sätt. Faktorer som ålder, diabetes, vitaminbrist, njur‑ eller sköldkörtelproblem samt ärftliga skillnader i gener som styr läkemedelshantering eller nervstruktur påverkar individens risk. En enkel blodmarkör, neurofilament light chain, kan redan följa axonskada hos både djur och patienter, men på egen hand fångar den inte tillståndets fulla komplexitet eller förklarar varför det uppstår.
Hur omik ger en molekylär röntgenbild av skadade nerver
Författarna visar hur transkriptomik (RNA‑profilering), proteomik (storskalig proteinanalys) och metabolomik (systematisk studie av småmolekyler) var och en erbjuder en annan lins på nervskador. Modern single‑cell RNA‑sekvensering kan skilja många undertyper av sensoriska neuroner och stödjeceller i dorsalrotsganglierna — kluster av nervcellskroppar nära ryggraden — och följa hur varje typ svarar på olika kemoterapiläkemedel. Till exempel visar specifika beröringskänsliga fibrer starka genförändringar efter paklitaxel, och vissa gener kopplade till nervåldrande och senescens aktiveras efter cisplatin. Proteomik har avslöjat tidiga förändringar i proteiner som upprätthåller cellskelettet, energiproduktionen och stressreaktioner, ofta dagar innan djur visar beteenden kopplade till smärta. Metabolomik lyfter fram stora störningar i lipider, aminosyror och gallsyror, vilket pekar på problem med energianvändning, membranstabilitet och inflammation som kan skilja sig beroende på läkemedel, ålder och till och med tarmmikrober.
Att se var skadan sker i vävnaderna
Utöver att katalogisera vilka molekyler som förändras kan nyare ”rumsliga” masspektrometrimetoder visa exakt var i vävnaden dessa förändringar förekommer. Imaging mass cytometry och mass spectrometry imaging kartlägger proteiner, lipider, metaboliter och till och med kemoterapiföreningarna själva direkt på nervsnitt och ryggmärgssnitt, samtidigt som neuronernas, gliacellernas och omgivande vävnaders arkitektur bevaras. Tidiga studier har använt dessa verktyg för att lokalisera smärtrelaterade neuropeptider och för att kartlägga hur lipider förskjuts i precisa regioner efter nervskada. Man har också följt långvariga depositioner av platinum från oxaliplatin i huden, vilket tyder på att läkemedelsmolekyler som blir kvar i icke‑cancervävnader kan bidra till att upprätthålla kroniska symtom. Även om bara ett fåtal sådana studier har gjorts specifikt i kemoterapibehandlade nerver är tekniken redo att klargöra vilka celltyper och mikroregioner som drabbas först, hårdast och längst.
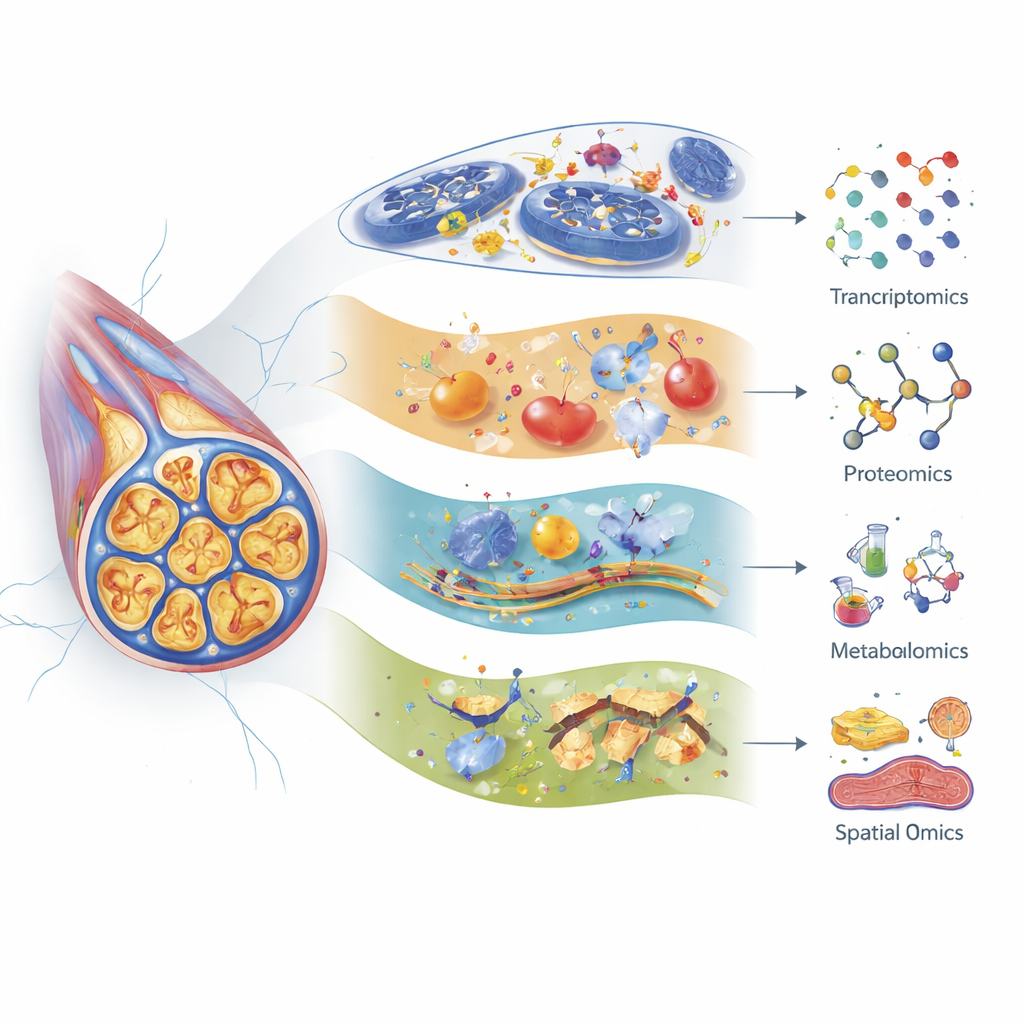
Att sätta ihop alla molekylära pusselbitarna
Ingen enskild typ av omik kan fullt ut förklara varför vissa patienter utvecklar svår neuropati och andra inte. Översikten förespråkar integrerade, flerskiktade angreppssätt som kombinerar genetisk variation, RNA‑förändringar, protein‑nätverk, metabolitförskjutningar, rumsliga kartor, nervfunktionstester och patientrapporterade symtom. Tidiga multi‑omikstudier länkar redan koordinerade förändringar i lipidsignalering, inflammatoriska vägar, mitokondriell stress och nervmodulerande system såsom endocannabinoider och opioidsignalering. Andra kopplar specifika lipidbudbärare och tarmderiverade gallsyror till smärta, vilket pekar på nya läkemedelsmål som sfingolipidreceptorer eller kemokinreceptorer som kan dämpa nervskada utan att försämra anticancereffekten. Stora, noggrant utformade studier på människor som anpassar laboratoriedata till kliniska mönster kommer att vara avgörande för att omvandla dessa insikter till praktiska verktyg.
Vad detta betyder för framtidens cancervård
För en lekmannaläsare är huvudbudskapet hoppfullt: genom att läsa de molekylära fingeravtryck som finns i blod, nervvävnad och till och med avföring börjar forskare förutsäga vem som löper störst risk för nervskada, förstå hur olika läkemedel skadar nervsystemet och identifiera svaga punkter i dessa vägar som kan skyddas. Författarna slår fast att integrerad omik, särskilt när den tillämpas på mänskliga prover över tid, så småningom kan vägleda läkare i valet av cancerläkemedel och doser som passar varje persons biologi, samtidigt som den pekar ut nya mediciner som skyddar nerverna från skada. Med tiden kan detta systemsynsätt göra det möjligt att behålla fördelarna med kraftfulla kemoterapier samtidigt som man kraftigt minskar långvarig smärta och funktionsnedsättning som så ofta följer.
Citering: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Nyckelord: kemoterapi‑inducerad perifer neuropati, multi‑omik, nervskada, biverkningar av cancerbehandling, biomarkörer