Clear Sky Science · pt
Usando uma abordagem ômica integrada para desvendar os mecanismos subjacentes à neuropatia periférica induzida por quimioterapia (NPIC)
Por que o tratamento do câncer pode prejudicar os nervos
A quimioterapia salva vidas, mas para muitas pessoas vem com um custo preocupante: queimação, formigamento ou dormência nas mãos e pés que podem durar meses ou anos. Essa condição, chamada neuropatia periférica induzida por quimioterapia, pode dificultar caminhar, dormir e até abotoar uma camisa, e às vezes obriga os médicos a reduzir ou interromper fármacos oncológicos que seriam eficazes. O artigo revisado explica como ferramentas ômicas de ponta, que vasculham milhares de moléculas de uma vez, estão começando a revelar o que dá errado nos nervos durante o tratamento — e como esse conhecimento pode levar a sinais de alerta mais precoces e a um cuidado oncológico mais suave e personalizado.
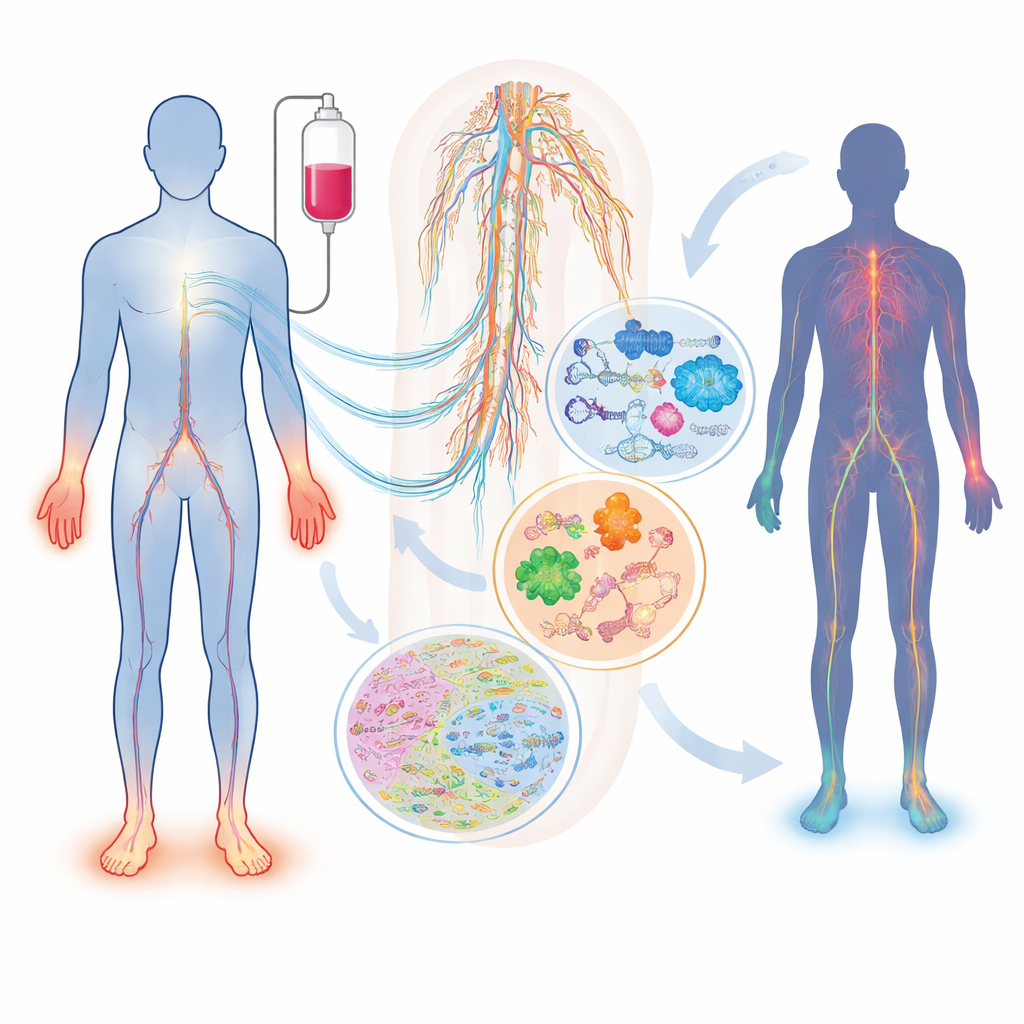
O que acontece aos nervos durante a quimioterapia
Nem todos os pacientes expostos ao mesmo medicamento e dose desenvolvem dano nervoso, e aqueles que desenvolvem podem apresentar sintomas muito diferentes. A revisão descreve como fármacos amplamente usados — como taxanos (paclitaxel, docetaxel), compostos de platina (cisplatina, oxaliplatina) e inibidores do proteassoma (bortezomibe, carfilzomibe) — podem lesar nervos sensoriais, motores e autonômicos de maneiras distintas. Fatores como idade, diabetes, carências vitamínicas, problemas renais ou da tireoide e diferenças hereditárias em genes que controlam o manejo do fármaco ou a estrutura nervosa alteram o risco individual. Um marcador sanguíneo simples, a cadeia leve de neurofilamento, já consegue acompanhar o dano axonal em animais e pacientes, mas isoladamente não captura a complexidade completa da condição nem explica por que ela se desenvolve.
Como as ômicas fornecem um raio‑X molecular dos nervos lesionados
Os autores mostram como transcriptômica (perfil de RNA), proteômica (análise em larga escala de proteínas) e metabolômica (estudo sistemático de pequenas moléculas) oferecem cada uma uma lente diferente sobre a lesão nervosa. O sequenciamento de RNA de célula única moderno pode distinguir muitos subtipos de neurônios sensoriais e células de suporte nos gânglios da raiz dorsal — aglomerados de corpos celulares nervosos próximos à coluna — e acompanhar como cada tipo responde a diferentes quimioterápicos. Por exemplo, fibras específicas sensíveis ao toque mostram fortes alterações gênicas após paclitaxel, e alguns genes ligados ao envelhecimento e senescência nervosa são ativados após cisplatina. A proteômica revelou mudanças precoces em proteínas que mantêm o esqueleto celular, as usinas de energia e as respostas ao estresse, frequentemente dias antes de os animais exibirem comportamentos de dor. A metabolômica destaca perturbações importantes em lipídios, aminoácidos e ácidos biliares, apontando problemas no uso de energia, estabilidade das membranas e inflamação que podem diferir conforme o fármaco, a idade e até os micróbios intestinais.
Ver onde o dano ocorre dentro dos tecidos
Além de catalogar quais moléculas mudam, métodos mais recentes de espectrometria de massa “espacial” podem mostrar exatamente onde, no tecido, essas mudanças ocorrem. Citometria por massa de imagem e imagiologia por espectrometria de massa mapeiam proteínas, lipídios, metabólitos e até os próprios compostos quimioterápicos diretamente em seções nervosas e fatias da medula espinhal, preservando a arquitetura de neurônios, células gliais e tecido circundante. Trabalhos iniciais usaram essas ferramentas para localizar neuropeptídeos relacionados à dor e traçar como os lipídios mudam em regiões precisas após a lesão nervosa. Também rastrearam depósitos duradouros de platina da oxaliplatina na pele, sugerindo que moléculas de fármaco que persistem em tecidos não cancerosos podem ajudar a sustentar sintomas crônicos. Embora apenas alguns desses estudos tenham sido feitos especificamente em nervos tratados com quimioterapia, a tecnologia está pronta para esclarecer quais tipos celulares e micro‑regiões são atingidos primeiro, com mais intensidade e por mais tempo.
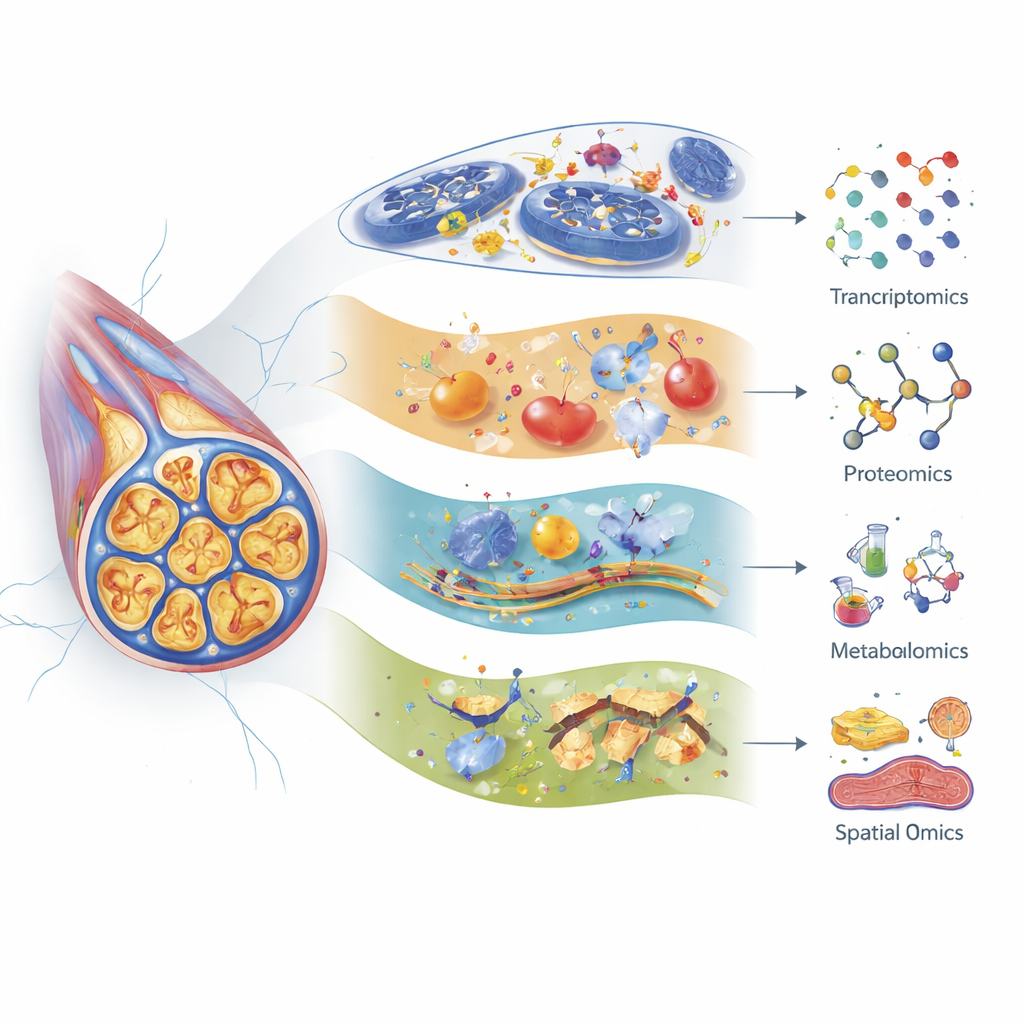
Juntando todas as peças moleculares
Nenhum tipo isolado de ômica pode explicar totalmente por que alguns pacientes desenvolvem neuropatia severa e outros não. A revisão defende abordagens integradas e multi‑camada que combinem variação genética, alterações de RNA, redes proteicas, mudanças de metabólitos, mapas espaciais, testes de função nervosa e sintomas relatados pelos pacientes. Estudos multi‑ômicos iniciais já vinculam mudanças coordenadas em sinalização lipídica, vias inflamatórias, estresse mitocondrial e sistemas que modulam o nervo, como endocanabinoides e sinalização opioide. Outros associam mensageiros lipídicos específicos e ácidos biliares derivados do intestino à dor, sugerindo novos alvos farmacológicos como receptores de esfingolipídios ou receptores de quimiocinas que poderiam atenuar a lesão nervosa sem enfraquecer os efeitos anticâncer. Estudos humanos grandes e cuidadosamente desenhados, que alinhem dados laboratoriais a padrões clínicos, serão cruciais para transformar esses insights em ferramentas práticas.
O que isso significa para o cuidado do câncer no futuro
Para um leitor leigo, a mensagem central é otimista: ao ler as impressões digitais moleculares deixadas no sangue, no tecido nervoso e até nas fezes, os cientistas estão começando a prever quem tem maior risco de dano nervoso, entender como diferentes fármacos lesionam o sistema nervoso e identificar pontos fracos nessas vias que podem ser protegidos. Os autores concluem que as ômicas integradas, especialmente quando aplicadas a amostras humanas ao longo do tempo, poderiam eventualmente orientar os médicos na escolha de medicamentos e doses que se ajustem à biologia de cada pessoa, ao mesmo tempo em que apontam novos medicamentos que protejam os nervos do dano. Com o tempo, essa visão em nível de sistema pode tornar possível manter os benefícios de quimioterapias poderosas reduzindo drasticamente a dor e a incapacidade duradouras que tantas vezes se seguem.
Citação: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Palavras-chave: neuropatia periférica induzida por quimioterapia, multi-ômica, dano nervoso, efeitos colaterais do tratamento do câncer, biomarcadores