Clear Sky Science · ar
استخدام نهج أوميكس متكامل لكشف الآليات الكامنة وراء الاعتلال العصبي الطرفي الناجم عن العلاج الكيميائي (CIPN)
لماذا يمكن أن يضر علاج السرطان بالأعصاب
العلاج الكيميائي ينقذ الأرواح، لكنه بالنسبة لكثيرين له ثمن مزعج: إحساس بالحرقان أو الوخز أو الخدر في اليدين والقدمين يمكن أن يستمر لأشهر أو سنوات. هذه الحالة، المسماة الاعتلال العصبي الطرفي الناجم عن العلاج الكيميائي، قد تجعل المشي والنوم وحتى غلق الأزرار أمورًا صعبة، وأحيانًا تضطر الأطباء إلى تخفيض جرعات أدوية فعالة أو إيقافها. تشرح المراجعة كيف أن أدوات «الأوميكس» المتطورة التي تفحص آلاف الجزيئات مرة واحدة بدأت تكشف ما الذي يخطئ في الأعصاب أثناء العلاج—وكيف يمكن أن يؤدي ذلك إلى علامات تحذير مبكرة ورعاية أوروبية ألطف وأكثر تخصيصًا للمرضى.
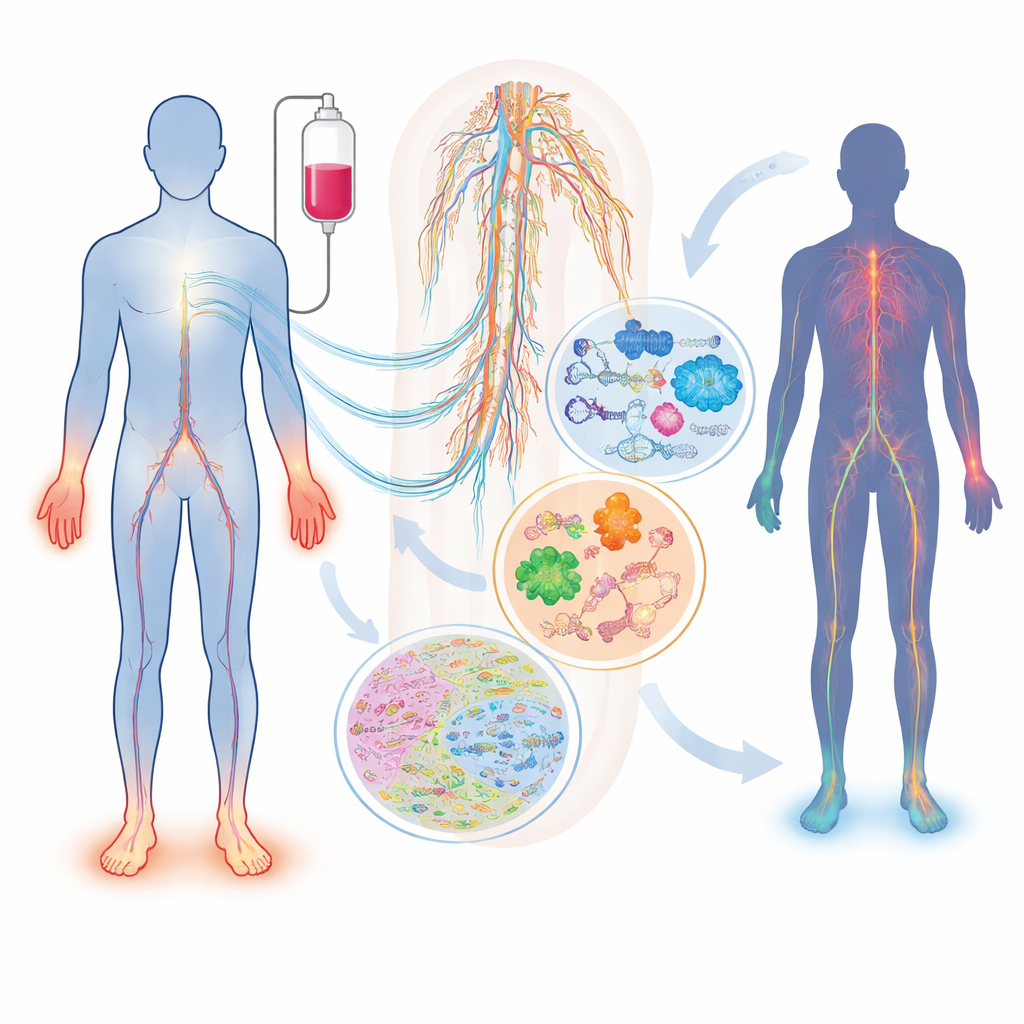
ماذا يحدث للأعصاب أثناء العلاج الكيميائي
ليس كل المرضى المعرضين لنفس الدواء والجرعة يصابون بتلف أعصاب، والذين يصابون قد يعانون أعراضًا مختلفة تمامًا. تصف المراجعة كيف يمكن لأدوية مستخدمة على نطاق واسع—مثل التاكسانات (باكليتاكسيل، دوستاكسل)، ومركبات الفلزات الثقيلة (سيسبلاتين، أوكساليبلاتين)، ومثبطات البروتيازوم (بورتيزوميب، كارفيليزوميب)—أن تلحق الضرر بالأعصاب الحسية والحركية والمستقلة بطرق مميزة. عوامل مثل العمر، والسكري، ونقص الفيتامينات، ومشكلات الكلى أو الغدة الدرقية، والاختلافات الموروثة في جينات تتحكم في معالجة الدواء أو بنية العصب كلها تؤثر في مخاطر الفرد. علامة دم بسيطة واحدة، سلسلة الخيوط العصبية الخفيفة (neurofilament light chain)، تستطيع تتبُّع تلف المحاور العصبية في الحيوانات والمرضى، لكن وحدها لا تلتقط التعقيد الكامل للحالة أو تشرح لماذا تتطور من الأساس.
كيف تقدم الأوميكس صورة جزيئية للأعصاب المصابة
يوضح المؤلفون كيف أن النسخياتية (تحليل الرنا)، والبروتيوميات (تحليل البروتينات على نطاق واسع)، والميتوبولوميات (دراسة منهجية للجزيئات الصغيرة) كل منها يقدم عدسة مختلفة لإصابة الأعصاب. تقرأ تقنيات تحديد تسلسل الرنا على مستوى الخلية الواحدة أنواعًا فرعية عديدة من الخلايا العصبية الحسية والخلايا الداعمة في عقد الجذور الظهرية—تجمعات لأجسام الخلايا العصبية قرب العمود الفقري—وتتبع كيف يستجيب كل نوع لأنواع مختلفة من أدوية العلاج الكيميائي. على سبيل المثال، تُظهر ألياف حساسة لللمس تغييرات جينية قوية بعد الباكليتاكسيل، وتُفعّل بعض الجينات المرتبطة شيخوخة الأعصاب والشيخوخة الخلوية بعد السيسبلاتين. كشفت البروتيوميات عن تحولات مبكرة في البروتينات التي تحافظ على هيكل الخلية ومصانع الطاقة واستجابات الإجهاد، غالبًا قبل أيام من ظهور سلوكيات الألم في الحيوانات. وتسجل الميتابولوميات اضطرابات كبيرة في الدهون والأحماض الأمينية والأحماض الصفراوية، مما يشير إلى مشاكل في استخدام الطاقة، وثبات الأغشية، والالتهاب التي قد تختلف بحسب الدواء والعمر وحتى ميكروبات الأمعاء.
رؤية مكان حدوث الضرر داخل الأنسجة
إلى ما وراء جرد الجزيئات المتغيرة، تستطيع طرق الطيف الكتلي «المكانية» الأحدث إظهار المكان الدقيق داخل النسيج الذي تحدث فيه تلك التغيرات. تقوم مطيافية الكتلة التصويرية المناعية وتصوير مطيافية الكتلة برسم خرائط للبروتينات والدهون والمواد الأيضية وحتى مركبات العلاج الكيميائي نفسها مباشرة على مقاطع الأعصاب وشرائح النخاع الشوكي، محافظَةً على بنية الخلايا العصبية والخلايا الدبقية والنسيج المحيط. استخدمت أعمال مبكرة هذه الأدوات لتحديد مواضع الببتيدات العصبية المرتبطة بالألم ولرسم كيف تتحرك الدهون في مناطق دقيقة بعد إصابة العصب. كما تتبعت رواسبًا طويلة الأمد من البلاتين الناتج عن الأوكساليبلاتين في الجلد، مما يوحي بأن جزيئات الدواء التي تظل في الأنسجة غير السرطانية قد تساهم في استمرار الأعراض المزمنة. على الرغم من أن عددًا قليلاً فقط من هذه الدراسات أُجرِيَت خصيصًا على الأعصاب المعالجة بالعلاج الكيميائي، فإن التقنية مؤهلة لتوضيح أي أنواع الخلايا والمناطق الدقيقة تتعرض للضرب أولًا وبشدة وبمدة أطول.
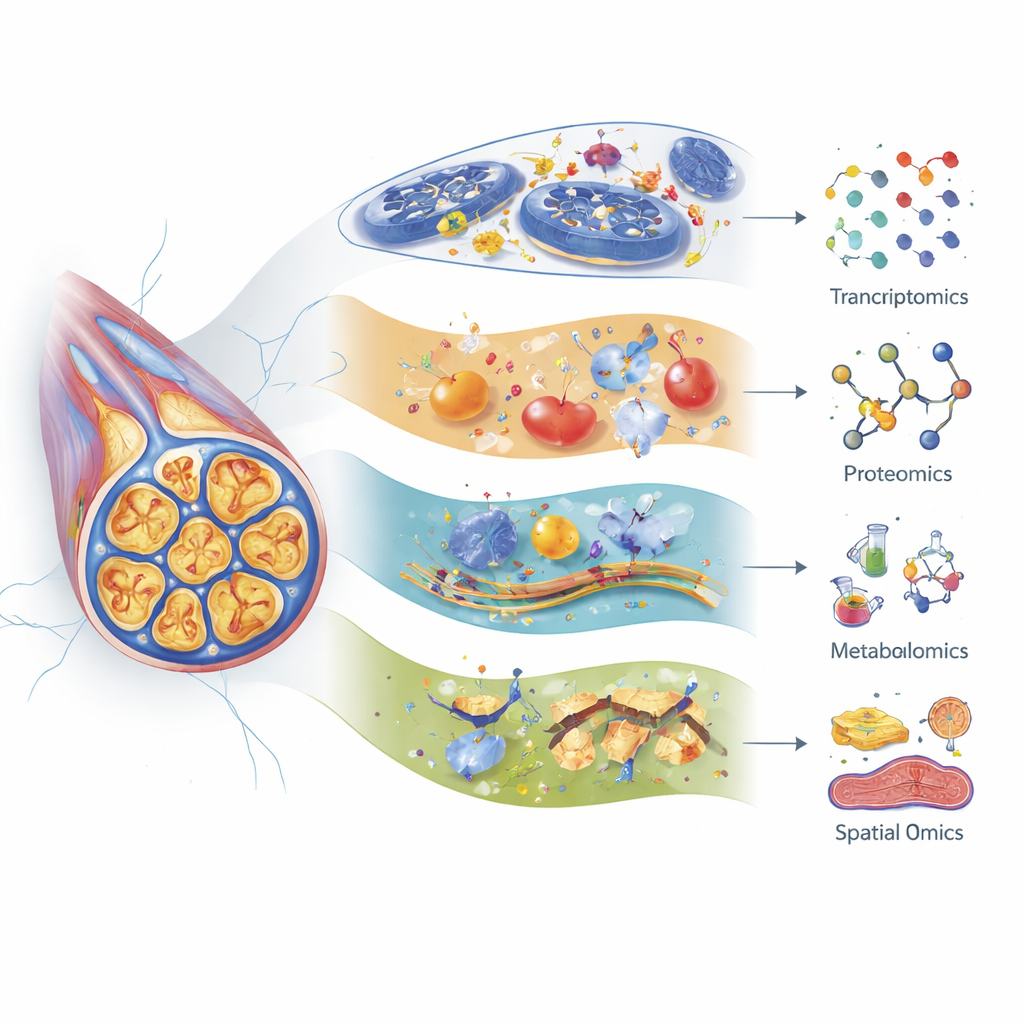
جمع كل الأجزاء الجزيئية معًا
لا يستطيع نوع واحد من الأوميكس وحده تفسير لماذا يطوّر بعض المرضى اعتلالًا عصبيًا شديدًا بينما لا يصاب آخرون. تدافع المراجعة عن نهج متكامل متعدد الطبقات يجمع التغايرات الجينية، وتغيرات الرنا، وشبكات البروتينات، وتحولات المستقلبات، والخرائط المكانية، واختبارات وظيفة الأعصاب، والأعراض المبلغ عنها من المرضى. تربط دراسات متعددة الأوميكس المبكرة بالفعل تغيرات منسقة في إشارات الدهون، ومسارات الالتهاب، وإجهاد الميتوكوندريا، وأنظمة تعديل الأعصاب مثل الإندوكينابينويديات وإشارات الأفيون. تربط دراسات أخرى مراسلات دهنية محددة وأحماض صفراوية مشتقة من الأمعاء بالألم، ما يقترح أهدافًا دوائية جديدة مثل مستقبلات السفينغوليبيد أو مستقبلات الكيموكين التي قد تخفف إصابة الأعصاب دون إضعاف التأثيرات المضادة للسرطان. ستكون الدراسات البشرية الكبيرة والمصممة بعناية التي توائم بيانات المختبر مع الأنماط السريرية حاسمة لتحويل هذه الرؤى إلى أدوات عملية.
ماذا يعني هذا لرعاية السرطان في المستقبل
بالنسبة للقارئ العام، الرسالة المركزية متفائلة: بقراءة البصمات الجزيئية المتروكة في الدم ونسيج الأعصاب وحتى البراز، بدأ العلماء يتنبأون بمن هم الأكثر عرضة لخطر تلف الأعصاب، ويفهمون كيف تضر الأدوية المختلفة الجهاز العصبي، ويحددون نقاط ضعف في تلك المسارات يمكن حمايتها. يستنتج المؤلفون أن الأوميكس المتكامل، وخاصة عند تطبيقه على عينات بشرية عبر الزمن، قد يوجه الأطباء في نهاية المطاف لاختيار أدوية السرطان والجرعات التي تتناسب مع بيولوجيا كل شخص، وفي الوقت نفسه يشير إلى أدوية جديدة تحمي الأعصاب من الضرر. مع الزمن، قد يجعل هذا المنظور على مستوى النظم من الممكن الاحتفاظ بفوائد العلاجات الكيميائية القوية مع تقليل الألم والعجز طويلي الأمد اللذين يتبعيانها في كثير من الأحيان.
الاستشهاد: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
الكلمات المفتاحية: الاعتلال العصبي الطرفي الناجم عن العلاج الكيميائي, تعدد الأوميكس, تلف الأعصاب, آثار جانبية لعلاج السرطان, مؤشرات حيوية