Clear Sky Science · de
Mit einem integrierten Omics‑Ansatz die Mechanismen der chemotherapieinduzierten peripheren Neuropathie (CIPN) aufdecken
Warum Krebstherapie den Nerven schaden kann
Chemotherapie rettet Leben, bringt für viele Betroffene aber einen belastenden Preis mit sich: Brennen, Kribbeln oder Taubheitsgefühle in Händen und Füßen, die Monate oder Jahre anhalten können. Diese Erkrankung, chemotherapieinduzierte periphere Neuropathie genannt, erschwert Gehen, Schlafen oder sogar das Knöpfen eines Hemdes und zwingt mitunter Ärztinnen und Ärzte, sonst wirksame Krebsmedikamente zu reduzieren oder abzusetzen. Der rezensierte Artikel erläutert, wie moderne „Omics“-Werkzeuge, die Tausende von Molekülen gleichzeitig erfassen, anfangen zu zeigen, was in Nerven während der Behandlung schiefläuft – und wie dieses Wissen zu früheren Warnzeichen und schonenderer, individuellerer Krebstherapie führen könnte.
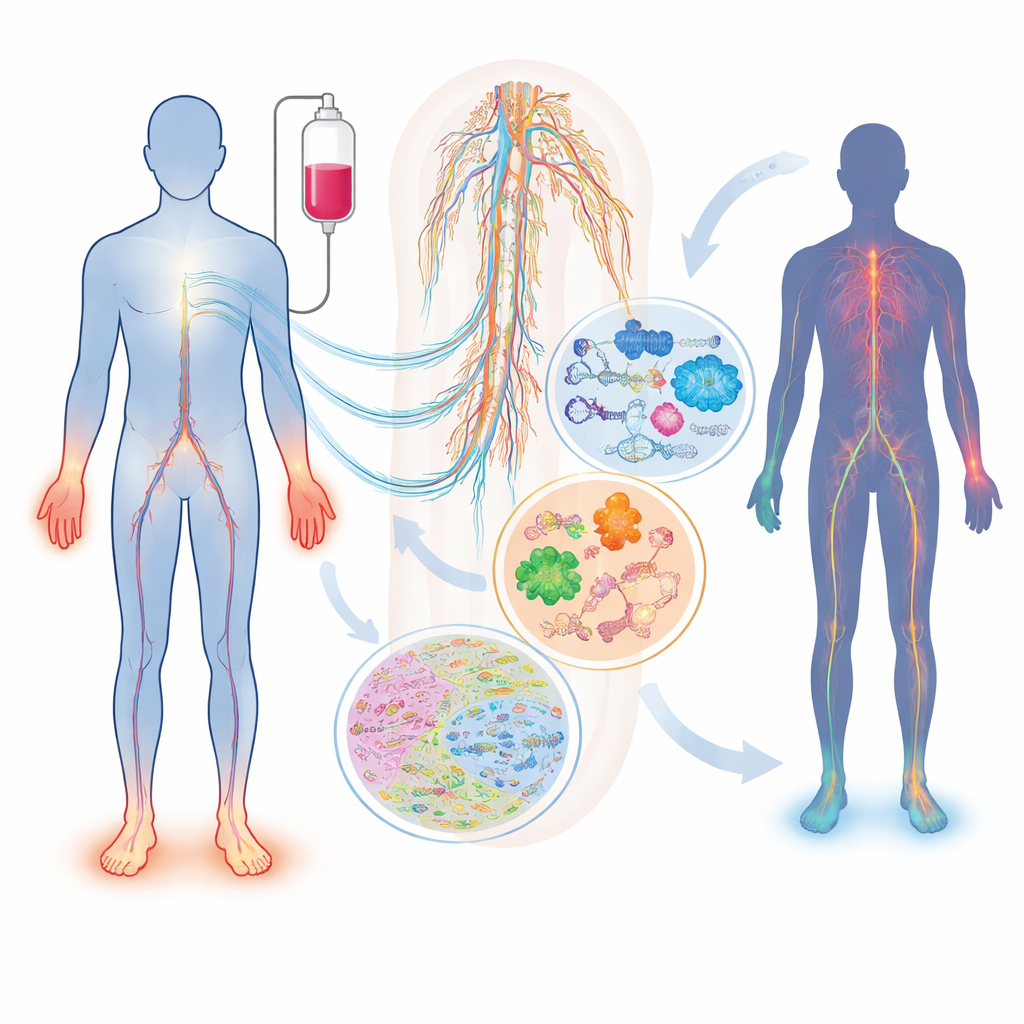
Was mit Nerven während der Chemotherapie passiert
Nicht alle Patienten, die demselben Medikament und derselben Dosis ausgesetzt sind, entwickeln Nervenschäden, und diejenigen, die es tun, können sehr unterschiedliche Symptome haben. Die Übersichtsarbeit beschreibt, wie weitverbreitete Medikamente – etwa Taxane (Paclitaxel, Docetaxel), Platinverbindungen (Cisplatin, Oxaliplatin) und Proteasom‑Inhibitoren (Bortezomib, Carfilzomib) – sensorische, motorische und autonome Nerven auf unterschiedliche Weise schädigen können. Faktoren wie Alter, Diabetes, Vitaminmangel, Nieren‑ oder Schilddrüsenprobleme sowie vererbte Unterschiede in Genen, die den Arzneimittelstoffwechsel oder die Nervenstruktur steuern, verändern das individuelle Risiko. Ein einfacher Blutmarker, die neurofilament light chain, kann bereits axonale Schäden bei Tieren und Patienten nachverfolgen, erfasst aber allein nicht die gesamte Komplexität der Erkrankung und erklärt nicht, warum sie entsteht.
Wie Omics ein molekulares Röntgenbild verletzter Nerven liefern
Die Autorinnen und Autoren zeigen, wie Transkriptomik (RNA‑Profiling), Proteomik (groß angelegte Proteinanalysen) und Metabolomik (systematische Untersuchung kleiner Moleküle) jeweils eine andere Perspektive auf Nervenschäden bieten. Moderne Einzelzell‑RNA‑Sequenzierung kann viele Subtypen sensorischer Neurone und unterstützender Zellen in den Spinalganglien – Ansammlungen von Nervenzellkörpern nahe der Wirbelsäule – unterscheiden und nachverfolgen, wie jeder Typ auf verschiedene Chemotherapeutika reagiert. So zeigen beispielsweise spezifische berührungssensitive Fasern nach Paclitaxel starke Genveränderungen, und nach Cisplatin werden einige Gene aktiviert, die mit Nervaltersprozessen und Seneszenz in Verbindung stehen. Die Proteomik hat frühe Verschiebungen in Proteinen offenbart, die das Zellskelett, Energieproduktionssysteme und Stressantworten erhalten – oft Tage bevor Tiere Schmerzverhalten zeigen. Metabolomik hebt große Störungen bei Lipiden, Aminosäuren und Gallensäuren hervor und deutet auf Probleme mit Energieversorgung, Membranstabilität und Entzündung hin, die je nach Wirkstoff, Alter und sogar Darmmikrobiom unterschiedlich ausfallen können.
Sehen, wo in Geweben Schäden auftreten
Über die bloße Auflistung veränderter Moleküle hinaus können neuere „räumliche“ Massenspektrometrie‑Methoden genau zeigen, wo im Gewebe diese Veränderungen vorkommen. Imaging‑Mass‑Cytometry und Massenspektrometrie‑Imaging kartieren Proteine, Lipide, Metabolite und sogar die Chemotherapie‑Verbindungen selbst direkt auf Nerven‑ und Rückenmarkschnitten und bewahren dabei die Architektur von Neuronen, Gliazellen und umgebendem Gewebe. Erste Arbeiten haben diese Werkzeuge genutzt, um schmerzbezogene Neuropeptide zu lokalisieren und darzustellen, wie Lipide sich nach Nervenschädigung in bestimmten Regionen verändern. Sie haben auch langanhaltende Ablagerungen von Platin aus Oxaliplatin in der Haut nachverfolgt, was darauf hindeutet, dass in Nicht‑Tumorgeweben verbleibende Wirkstoffmoleküle chronische Symptome aufrechterhalten könnten. Obwohl bislang nur wenige solcher Studien speziell an durch Chemotherapie behandelten Nerven durchgeführt wurden, ist die Technologie gut positioniert, um zu klären, welche Zelltypen und Mikroregionen zuerst, am stärksten und am längsten betroffen sind.
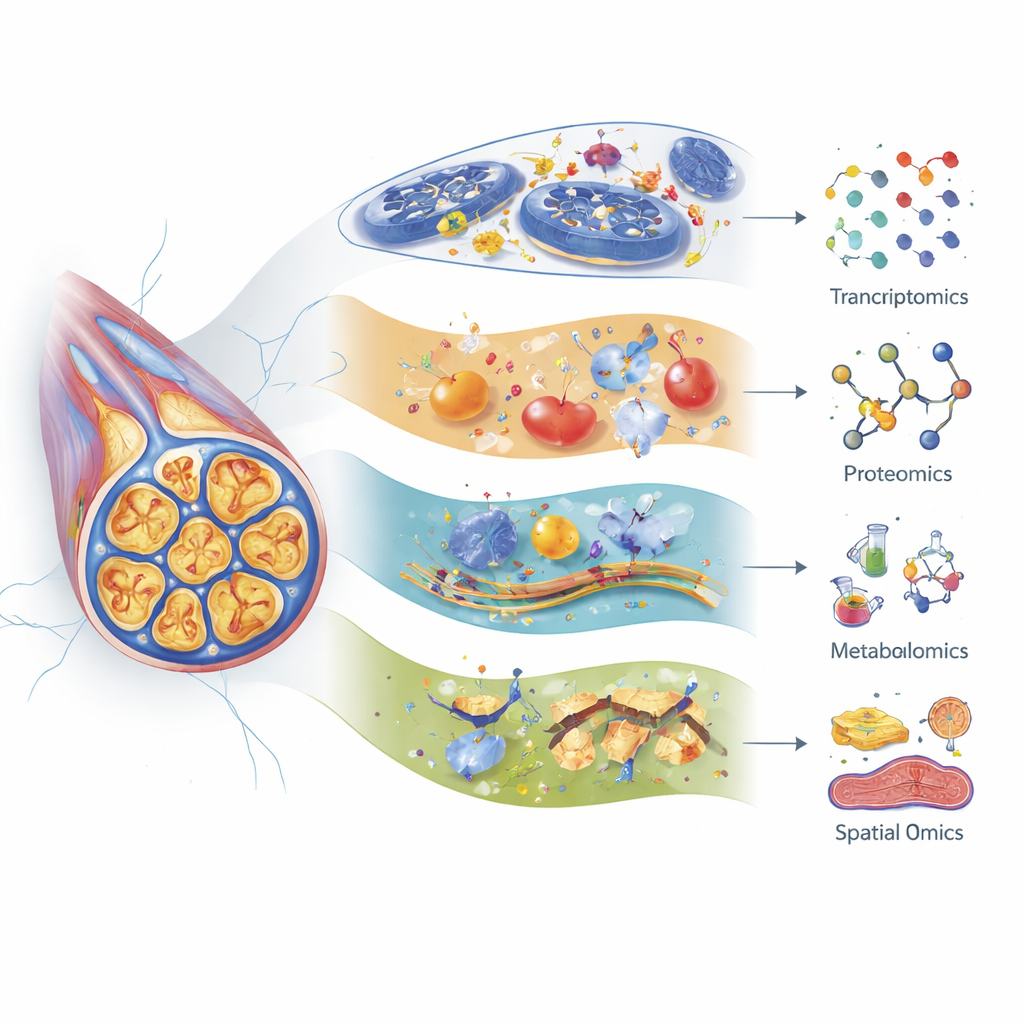
Die molekularen Puzzleteile zusammenfügen
Kein einzelner Omics‑Ansatz kann vollständig erklären, warum manche Patientinnen und Patienten starke Neuropathien entwickeln und andere nicht. Die Übersichtsarbeit plädiert für integrierte, mehrschichtige Ansätze, die genetische Variation, RNA‑Veränderungen, Proteinnetzwerke, Metabolitverschiebungen, räumliche Karten, Nervenfunktionsprüfungen und patientenberichtete Symptome kombinieren. Frühere Multi‑Omics‑Studien verbinden bereits koordinierte Veränderungen in Lipidsignalwegen, Entzündungswegen, mitochondrialem Stress und nervenmodulierenden Systemen wie Endocannabinoiden und Opioidsignalgebung. Andere knüpfen spezifische Lipidbotenstoffe und im Darm gebildete Gallensäuren an Schmerzen und schlagen damit neue Wirkstoffziele wie Sphingolipid‑Rezeptoren oder Chemokinrezeptoren vor, die Nervenschäden abschwächen könnten, ohne die krebsbekämpfende Wirkung zu vermindern. Große, sorgfältig konzipierte Humanstudien, die Laborbefunde mit klinischen Mustern in Einklang bringen, werden entscheidend sein, um diese Erkenntnisse in praktische Werkzeuge zu überführen.
Was das für die künftige Krebsversorgung bedeutet
Für eine allgemein interessierte Leserschaft ist die Kernbotschaft hoffnungsvoll: Indem sie die molekularen Fingerabdrücke in Blut, Nervengewebe und sogar Stuhl lesen, beginnen Forschende vorherzusagen, wer besonders gefährdet ist, Nervenschäden zu entwickeln, zu verstehen, wie verschiedene Medikamente das Nervensystem schädigen, und Schwachstellen in diesen Wegen zu identifizieren, die geschützt werden könnten. Die Autorinnen und Autoren schließen, dass integrierte Omics, vor allem wenn sie an menschlichen Proben über die Zeit angewandt werden, Ärztinnen und Ärzten letztlich helfen könnten, Krebsmedikamente und Dosierungen an die Biologie jedes Menschen anzupassen und gleichzeitig neue Mittel aufzuzeigen, die Nerven vor Schäden bewahren. Auf lange Sicht könnte diese systemische Sichtweise ermöglichen, die Vorteile leistungsstarker Chemotherapien zu erhalten und zugleich die langanhaltenden Schmerzen und Behinderungen, die so häufig folgen, deutlich zu verringern.
Zitation: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Schlüsselwörter: chemotherapieinduzierte periphere Neuropathie, Multi‑Omics, Nervenschädigung, Nebenwirkungen von Krebstherapien, Biomarker