Clear Sky Science · he
שימוש בגישה אומיקס משולבת לחשיפת המנגנונים שעומדים בבסיס נוירופתיה היקפית עקב כימותרפיה (CIPN)
מדוע טיפול בסרטן יכול לפגוע בעצבים
כימותרפיה מצילה חיים, אך אצל רבים היא נושאת עלות מטרידה: צריבה, עיקצוץ או חוסר תחושה בידיים וברגליים שיכולים להימשך חודשים או שנים. מצב זה, המכונה נוירופתיה היקפית הנגרמת על ידי כימותרפיה, יכול להקשות על הליכה, שינה ואפילו כפתור חולצה, ובמקרים מסוימים מאלץ רופאים להפחית או להפסיק תרופות סרטניות שבאופן אחר היו יעילות. המאמר הסקרי מסביר כיצד כלי "אומיקס" מתקדמים הסורקים אלפי מולקולות בבת אחת מתחילים לחשוף מה משתבש בעצבים במהלך הטיפול — וכיצד הידע הזה יכול להוביל לאיתותים מוקדמים ולטיפול בסרטן עדין ומותאם אישית יותר.
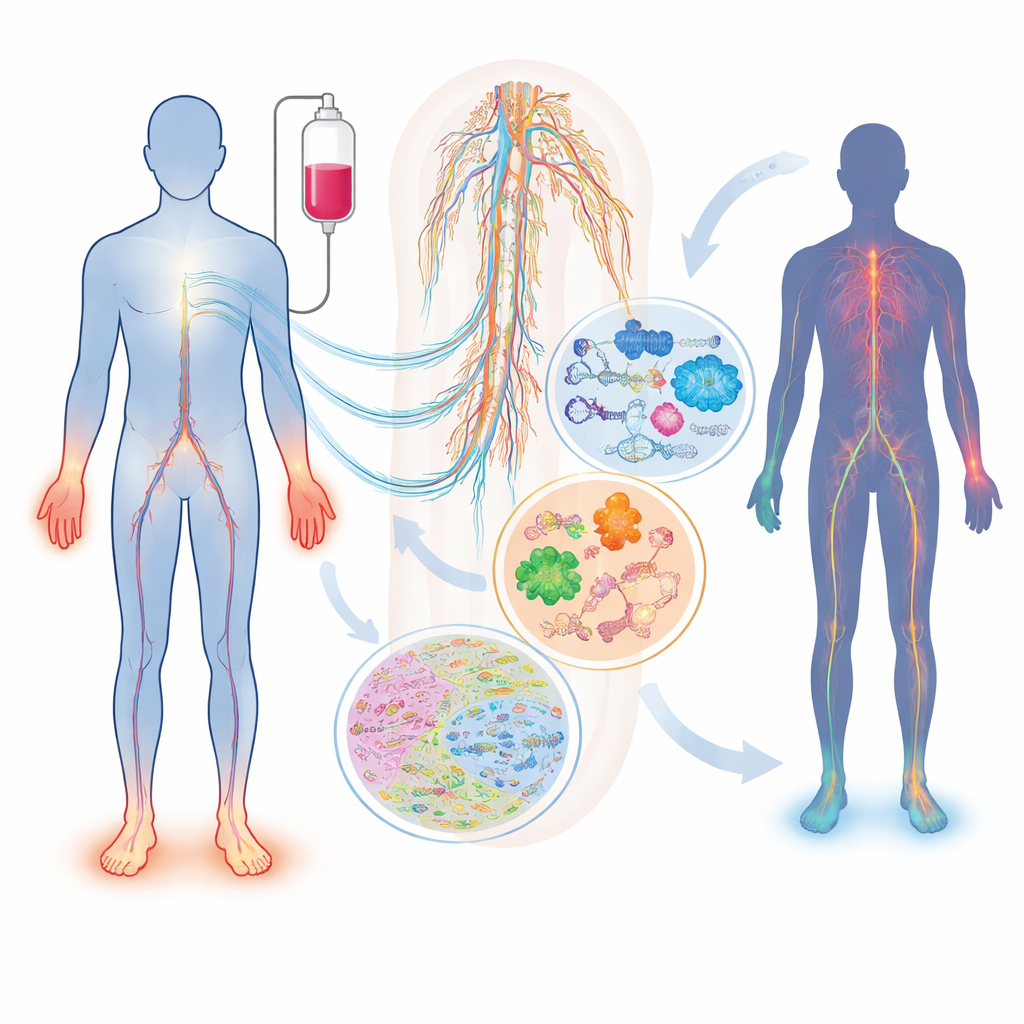
מה קורה לעצבים במהלך כימותרפיה
לא כל המטופלים החשופים לאותה תרופה ומינון מפתחים נזק עצבי, ובין אלה שכן חווים תסמינים שונים במידה רבה. הסקירה מתארת כיצד תרופות נפוצות — כגון טקסנים (פאסלטקסל, דוקטקסל), תרכובות פלסטינה (ציספלטין, אוקסליפלטין) וחוסמי פרוטאוזום (בורטזומיב, קארפילזומיב) — יכולות לפגוע בעצבים סנסוריים, מוטוריים ואוטונומיים בדרכים שונות. גורמים כמו גיל, סוכרת, חסרים בוויטמינים, בעיות בכליה או בתירואיד, ושינויים תורשתיים בגנים האחראים על מטען התרופה או על מבנה העצב משפיעים כולם על הסיכון האישי. סימן דם פשוט אחד, שרשרת נוירופילמנט קלה, כבר יכול לעקוב אחרי נזק אקסונלי בבעלי חיים ובמטופלים, אך לבדו הוא אינו מסוגל ללכוד את העומק המורכב של המצב או להסביר מדוע הוא מתפתח מלכתחילה.
כיצד אומיקס מעניקים צילום רנטגן מולקולרי של עצבים פגועים
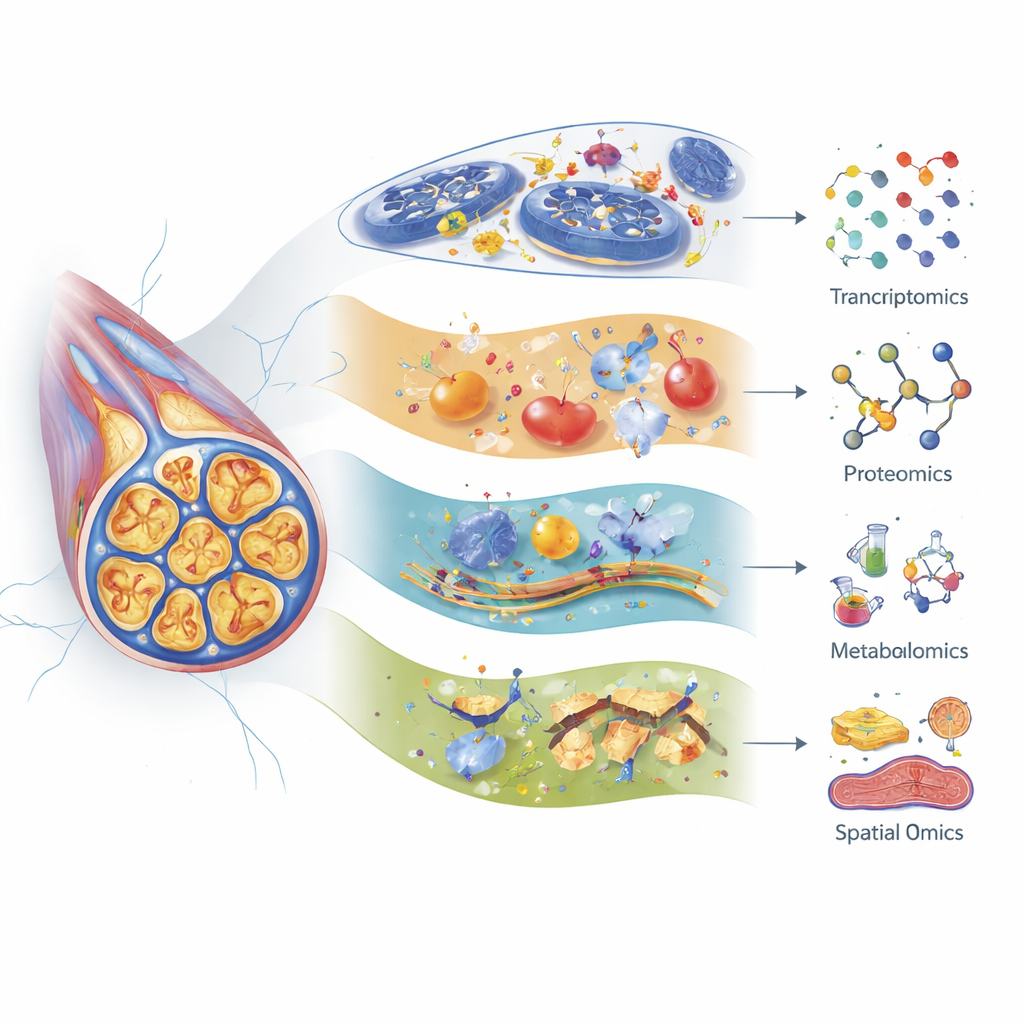
המחברים מראים כיצד טרנסקריפטומיקה (פרופיל ה-RNA), פרוטאומיקה (ניתוח חלבונים בקנה מידה גדול) ומתבולומיקה (חקר שיטתי של מולקולות קטנות) כל אחת מציעה עדשה שונה לפגיעה עצבית. רצף RNA בתא יחיד מודרני יכול להבחין בין תת-סוגים רבים של תאי חישה ותאי תמיכה בגרעיני שורש גבי — קבוצות של גופי תאים עצביים בקרבת עמוד השדרה — ולעקוב כיצד כל סוג מגיב לתרופות כימותרפיות שונות. למשל, סיבים רגישים למגע מראים שינויים גנטיים חזקים לאחר פקסליטקסל, וחלק מהגנים המקושרים להזדקנות עצבית וסנֶסֶנְס מועלים לאחר ציספלטין. פרוטאומיקה חשפה הזזות מוקדמות בחלבונים השומרים על שלד התא, על תחנות האנרגיה ועל תגובות ללחץ, לעתים ימים לפני שבעלי החיים מראים התנהגות של כאב. מתבולומיקה מדגישה הפרעות משמעותיות בשומנים, בחומצות אמינו ובחומצות מרה, ומצביעה על בעיות בשימוש באנרגיה, ביציבות הממברנה ובהיווצרות דלקת — שיכולות להשתנות לפי תרופה, גיל ואפילו מיקרוביוטת המעי.
לראות היכן הנזק מתרחש ברקמות
מעבר לרישום אילו מולקולות משתנות, שיטות חדשות של ספקטרומטריית מסה "מרחבית" יכולות להראות בדיוק באיזו נקודה ברקמה מתרחשות השינויים הללו. דימות מסה ציטומטרי ודימות בספקטרומטריית מסה ממפים חלבונים, שומנים, מטבוליטים ואפילו את תרופות הכימותרפיה עצמן ישירות על פרוסות של עצב וחוט השדרה, ושומרים על הארכיטקטורה של נוירונים, תאי גליה והרקמה הסובבת. עבודות מוקדמות השתמשו בכלים אלה כדי למקם נוירופפטידים הקשורים לכאב ולמפות כיצד שומנים משתנים באזורים מדויקים לאחר פגיעה עצבית. הם גם עקבו אחרי משקעים מתמשכים של פלטינה מאוקסליפלטין בעור, מה שמרמז כי מולקולות תרופה הנצברות ברקמות שאינן סרטניות עשויות לתרום לשימור התסמינים הכרוניים. למרות שרק מספר מועט של מחקרים כאלה נעשו ספציפית בעיצבים שטופלו בכימותרפיה, הטכנולוגיה נמצאת בעמדה להבהיר אילו סוגי תאים ותת-אזורים נפגעים ראשונים, בעוצמה הגדולה ביותר ובאורך זמן הארוך ביותר.
לרקום יחד את כל החלקים המולקולריים
אין סוג אומיקס יחיד שמסביר עד תום מדוע חלק מהמטופלים מפתחים נוירופתיה חמורה ואחרים לא. הסקירה טוענת לטובת גישות משולבות רב-שכבתיות שמחברות וריאציה גנטית, שינויים ב-RNA, רשתות חלבונים, הזזות מטבוליטים, מפות מרחביות, בדיקות תפקוד עצבי ודיווחים של מטופלים על תסמינים. מחקרים מרובי-אומיקס ראשוניים כבר מקשרים שינויים מתואמים באיתות שומנים, במסלולי דלקת, בלחץ מיטוכונדריאלי ובמערכות שמווסתות עצב כגון אנדוקנבינואידים ואיתות אופיאטי. אחרים מקשרים שליחי שומן ספציפיים וחומצות מרה שמקורן במעי לכאב, ומציעים יעדי תרופות חדשים כמו קולטי ספינגוליפידים או קולטי כימוקינים שיכולים להחליש פגיעה עצבית מבלי להחליש את השפעות נגד הסרטן. מחקרים אנושיים גדולים ומתוכננים בקפידה שיתאימו נתוני מעבדה לדפוסים קליניים יהיו קריטיים להפיכת התובנות הללו לכלים פרקטיים.
מה משמעות הדבר עבור טיפול בסרטן בעתיד
לקורא שאינו מומחה, המסר המרכזי הוא אופטימי: על ידי קריאת טביעות האצבע המולקולריות שמושארות בדם, ברקמת העצב ואפילו בצואה, המדענים מתחילים לחזות מי בסיכון הגבוה ביותר לנזק עצבי, להבין כיצד תרופות שונות פוגעות במערכת העצבים, ולזהות נקודות תורפה בדרך שניתן להגן עליהן. המחברים מסכמים כי אומיקס משולב, במיוחד כאשר מוחל על דגימות אנושיות לאורך זמן, עשוי בסופו של דבר להנחות רופאים בבחירת תרופות ומינונים המתאימים לביולוגיה האישית של כל מטופל, ובמקביל להצביע על תרופות חדשות המגינות על העצבים מפני נזק. עם הזמן, ראייה במערכות רחבת היקף זו עשויה לאפשר לשמור על יתרונות הכימותרפיות החזקות תוך צמצום משמעותי של הכאב והתשישות המתמשכת שלעיתים קרובות עוקבים אחריהן.
ציטוט: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
מילות מפתח: נוירופתיה היקפית הנגרמת על ידי כימותרפיה, מולטי-אומיקס, נזק לעצבים, תופעות לוואי של טיפול בסרטן, סמנים ביולוגיים