Clear Sky Science · fr
Utiliser une approche omique intégrée pour découvrir les mécanismes sous‑jacents à la neuropathie périphérique induite par la chimiothérapie (NPIC)
Pourquoi le traitement du cancer peut endommager les nerfs
La chimiothérapie sauve des vies, mais pour beaucoup elle a un prix troublant : des sensations de brûlure, des picotements ou un engourdissement des mains et des pieds qui peuvent durer des mois, voire des années. Cette affection, appelée neuropathie périphérique induite par la chimiothérapie, peut rendre la marche, le sommeil et même le fait de boutonner une chemise difficiles, et contraindre parfois les médecins à réduire ou interrompre des médicaments anticancéreux pourtant efficaces. L’article de synthèse explique comment les outils omiques de pointe, capables d’analyser des milliers de molécules à la fois, commencent à révéler ce qui dysfonctionne dans les nerfs pendant le traitement — et comment ces connaissances pourraient permettre des signes d’alerte plus précoces et des soins anticancéreux plus doux et personnalisés.
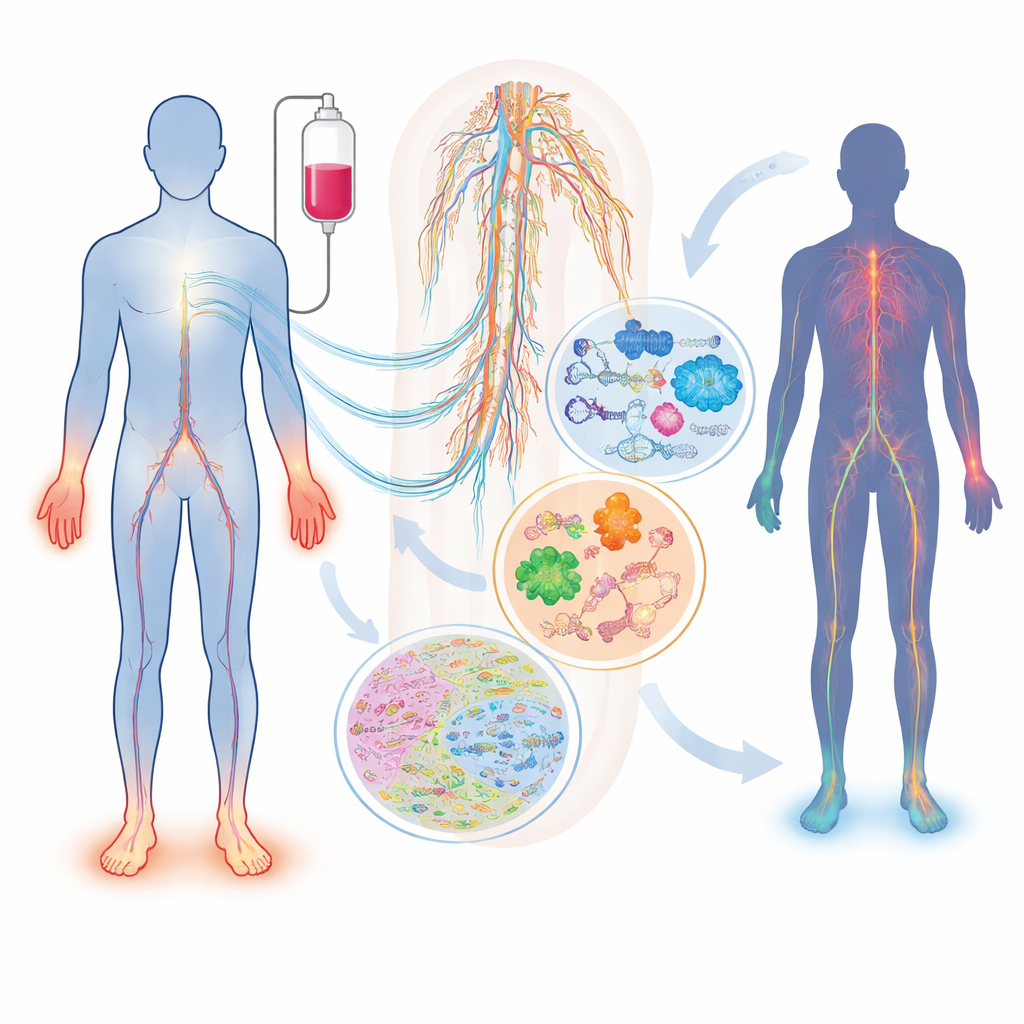
Ce qui arrive aux nerfs pendant la chimiothérapie
Tous les patients exposés au même médicament et à la même dose ne développent pas de lésion nerveuse, et ceux qui en souffrent peuvent présenter des symptômes très différents. La revue décrit comment des médicaments largement utilisés — tels que les taxanes (paclitaxel, docétaxel), les composés à base de platine (cisplatine, oxaliplatine) et les inhibiteurs du protéasome (bortézomib, carfilzomib) — peuvent endommager différemment les nerfs sensitifs, moteurs et autonomes. Des facteurs comme l’âge, le diabète, des carences en vitamines, des problèmes rénaux ou thyroïdiens, et des différences génétiques héréditaires affectant le métabolisme des médicaments ou la structure nerveuse modulent tous le risque individuel. Un marqueur sanguin simple, la chaîne légère de neurofilament, peut déjà suivre les lésions axonales chez les animaux comme chez les patients, mais isolément il ne capture pas la complexité complète de l’affection ni n’explique pourquoi elle se développe.
Comment les omiques offrent une radiographie moléculaire des nerfs lésés
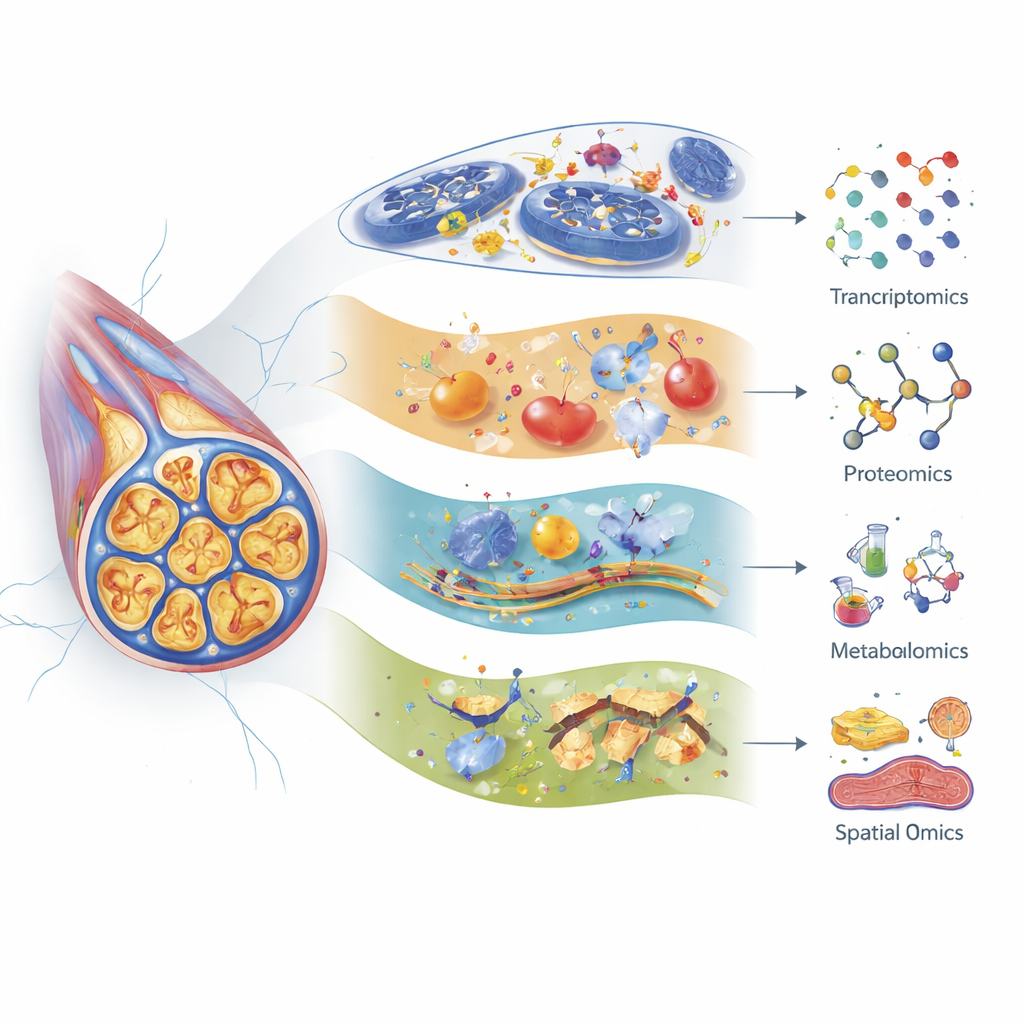
Les auteurs montrent comment la transcriptomique (profilage de l’ARN), la protéomique (analyse à grande échelle des protéines) et la métabolomique (étude systématique des petites molécules) offrent chacune un regard différent sur la lésion nerveuse. Le séquençage d’ARN monocellulaire moderne peut distinguer de nombreux sous‑types de neurones sensitifs et de cellules de soutien dans les ganglions rachidiens — regroupements de corps cellulaires nerveux proches de la moelle — et suivre la réponse de chaque type à différents médicaments de chimiothérapie. Par exemple, certaines fibres sensibles au toucher montrent d’importantes modifications géniques après le paclitaxel, et des gènes liés au vieillissement et à la sénescence nerveuse sont activés après le cisplatine. La protéomique a révélé des modifications précoces des protéines qui maintiennent le cytosquelette, les centrales énergétiques et les réponses au stress, souvent des jours avant que les animaux ne présentent des comportements douloureux. La métabolomique met en évidence des perturbations majeures des lipides, des acides aminés et des acides biliaires, suggérant des problèmes d’utilisation de l’énergie, de stabilité membranaire et d’inflammation qui peuvent varier selon le médicament, l’âge et même le microbiote intestinal.
Voir où la lésion se produit dans les tissus
Au‑delà de l’inventaire des molécules modifiées, des méthodes de spectrométrie de masse « spatiale » plus récentes permettent de montrer précisément où, dans le tissu, ces changements ont lieu. La cytométrie d’imagerie par spectrométrie de masse et l’imagerie par spectrométrie de masse cartographient protéines, lipides, métabolites et même les composés chimiothérapeutiques eux‑mêmes directement sur des sections nerveuses et des coupes de moelle épinière, en conservant l’architecture des neurones, des cellules gliales et des tissus environnants. Des travaux initiaux ont utilisé ces outils pour localiser des neuropeptides liés à la douleur et pour cartographier comment les lipides évoluent dans des régions précises après une lésion nerveuse. Ils ont également suivi des dépôts persistants de platine issus de l’oxaliplatine dans la peau, suggérant que des molécules médicamenteuses qui persistent dans des tissus non cancéreux peuvent contribuer au maintien de symptômes chroniques. Bien que seules quelques études de ce type aient été réalisées spécifiquement sur des nerfs traités par chimiothérapie, la technologie est prête à préciser quels types cellulaires et micro‑régions sont touchés en premier, le plus fortement et le plus durablement.
Assembler toutes les pièces moléculaires
Aucun type d’omics, pris isolément, ne peut expliquer pleinement pourquoi certains patients développent une neuropathie sévère et d’autres non. La revue plaide pour des approches intégrées et multi‑couches qui combinent variation génétique, modifications de l’ARN, réseaux protéiques, variations métaboliques, cartes spatiales, tests de fonction nerveuse et symptômes déclarés par les patients. Les premières études multi‑omiques relient déjà des changements coordonnés dans la signalisation lipidique, les voies inflammatoires, le stress mitochondrial et les systèmes modulateurs de la douleur tels que les endocannabinoïdes et la signalisation opioïde. D’autres associent des messagers lipidiques spécifiques et des acides biliaires d’origine intestinale à la douleur, suggérant de nouvelles cibles médicamenteuses comme les récepteurs des sphingolipides ou des chimiokines qui pourraient atténuer la lésion nerveuse sans affaiblir l’effet anticancéreux. De grandes études humaines soigneusement conçues, alignant données de laboratoire et profils cliniques, seront cruciales pour transformer ces découvertes en outils pratiques.
Ce que cela signifie pour les soins anticancéreux futurs
Pour un lecteur non spécialiste, le message principal est porteur d’espoir : en lisant les empreintes moléculaires laissées dans le sang, le tissu nerveux et même les selles, les chercheurs commencent à prédire qui est le plus à risque de lésion nerveuse, à comprendre comment différents médicaments endommagent le système nerveux et à identifier des points faibles dans ces voies qui pourraient être protégés. Les auteurs concluent que les omiques intégrées, en particulier lorsqu’elles sont appliquées à des échantillons humains suivis dans le temps, pourraient un jour guider les médecins dans le choix des médicaments et des doses adaptés à la biologie de chaque personne, tout en orientant vers de nouveaux traitements protégeant les nerfs. Avec le temps, cette vision systémique pourrait permettre de conserver les bénéfices des chimiothérapies puissantes tout en réduisant fortement la douleur et le handicap durables qui les accompagnent si souvent.
Citation: Piga, I., Bonomo, R., Chinello, C. et al. Using an integrated omics approach to uncover the mechanisms underlying chemotherapy-induced peripheral neuropathy (CIPN). Commun Med 6, 269 (2026). https://doi.org/10.1038/s43856-026-01622-6
Mots-clés: neuropathie périphérique induite par la chimiothérapie, multi-omique, lésion nerveuse, effets secondaires des traitements du cancer, biomarqueurs