Clear Sky Science · zh
GENEVA 平台通过模拟肿瘤镶嵌体揭示对 KRAS 抑制剂的反应差异并识别更优药物组合
这对未来癌症治疗意味着什么
靶向抗癌药旨在攻击肿瘤中特定的遗传弱点,但看似相似的癌症患者对治疗的反应可能截然不同。本文介绍了 GENEVA——一种新的实验平台,它在体外和小鼠体内重建这种真实世界的多样性,并追踪成千上万个单个癌细胞随时间对治疗的反应。通过这种方法,研究者揭示了为何有些细胞死亡、为何有些细胞存活,以及如何选择更聪明的药物组合以防止肿瘤复发。
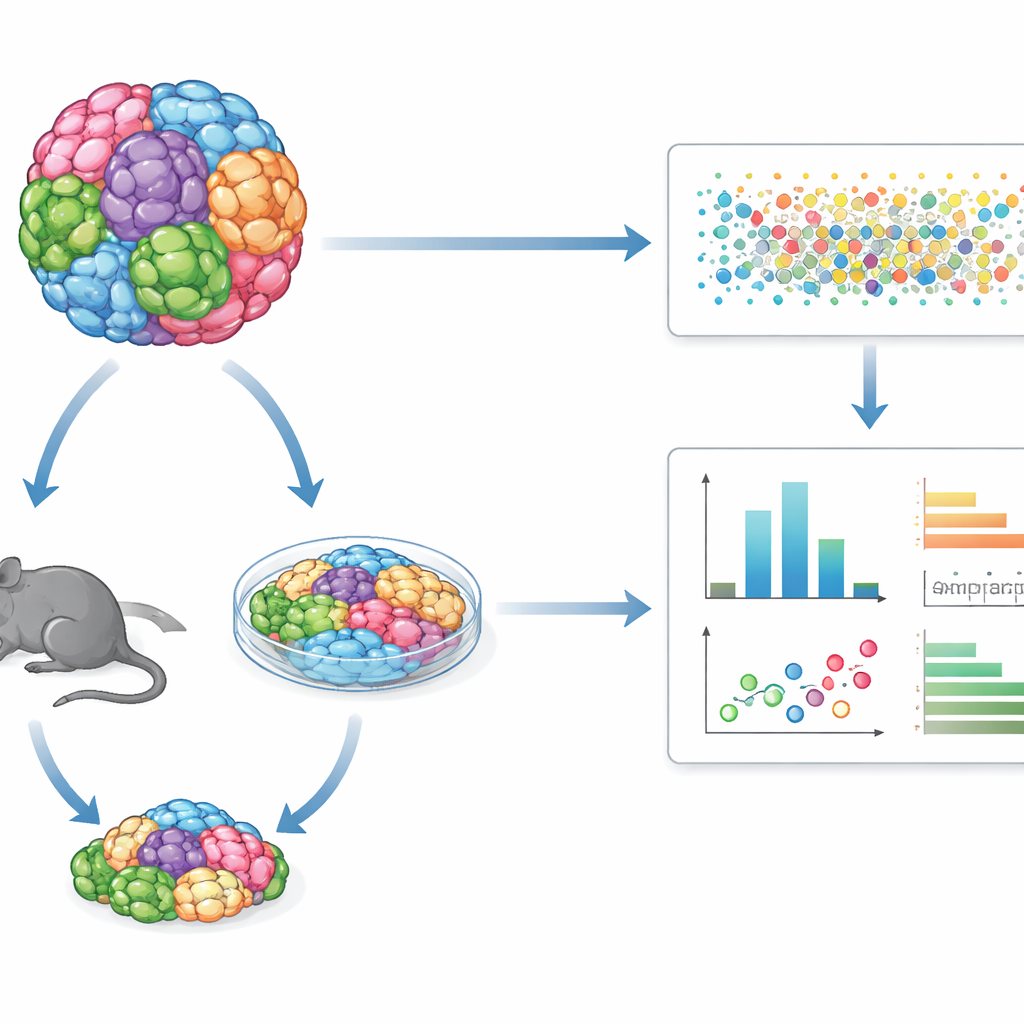
在同一项试验中测试多种肿瘤类型
GENEVA 不是逐一研究单个癌细胞系,而是将数十个遗传上不同的人类癌细胞系或来源于患者的肿瘤样本混合成单一的“镶嵌”培养物或肿瘤。这些混合群体在三维体外培养或以小鼠体内肿瘤的形式生长。用药后,团队利用单细胞 RNA 测序和遗传条码逐细胞读取每个细胞来自哪种遗传背景以及其分子状态。这不仅能测量存活细胞的数量,还能观察其内部程序如何改变,从而在一次实验中揭示多种肿瘤类型的敏感性与耐药性模式。
探查新一类阻断 KRAS 的药物
为展示 GENEVA 的能力,研究者将注意力集中在最近获批的一类阻断致癌突变 KRAS G12C 的药物上。这些药物已为部分肺癌及其他癌症患者带来真实收益,但疗效常常短暂。利用 GENEVA,团队将 KRAS 突变和非突变的细胞系混合,并在不同剂量下用多种 KRAS G12C 抑制剂处理,既在培养皿中也在小鼠体内。正如预期,KRAS G12C 细胞总体上更敏感,但即便在该群体内,也有一些细胞或细胞系存活,提示存在标准检测难以发现的隐藏生存策略。
细胞“动力工厂”的能量激增
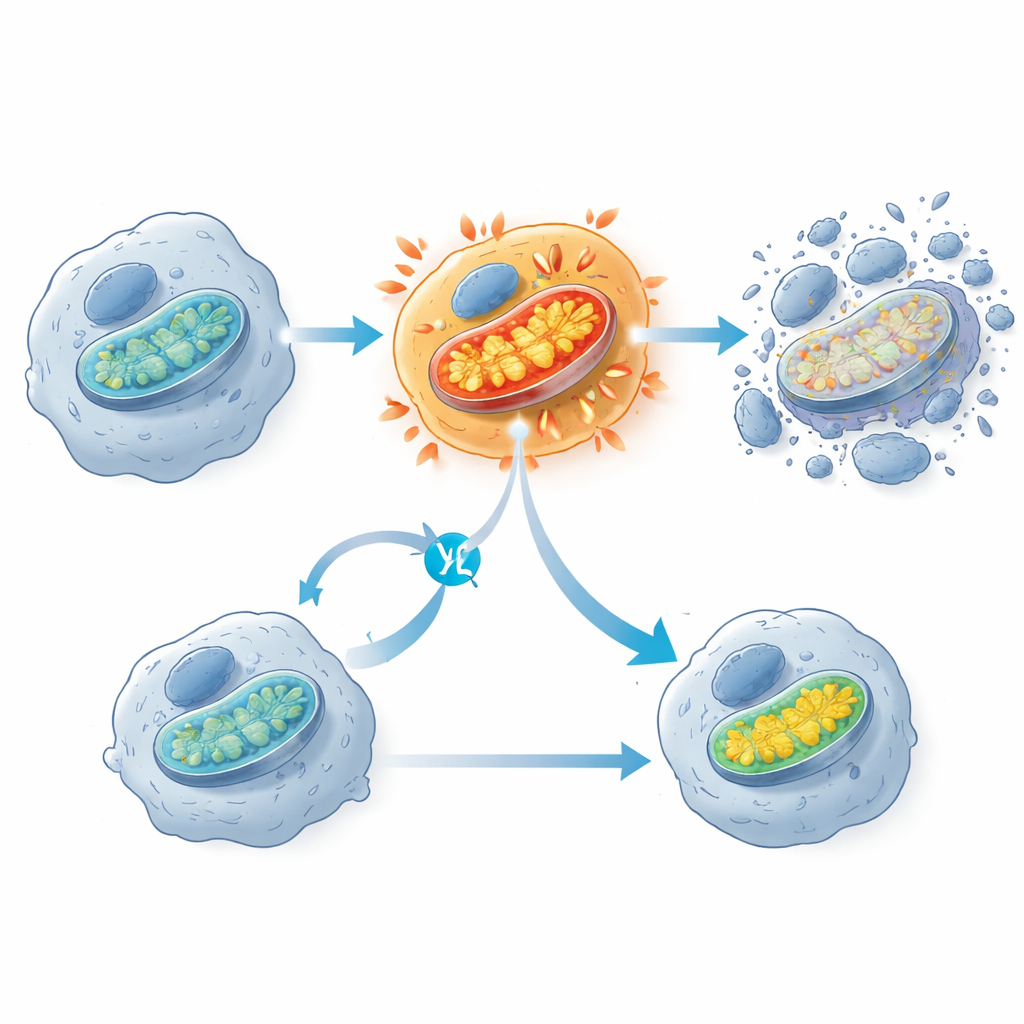
一个显著发现是,KRAS G12C 抑制剂会触发线粒体的早期活性爆发,线粒体通常被描述为细胞的动力工厂。药物暴露后不久,敏感的癌细胞表现出氧耗和线粒体膜电位的短暂峰值,数小时后细胞死亡相关的酶被激活。经受住治疗的细胞通常具有较少的线粒体成分和减弱的线粒体基因活性。当研究者用另一种药物部分阻断线粒体电子传递链时,反而保护了 KRAS G12C 突变细胞免于死亡,这表明这种突发的线粒体过度驱动是将细胞推向死亡边缘的关键步骤。团队还观察到细胞膜脂质的氧化损伤迹象,但阻断该过程并不能阻止细胞死亡,表明它是副作用而非主要的致死开关。
发现隐藏的逃逸通路与更佳配对方案
由于 GENEVA 能对成千上万存活细胞进行谱系描绘,它可以凸显在药物耐受的 KRAS G12C 细胞中特异性上调的基因和通路。研究指出了若干此类路径,包括通过 mTOR 的信号传导、改变 DNA 包装的酶类,以及与上皮-间质转化(EMT,影响细胞形态和迁移)相关的程序。许多这些特征在小鼠体内生长的肿瘤中更为显著,在那里存在周围组织的微环境。受这些信号指引,团队测试了联合治疗:将 KRAS G12C 抑制剂与 mTOR 抑制剂或与阻断 TGF-β(EMT 的驱动因子)药物联用,在小鼠中比任何单药均呈现更强且更持久的肿瘤缩小。
从单细胞到更明智的精准疗法
简单来说,这项工作表明癌细胞如何管理其能量与形态,能决定一个靶向 KRAS 的药物是将其治愈还是仅仅抑制其生长。GENEVA 平台使得在多种肿瘤类型和条件下同时观察这些决策成为可能,从而揭示共同薄弱点与逃逸通路。通过识别线粒体的“能量激增”有助于杀死 KRAS G12C 突变细胞,以及像 mTOR 和 EMT 这样的通路让部分细胞逃逸,研究指向了可望延长患者反应的具体药物组合。更广泛地说,GENEVA 提供了一种在临床试验前于逼真、遗传多样的模型中测试未来抗癌药物的方法,增加精准疗法惠及更多患者的可能性。
引用: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
关键词: KRAS G12C 抑制剂, 肿瘤异质性, 线粒体代谢, 药物耐药, 联合抗癌治疗