Clear Sky Science · ru
Платформа GENEVA моделирует мозаичность опухолей, чтобы выявить вариативность ответов на ингибиторы KRAS и подобрать улучшенные комбинации препаратов
Почему это важно для будущего лечения рака
Таргетные противораковые препараты разрабатываются для поражения конкретных генетических уязвимостей опухолей, однако пациенты с, казалось бы, похожими раками могут отвечать на лечение очень по‑разному. В этой статье представлена GENEVA — новая экспериментальная платформа, которая воссоздаёт такое реальное разнообразие в лаборатории и на мышах, а затем отслеживает, как тысячи отдельных раковых клеток реагируют на терапию со временем. Это позволяет исследователям понять, почему одни клетки гибнут, другие выживают, и как выбирать более разумные сочетания препаратов, которые могли бы помешать рецидиву опухоли.
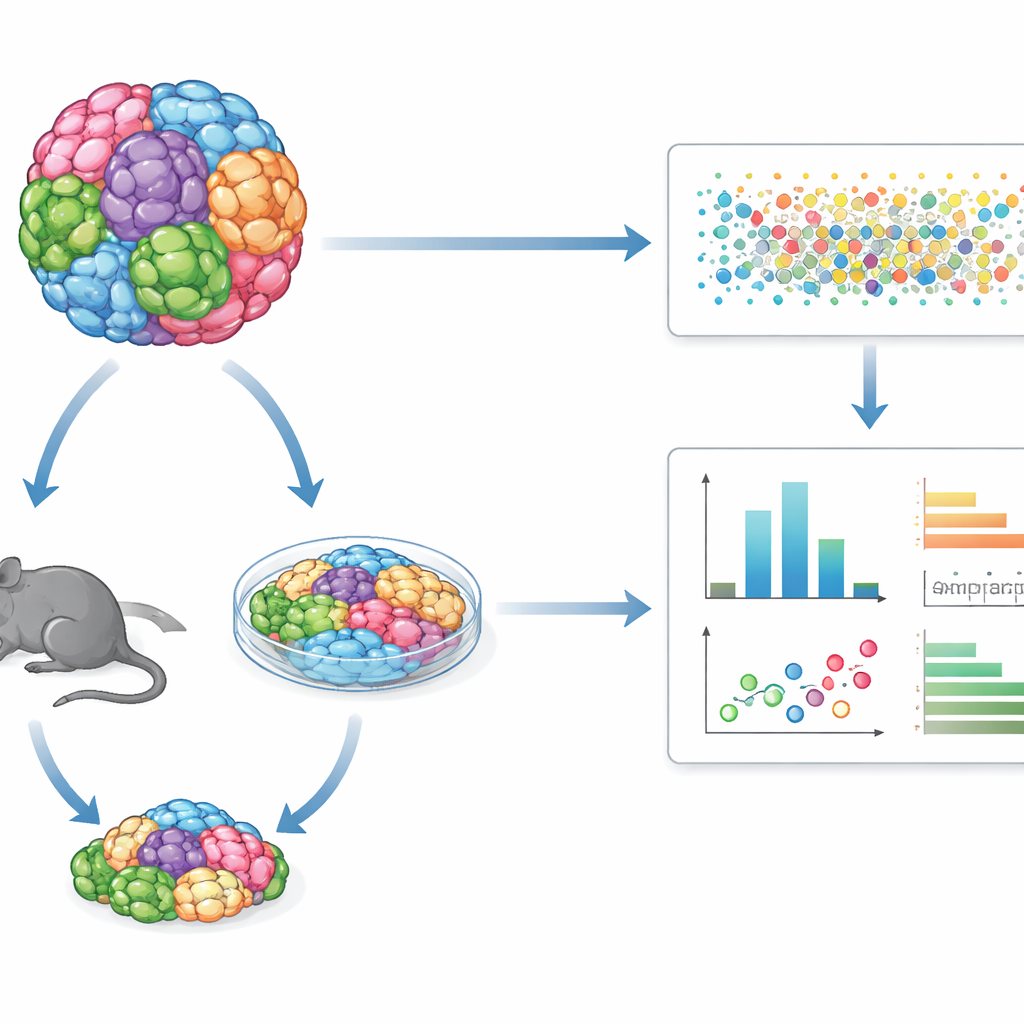
Много типов опухолей в одном общем испытании
Вместо изучения одной линии раковых клеток за раз GENEVA смешивает десятки генетически различных человеческих линий клеток или образцов опухолей от пациентов в единую «мозаичную» культуру или опухоль. Эти смешанные популяции выращивают либо в трёхмерных культурах в лаборатории, либо в виде опухолей у мышей. После лечения препаратом команда использует одноклеточное РНК‑секвенирование и генетические штрих‑коды, чтобы построчно определить, из какого генетического фона пришла каждая клетка и в каком молекулярном состоянии она находится. Это позволяет измерять не только число выживших клеток, но и то, как меняются их внутренние программы, выявляя шаблоны чувствительности и устойчивости сразу для многих типов опухолей в одном эксперименте.
Исследование нового класса препаратов, блокирующих KRAS
Чтобы продемонстрировать возможности GENEVA, исследователи сосредоточились на недавно одобренной группе препаратов, блокирующих онкогенную мутацию KRAS G12C. Эти лекарства принесли реальную пользу некоторым пациентам с раком лёгких и другими опухолями, но ответы часто бывают недолгими. Используя GENEVA, команда объединила линии клеток с мутацией KRAS и без неё и обработала их несколькими ингибиторами KRAS G12C в разных дозах как в чашках, так и у мышей. Как и ожидалось, клетки с KRAS G12C в целом были более чувствительны, но даже в этой группе некоторые клетки или линии сохранялись, что указывает на скрытые стратегии выживания, которые ускользают от стандартных тестов.
Всплеск активности в энергетических станциях клетки
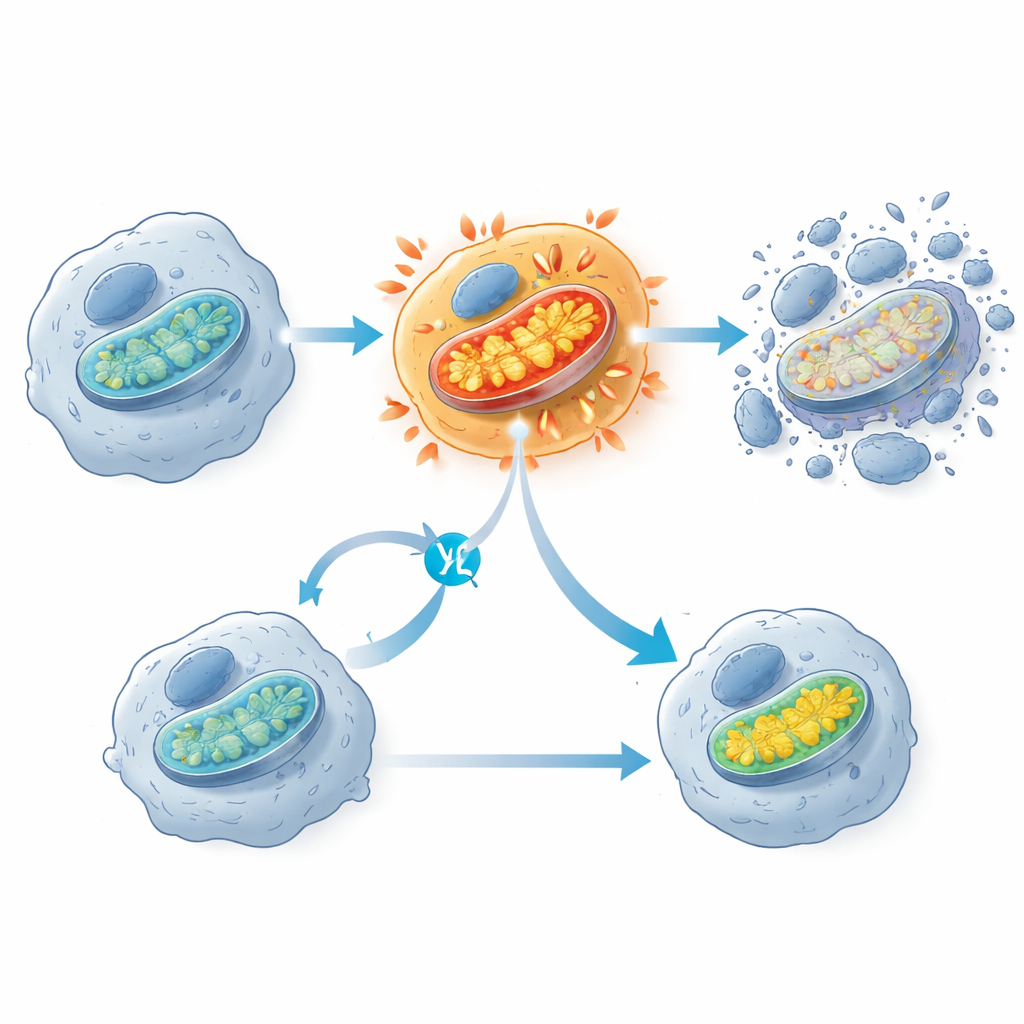
Впечатляющий вывод заключался в том, что ингибиторы KRAS G12C вызывают ранний всплеск активности митохондрий — структур, которые часто называют энергетическими станциями клетки. Вскоре после воздействия препарата чувствительные раковые клетки демонстрировали рост потребления кислорода и мембранного потенциала митохондрий, за которым через несколько часов следовала активация ферментов, запускающих гибель клетки. Клетки, пережившие лечение, как правило, имели меньше митохондриальных компонентов и пониженную активность митохондриальных генов. Когда исследователи частично блокировали электронную транспортную цепь митохондрий другим веществом, это фактически защищало клетки с KRAS G12C от гибели, что указывает на то, что этот внезапный митохондриальный «разгон» является ключевым шагом, подталкивающим клетки за грань. Команда также зафиксировала признаки окислительного повреждения липидов в клеточных мембранах, но блокада этого процесса не предотвращала гибель клеток, что говорит о том, что это скорее побочный эффект, чем основной механизм смерти.
Выявление скрытых путей спасения и более удачных сочетаний
Поскольку GENEVA профилирует тысячи выживших клеток, платформа может выделить гены и пути, которые специфически активированы в лекарственно‑толерантных клетках KRAS G12C. В исследовании были отмечены несколько таких направлений, включая сигналы через mTOR, ферменты, изменяющие упаковку ДНК, и программы, связанные с изменением формы и подвижности клетки, известные как эпителиально‑мезенхимальный переход (EMT). Многие из этих особенностей проявлялись сильнее всего в опухолях, растущих в мышах, где присутствует окружающая тканевая микроокружение. Исходя из этих сигналов, команда протестировала комбинированные подходы: сочетание ингибитора KRAS G12C с ингибитором mTOR или с блокатором TGF‑β (активатора EMT) вызывало более сильное и продолжительное сокращение опухолей у мышей, чем любой отдельный препарат.
От отдельных клеток к более умной точной терапии
Проще говоря, работа показывает, что то, как раковая клетка управляет своей энергией и формой, может определять, вылечит ли её таргетный препарат против KRAS, либо он лишь замедлит рост. Платформа GENEVA даёт возможность наблюдать, как эти решения разворачиваются одновременно в разных типах опухолей и условиях, выявляя общие слабые места и пути ухода. Выявив, что митохондриальный «энергетический всплеск» помогает убивать клетки с мутацией KRAS G12C, а пути, такие как mTOR и EMT, позволяют некоторым клеткам уходить, исследование указывает на конкретные комбинации препаратов, которые могут продлить ответ у пациентов. В более широком смысле GENEVA предлагает способ тестировать будущие противораковые лекарства в реалистичных, генетически разнообразных моделях задолго до клинических испытаний, повышая шансы того, что таргетная терапия сработает для большего числа людей.
Цитирование: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Ключевые слова: ингибиторы KRAS G12C, гетерогенность опухоли, митохондриальный метаболизм, лекарственная резистентность, комбинированная терапия рака