Clear Sky Science · de
Die GENEVA-Plattform modelliert Tumormosaik und zeigt Variationen der Reaktionen auf KRAS-Inhibitoren sowie verbesserte Wirkstoffkombinationen auf
Warum das für künftige Krebstherapien wichtig ist
Gezielte Krebstherapeutika sollen spezifische genetische Schwachstellen in Tumoren angreifen, doch Patienten mit scheinbar ähnlichen Krebsarten können sehr unterschiedlich reagieren. Dieser Artikel stellt GENEVA vor, eine neue experimentelle Plattform, die diese reale Vielfalt im Labor und in Mäusen nachbildet und dann über die Zeit verfolgt, wie tausende einzelne Krebszellen auf Behandlungen reagieren. Dadurch decken die Forschenden auf, warum einige Zellen sterben, andere überdauern und wie man intelligentere Wirkstoffkombinationen auswählt, die das Wiederauftauchen von Tumoren verhindern könnten.
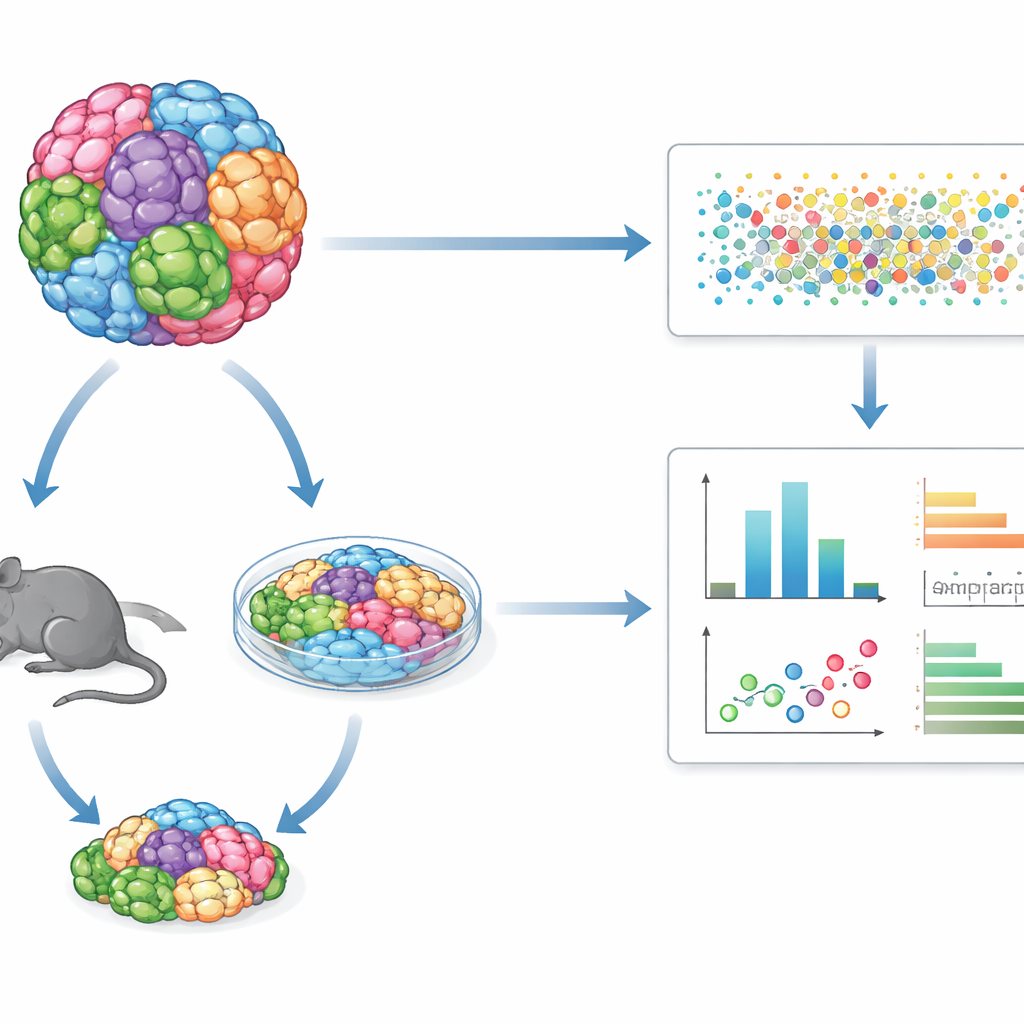
Viele Tumortypen in einem gemeinsamen Test
Statt eine Zelllinie nach der anderen zu untersuchen, mischt GENEVA Dutzende genetisch unterschiedlicher menschlicher Krebszelllinien oder patientenabgeleiteter Tumorproben zu einer einzigen „Mosaik“-Kultur oder einem Tumor. Diese gemischten Populationen werden entweder in dreidimensionalen Labor-Kulturen oder als Tumoren in Mäusen gezüchtet. Nach einer Behandlung mit einem Wirkstoff nutzen die Forschenden Einzelzell-RNA-Sequenzierung und genetische Barcodes, um Zelle für Zelle auszulesen, aus welchem genetischen Hintergrund jede Zelle stammt und in welchem molekularen Zustand sie sich befindet. So können sie nicht nur messen, wie viele Zellen überleben, sondern auch, wie sich ihre inneren Programme verändern — und dabei Muster von Sensitivität und Resistenz über viele Tumortypen in einem Experiment aufdecken.
Untersuchung einer neuen Klasse KRAS-blockierender Wirkstoffe
Um die Leistungsfähigkeit von GENEVA zu demonstrieren, konzentrierte sich das Team auf eine kürzlich zugelassene Gruppe von Wirkstoffen, die eine krebsanregende Mutation namens KRAS G12C blockieren. Diese Medikamente haben einigen Patientinnen und Patienten mit Lungen- und anderen Krebsarten echte Vorteile gebracht, doch die Ansprechraten sind oft nur von kurzer Dauer. Mit GENEVA bündelte das Team KRAS-mutierte und nicht-mutierte Zelllinien und behandelte sie mit mehreren KRAS G12C-Inhibitoren in unterschiedlichen Dosen, sowohl in Zellkulturen als auch in Mäusen. Wie zu erwarten, waren KRAS G12C-Zellen insgesamt empfindlicher, doch selbst innerhalb dieser Gruppe überdauerten einige Zellen oder Linien, was auf verborgene Überlebensstrategien hinweist, die Standardassays übersehen würden.
Power-Schub in den Kraftwerken der Zelle
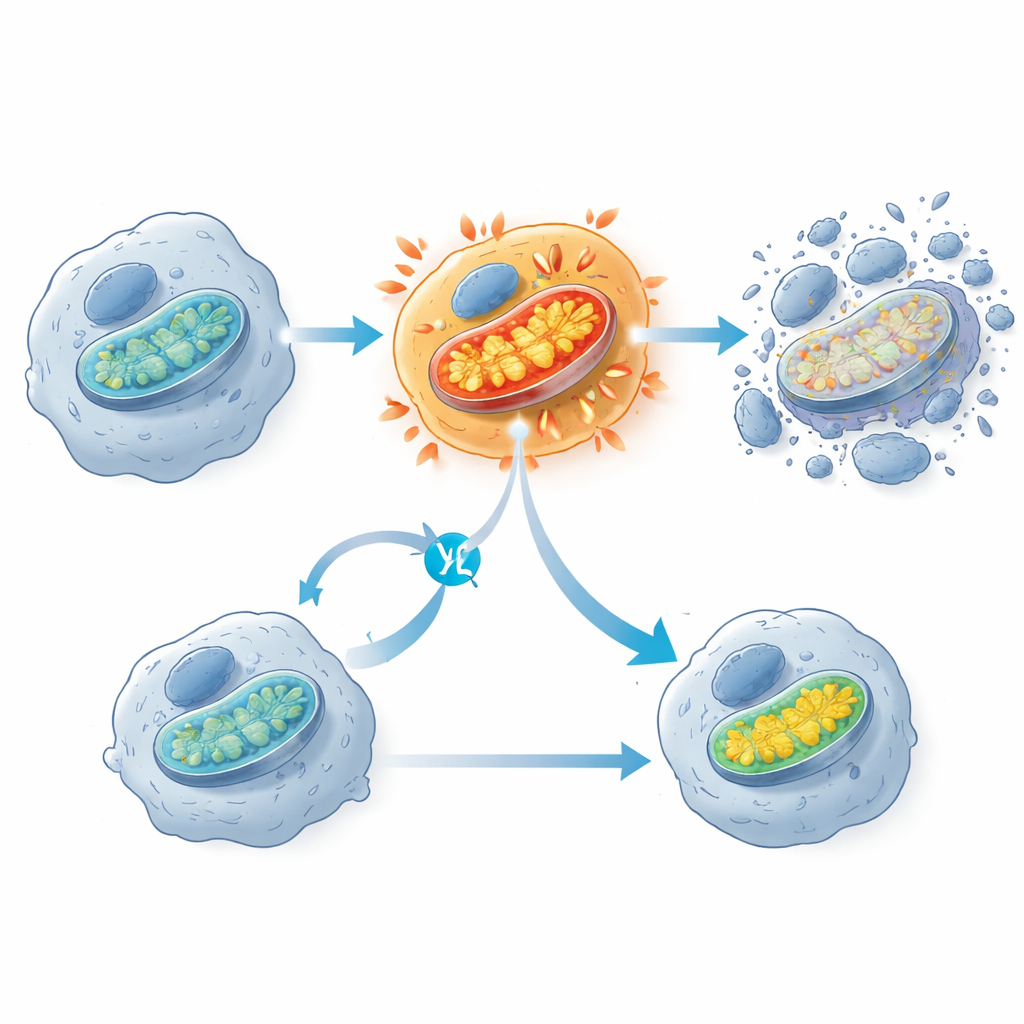
Eine auffällige Beobachtung war, dass KRAS G12C-Inhibitoren einen frühen Aktivitätsschub in den Mitochondrien auslösen — den Strukturen, die oft als Kraftwerke der Zelle beschrieben werden. Kurz nach der Wirkstoffexposition zeigten sensible Krebszellen einen Anstieg des Sauerstoffverbrauchs und des mitochondrialen Membranpotenzials, gefolgt Stunden später von der Aktivierung von Todesenzymen. Zellen, die die Behandlung überstanden, wiesen tendenziell weniger mitochondriale Komponenten und abgeschwächte mitochondriale Genaktivität auf. Wenn die Forschenden die mitochondriale Elektronentransportkette teilweise mit einem anderen Wirkstoff blockierten, schützte dies die KRAS G12C-mutierten Zellen tatsächlich vor dem Zelltod, was darauf hindeutet, dass dieser plötzliche mitochondriale Überantrieb ein Schlüsselereignis ist, das die Zellen über die Kippe treibt. Das Team beobachtete außerdem Anzeichen von oxidativen Schäden an Membranlipiden, doch das Blockieren dieses Prozesses verhinderte den Zelltod nicht, sodass es sich offenbar um einen Nebeneffekt und nicht um den hauptsächlichen Auslöser handelt.
Verdeckte Fluchtwege aufdecken und bessere Kombinationen finden
Weil GENEVA Tausende überlebender Zellen profilieren kann, hebt es Gene und Signalwege hervor, die speziell in arzneimittel-toleranten KRAS G12C-Zellen hochreguliert sind. Die Studie identifizierte mehrere solcher Routen, darunter Signalübertragung über mTOR, Enzyme, die die DNA-Verpackung verändern, und Programme, die mit Form- und Bewegungsveränderungen der Zelle verbunden sind, bekannt als epithelial–mesenchymale Transition (EMT). Viele dieser Merkmale traten besonders stark in Tumoren auf, die in Mäusen wuchsen, wo das umgebende Gewebemikromilieu vorhanden ist. Anhand dieser Signale testete das Team Kombinationstherapien. Die Kombination eines KRAS G12C-Inhibitors mit einem mTOR-Inhibitor oder mit einem Hemmer von TGF-β (einem Treiber von EMT) führte in Mäusen zu stärkeren und länger anhaltenden Tumorrückbildungen als jeder Einzelwirkstoff allein.
Von Einzelzellen zu klügeren Präzisionstherapien
Vereinfacht gesagt zeigt diese Arbeit, dass die Art und Weise, wie eine Krebszelle ihre Energie und Gestalt handhabt, darüber entscheiden kann, ob ein gezielter KRAS-Wirkstoff sie heilbar macht oder nur verlangsamt. Die GENEVA-Plattform macht es möglich, diese Entscheidungen zugleich über viele Tumortypen und Bedingungen hinweg zu beobachten und gemeinsame Schwachstellen und Fluchtwege aufzudecken. Indem sie identifiziert, dass ein mitochondrialer „Power-Schub“ beim Abtöten von KRAS G12C-mutierten Zellen hilft und dass Wege wie mTOR und EMT einigen Zellen das Entkommen erlauben, weist die Studie auf konkrete Wirkstoffkombinationen hin, die das Ansprechen bei Patientinnen und Patienten verlängern könnten. Allgemeiner bietet GENEVA eine Möglichkeit, künftige Krebsmedikamente in realistischen, genetisch vielfältigen Modellen lange vor klinischen Studien zu testen und so die Wahrscheinlichkeit zu erhöhen, dass Präzisionstherapien für mehr Menschen wirken.
Zitation: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Schlüsselwörter: KRAS G12C-Inhibitoren, Tumorheterogenität, mitochondriale Stoffwechselprozesse, Arzneimittelresistenz, Kombinationstherapie bei Krebs