Clear Sky Science · ja
GENEVAプラットフォームは腫瘍のモザイク性をモデル化し、KRAS阻害薬への反応の差異を明らかにし改善された薬剤併用を同定する
将来のがん治療にとってなぜ重要か
標的薬は腫瘍の特定の遺伝的弱点を突くよう設計されていますが、見た目は似ているが反応が大きく異なる患者がいるのが現実です。本稿はGENEVAという新しい実験プラットフォームを紹介します。GENEVAは実際の多様性を試験管やマウス内で再現し、数千の個々のがん細胞が時間経過で治療にどう応答するかを追跡します。こうして研究者らは、なぜ一部の細胞が死に、他が生き残るのかを突き止め、がんが再発するのを防ぐためのより賢い薬剤併用を選ぶ手がかりを得ます。
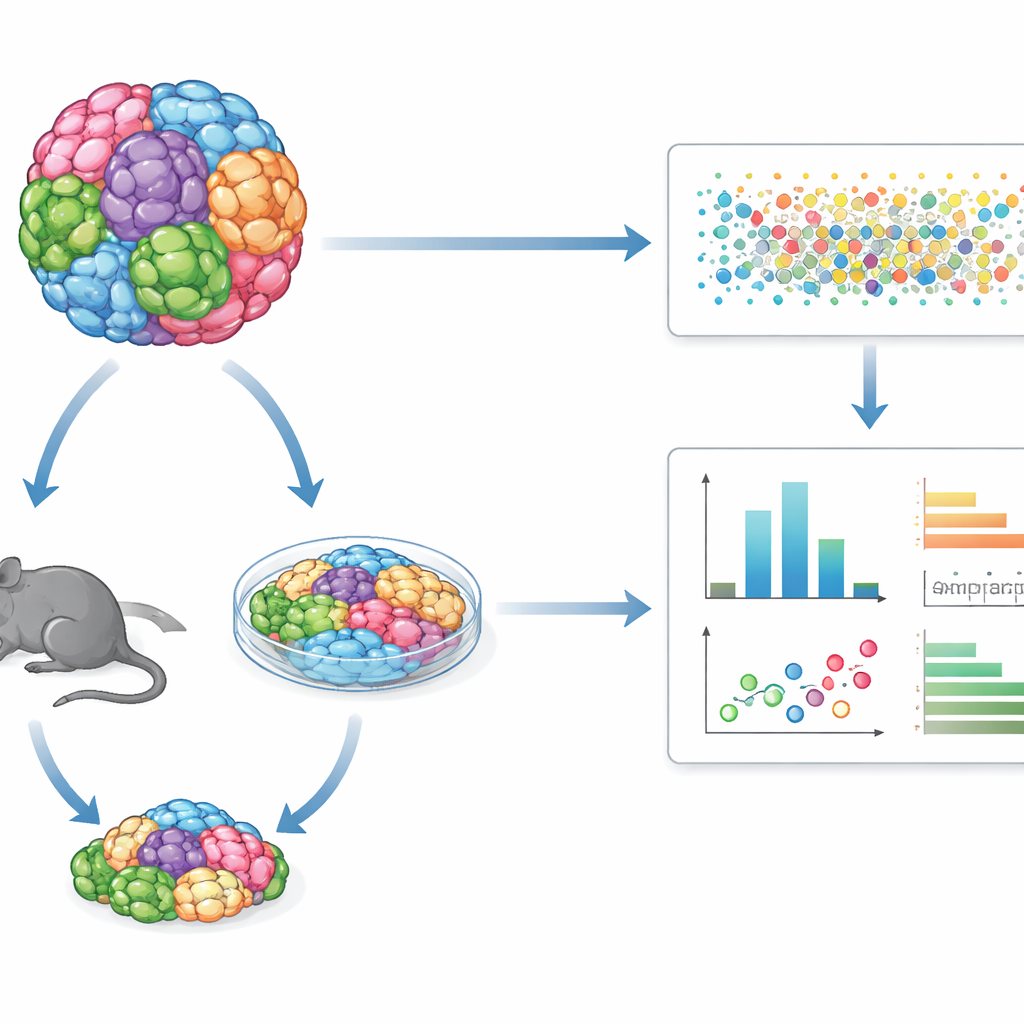
単一の共通試験で多数の腫瘍種を解析
GENEVAでは一度に一つの細胞株を調べる代わりに、遺伝的に異なる数十のヒトがん細胞株や患者由来腫瘍試料を混ぜ合わせた「モザイク」培養や腫瘍として扱います。これらの混合集団は立体培養またはマウス内腫瘍として増殖させます。薬剤処理後、単一細胞RNAシーケンスと遺伝的バーコードを用いて、細胞ごとにどの遺伝的背景に由来するか、どのような分子状態にあるかを読み取ります。これにより生存する細胞数だけでなく、細胞内部のプログラムがどう変化するかを測定でき、1回の実験で多くの腫瘍種にわたる感受性と耐性のパターンを明らかにします。
新たなKRAS阻害薬クラスの検証
GENEVAの力を示すために、研究チームはKRAS G12Cというがんを駆動する変異を阻害する、最近承認された薬剤群に注目しました。これらは肺がんなどで実際の利益をもたらしていますが、反応はしばしば長続きしません。GENEVAを用いて、KRAS変異を持つ細胞株と持たない細胞株を混合し、複数のKRAS G12C阻害薬を異なる用量で培養およびマウス内で投与しました。予想どおりKRAS G12C細胞は一般に感受性が高かったものの、その群内でも一部の細胞や株は生き残り、従来のアッセイでは見落とされる隠れた生存戦略の存在を示しました。
細胞の“発電所”で起きるパワーサージ
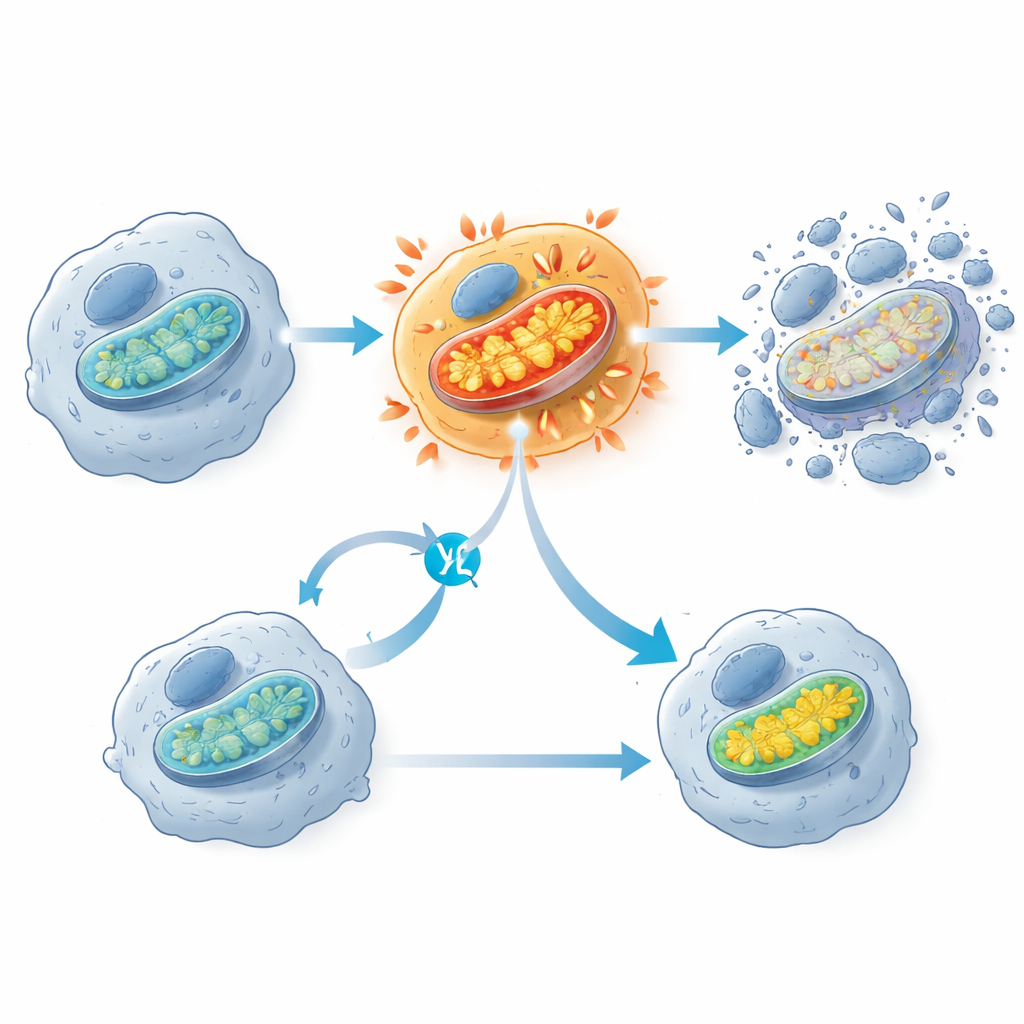
注目すべき発見は、KRAS G12C阻害薬がミトコンドリア(しばしば細胞の発電所と呼ばれる構造)で早期の活動急増を引き起こすことでした。薬剤露出の直後、感受性のあるがん細胞では酸素消費量とミトコンドリア膜電位が急上昇し、数時間後に細胞死酵素が活性化しました。一方、治療を耐え抜く細胞はミトコンドリア構成要素が少なく、ミトコンドリア遺伝子の活動が抑えられている傾向がありました。研究者らが別の薬剤でミトコンドリア電子伝達鎖を部分的に阻害すると、むしろKRAS G12C変異細胞が死から保護され、この急激なミトコンドリアの過活動が細胞を死に至らしめる重要な段階であることを示唆しました。膜脂質に対する酸化的ダメージの兆候も観察されましたが、これを阻害しても細胞死は防げず、主たる死の引き金ではなく副次的な影響であることが示されました。
隠れた逃避経路とより良い併用療法の発見
GENEVAは生き残った何千もの細胞をプロファイリングできるため、薬剤耐性を示すKRAS G12C細胞で特異的に活性化される遺伝子や経路を浮かび上がらせます。本研究はmTORを介したシグナル伝達、DNAのパッケージングを変える酵素、および上皮–間葉転換(EMT)として知られる形態・運動性の変化に関連するプログラムなど、いくつかの回避経路を指摘しました。これらの特徴は、周辺組織の微小環境が存在するマウス内で特に強く現れました。こうしたシグナルに導かれて、研究チームは併用療法を試験しました。KRAS G12C阻害薬とmTOR阻害薬、あるいはTGF-β(EMTを駆動する因子)阻害薬を組み合わせると、単剤よりもマウスでより強くかつ持続的な腫瘍縮小をもたらしました。
単一細胞からより賢い精密医療へ
平たく言えば、この研究はがん細胞がエネルギーや形をどう管理するかが、標的とするKRAS薬が細胞を治癒するか単に抑制するかを左右することを示しています。GENEVAプラットフォームにより、多数の腫瘍種と条件にわたってこうした決定過程を同時に観察でき、共通の弱点や逃避経路を明らかにできます。ミトコンドリアの「パワーサージ」がKRAS G12C変異細胞を死に至らしめる助けになり、mTORやEMTのような経路が一部の細胞を逃がすことを同定したことで、本研究は患者における反応持続を延ばしうる具体的な薬剤併用を示しています。より広くは、GENEVAは臨床試験のはるか前に遺伝的に多様な現実的モデルで将来のがん薬を検証する方法を提供し、より多くの人に精密治療が効く可能性を高めます。
引用: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
キーワード: KRAS G12C阻害薬, 腫瘍の不均一性, ミトコンドリア代謝, 薬剤耐性, 併用がん療法