Clear Sky Science · pl
Platforma GENEVA modeluje mozaikowość nowotworów, aby ujawnić zróżnicowane odpowiedzi na inhibitory KRAS i zidentyfikować lepsze kombinacje leków
Dlaczego ma to znaczenie dla przyszłych terapii przeciwnowotworowych
Leki celowane w onkologii są projektowane tak, by atakować konkretne genetyczne słabości nowotworów, tymczasem pacjenci z pozornie podobnymi nowotworami mogą reagować bardzo różnie. W artykule przedstawiono GENEVA — nową platformę eksperymentalną, która odtwarza tę rzeczywistą różnorodność w laboratorium i na myszach, a następnie śledzi, jak tysiące pojedynczych komórek nowotworowych reaguje na leczenie w czasie. Dzięki temu badacze odkrywają, dlaczego niektóre komórki umierają, dlaczego inne przetrwają i jak wybierać mądrzejsze kombinacje leków, które mogłyby zapobiec nawrotom choroby.
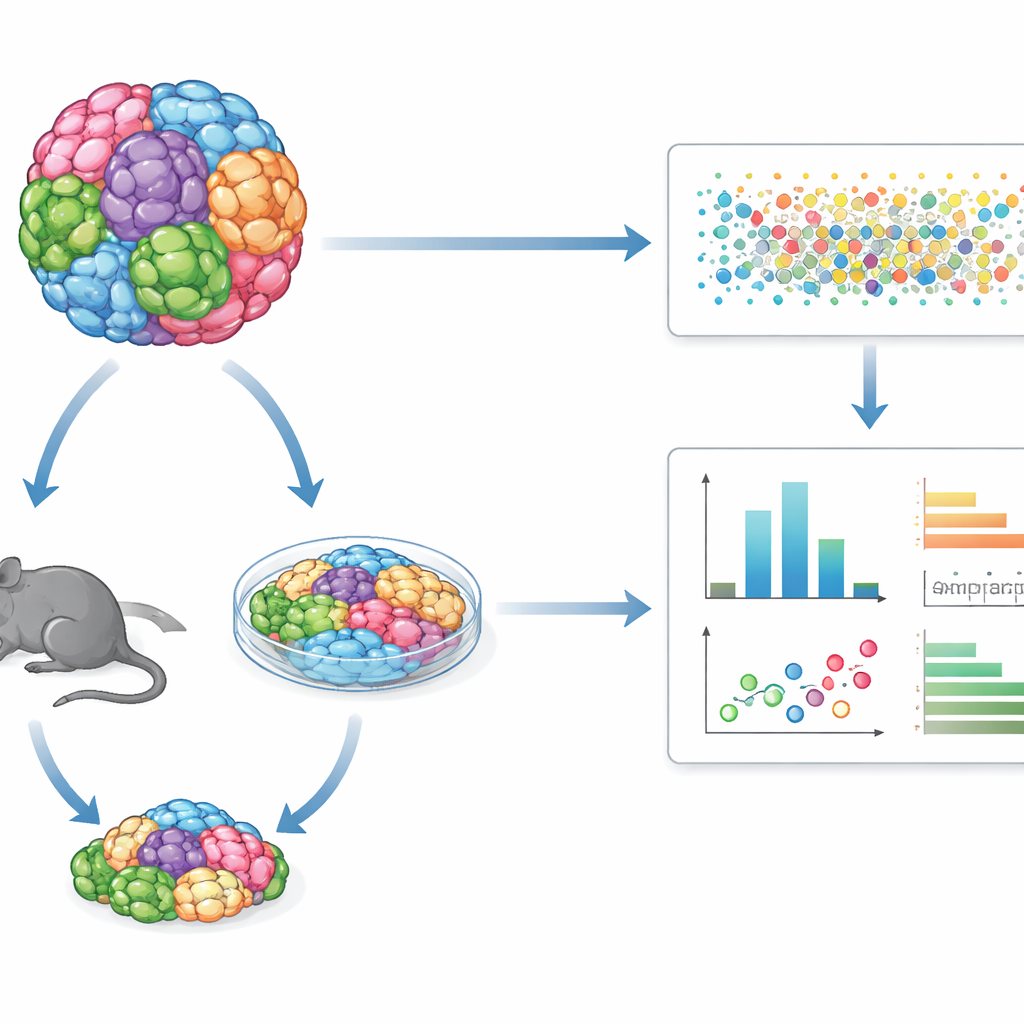
Wiele typów nowotworów w jednym wspólnym teście
Zamiast badać po jednej linii komórkowej nowotworu, GENEVA miesza dziesiątki genetycznie odmiennych ludzkich linii komórkowych lub próbek pochodzących od pacjentów w ramach jednej „mozaikowej” hodowli lub guza. Takie mieszane populacje są hodowane albo w trójwymiarowych kulturach laboratoryjnych, albo jako guzy u myszy. Po podaniu leku zespół używa sekwencjonowania RNA pojedynczych komórek oraz genetycznych kodów kreskowych, by odczytać, komórka po komórce, z jakiego tła genetycznego pochodzi każda komórka i jaki ma stan molekularny. Pozwala to mierzyć nie tylko ile komórek przeżywa, lecz także jak zmieniają się ich wewnętrzne programy, ujawniając wzory wrażliwości i oporności w wielu typach nowotworów w ramach jednego eksperymentu.
Badanie nowej klasy leków blokujących KRAS
Aby zaprezentować możliwości GENEVA, badacze skupili się na niedawno zatwierdzonej grupie leków blokujących mutację napędzającą nowotwór — KRAS G12C. Leki te przyniosły rzeczywiste korzyści niektórym chorym z rakiem płuca i innymi nowotworami, lecz odpowiedzi często są krótkotrwałe. Korzystając z GENEVA, zespół połączył linie komórkowe z mutacją KRAS i bez niej i leczył je kilkoma inhibitorami KRAS G12C w różnych dawkach, zarówno w hodowlach, jak i u myszy. Jak można się było spodziewać, komórki z KRAS G12C były ogólnie bardziej wrażliwe, ale nawet w tej grupie niektóre komórki lub linie przetrwały, co wskazuje na ukryte strategie przetrwania, których standardowe testy by nie wykryły.
Wzrost aktywności w „elektrowni” komórki
Uderzającym odkryciem było to, że inhibitory KRAS G12C wywołują wczesny wysyp aktywności w mitochondriach — strukturach często opisywanych jako elektrownie komórki. Krótko po ekspozycji na lek wrażliwe komórki nowotworowe wykazywały skok w pobieraniu tlenu i potencjale błony mitochondrialnej, po którym kilka godzin później następowała aktywacja enzymów odpowiedzialnych za śmierć komórki. Komórki, które przetrwały terapię, miały zwykle mniej składników mitochondrialnych i stłumioną aktywność genów mitochondrialnych. Gdy badacze częściowo zablokowali łańcuch transportu elektronów mitochondriów innym lekiem, w rzeczywistości chroniło to komórki z mutacją KRAS G12C przed śmiercią, co sugeruje, że ten nagły mitochondrialny „zryw mocy” jest kluczowym krokiem, który popycha komórki za próg nieodwracalnej utraty żywotności. Zespół zaobserwował także oznaki uszkodzeń oksydacyjnych lipidów w błonach komórkowych, lecz blokowanie tego procesu nie zapobiegało śmierci komórek, co wskazuje, że jest to skutek uboczny, a nie główny mechanizm zabijający.
Odkrywanie ukrytych dróg ucieczki i lepszych połączeń terapeutycznych
Ponieważ GENEVA profiluje tysiące komórek, które przeżyły, potrafi wyróżnić geny i szlaki, które są specyficznie aktywowane w komórkach tolerujących lek z mutacją KRAS G12C. Badanie wskazało kilka takich dróg, w tym sygnalizację przez mTOR, enzymy modyfikujące upakowanie DNA oraz programy związane ze zmianami kształtu i ruchliwości komórek, znane jako przejście epitelialno-mezenchymalne (EMT). Wiele z tych cech pojawiało się najsilniej w guzach rosnących u myszy, gdzie obecne jest otaczające mikrośrodowisko tkankowe. Kierując się tymi sygnałami, zespół przetestował terapie skojarzone. Połączenie inhibitora KRAS G12C z inhibitorem mTOR lub z blokującym TGF-β (czynnik napędzający EMT) dawało silniejsze i trwalsze kurczenie się guzów u myszy niż jakikolwiek pojedynczy lek.
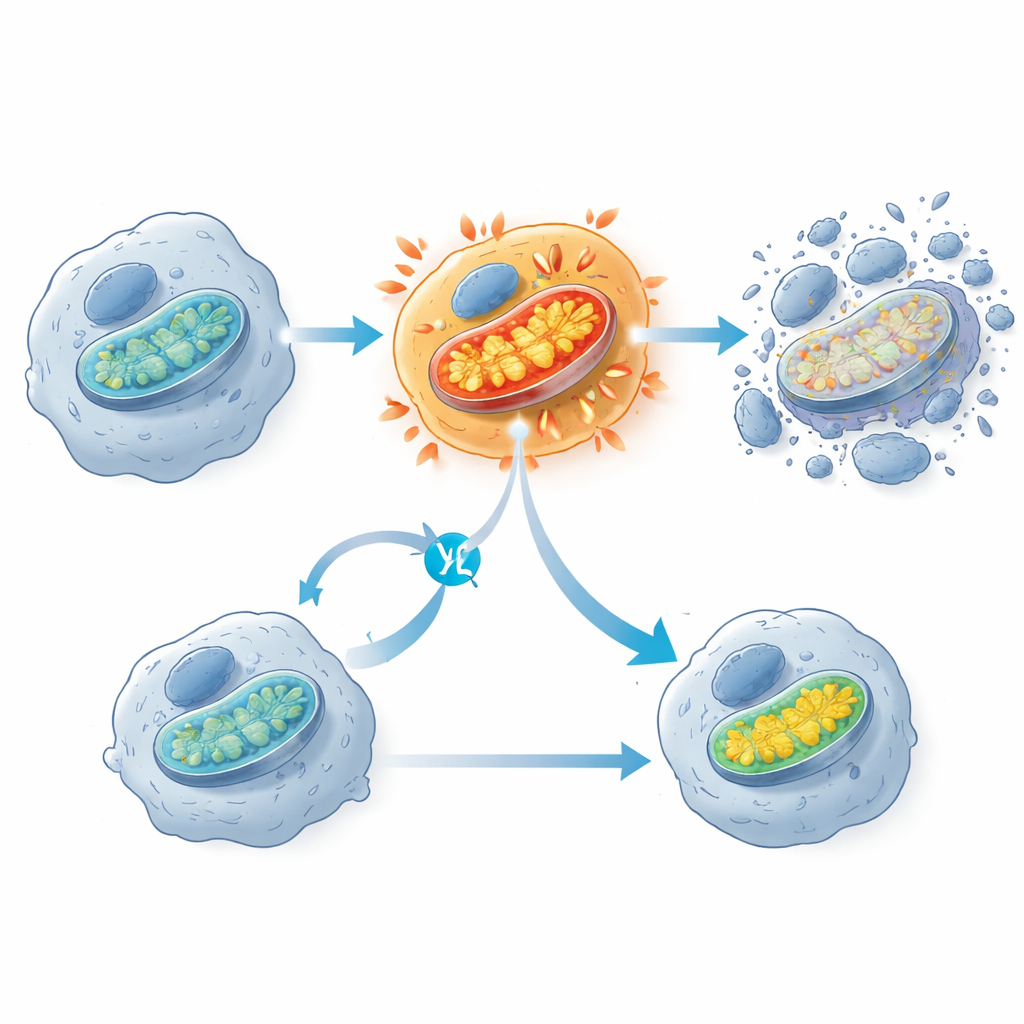
Od pojedynczych komórek do mądrzejszych terapii precyzyjnych
Mówiąc prosto, praca ta pokazuje, że sposób, w jaki komórka nowotworowa gospodaruje energią i kształtem, może zadecydować, czy celowany lek przeciwko KRAS ją wyleczy, czy jedynie spowolni. Platforma GENEVA umożliwia obserwowanie tych decyzji w wielu typach nowotworów i warunkach jednocześnie, ujawniając wspólne słabe punkty i drogi ucieczki. Poprzez wskazanie, że mitochondrialny „zryw mocy” pomaga zabić komórki z mutacją KRAS G12C, oraz że szlaki takie jak mTOR i EMT pozwalają niektórym komórkom ujść, badanie wskazuje konkretne kombinacje leków, które mogą wydłużyć odpowiedzi u pacjentów. W szerszym ujęciu GENEVA oferuje sposób testowania przyszłych leków przeciwnowotworowych w realistycznych, genetycznie zróżnicowanych modelach na długo przed badaniami klinicznymi, zwiększając szanse, że terapie precyzyjne zadziałają u większej liczby osób.
Cytowanie: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Słowa kluczowe: inhibitory KRAS G12C, heterogenność nowotworu, metabolizm mitochondrialny, oporność na leki, terapia skojarzona w onkologii