Clear Sky Science · it
La piattaforma GENEVA modella il mosaico tumorale per rivelare variazioni nelle risposte agli inibitori di KRAS e individuare combinazioni farmacologiche migliori
Perché questo è importante per i futuri trattamenti oncologici
I farmaci oncologici mirati sono progettati per colpire debolezze genetiche specifiche nei tumori, eppure pazienti con tumori apparentemente simili possono rispondere in modo molto diverso. Questo articolo presenta GENEVA, una nuova piattaforma sperimentale che ricrea in laboratorio e nei topi quella diversità del mondo reale, tracciando quindi come migliaia di singole cellule tumorali rispondono al trattamento nel tempo. Così facendo, i ricercatori scoprono perché alcune cellule muoiono, perché altre resistono e come scegliere combinazioni di farmaci più intelligenti che potrebbero impedire al cancro di ripresentarsi.
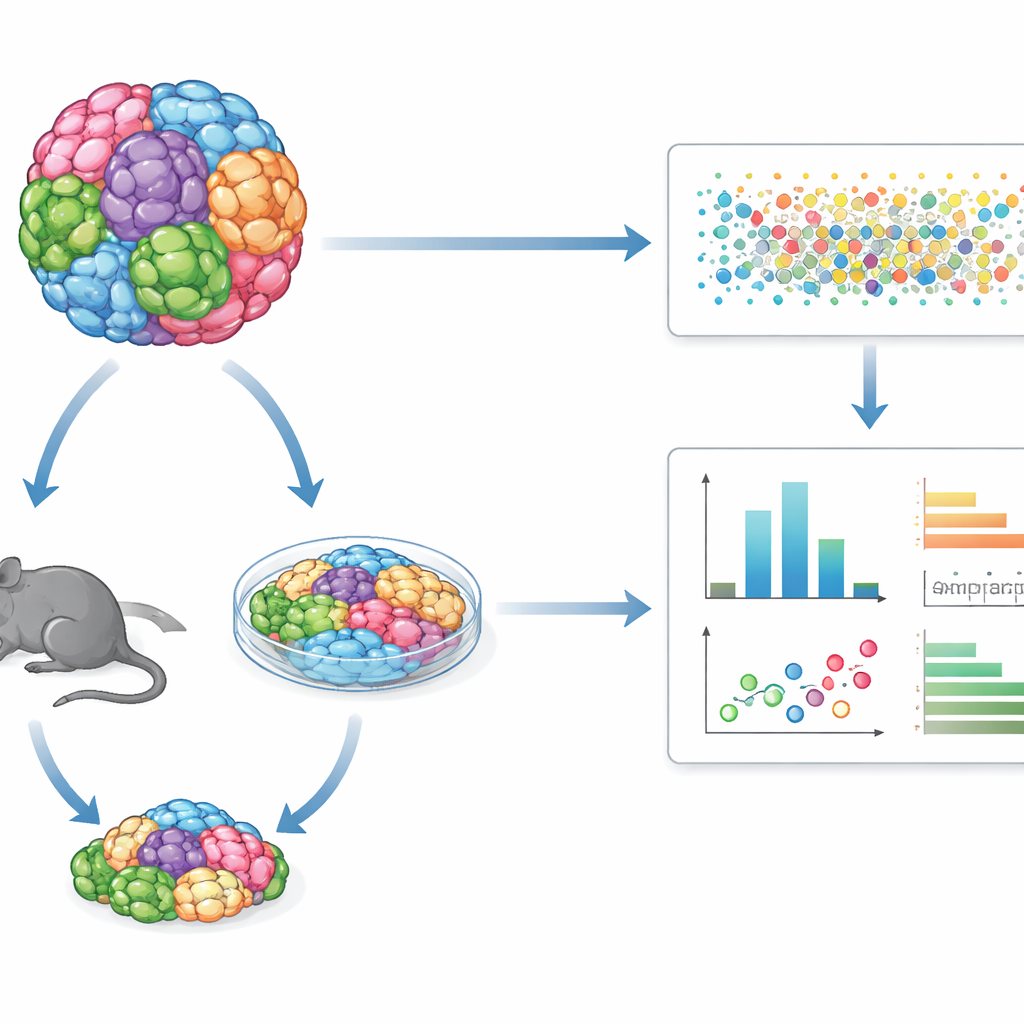
Molti tipi di tumore in un unico test condiviso
Invece di studiare una linea cellulare tumorale alla volta, GENEVA miscela decine di linee cellulari umane geneticamente distinte o campioni tumorali derivati da pazienti in un’unica coltura o tumore “mosaico”. Queste popolazioni miste vengono coltivate sia in colture tridimensionali in laboratorio sia come tumori nei topi. Dopo il trattamento con un farmaco, il team usa il sequenziamento dell’RNA a cellula singola e codici a barre genetici per leggere, cellula per cellula, da quale background genetico proviene ogni cellula e in quale stato molecolare si trova. Questo permette di misurare non solo quante cellule sopravvivono, ma come cambiano i loro programmi interni, rivelando schemi di sensibilità e resistenza attraverso molti tipi tumorali in un unico esperimento.
Esplorare una nuova classe di farmaci che bloccano KRAS
Per dimostrare la potenza di GENEVA, i ricercatori si sono concentrati su un gruppo di farmaci di recente approvazione che bloccano una mutazione oncogenica chiamata KRAS G12C. Questi farmaci hanno portato benefici reali ad alcune persone con tumori polmonari e altri tipi di cancro, ma le risposte sono spesso di breve durata. Usando GENEVA, il team ha messo insieme linee cellulari con e senza la mutazione KRAS e le ha trattate con diversi inibitori di KRAS G12C a varie dosi, sia in piastre che nei topi. Come previsto, le cellule KRAS G12C erano in generale più sensibili, ma anche all’interno di quel gruppo alcune cellule o linee persistevano, suggerendo strategie di sopravvivenza nascoste che gli saggi standard non rileverebbero.
Aumento di attività negli impianti energetici della cellula
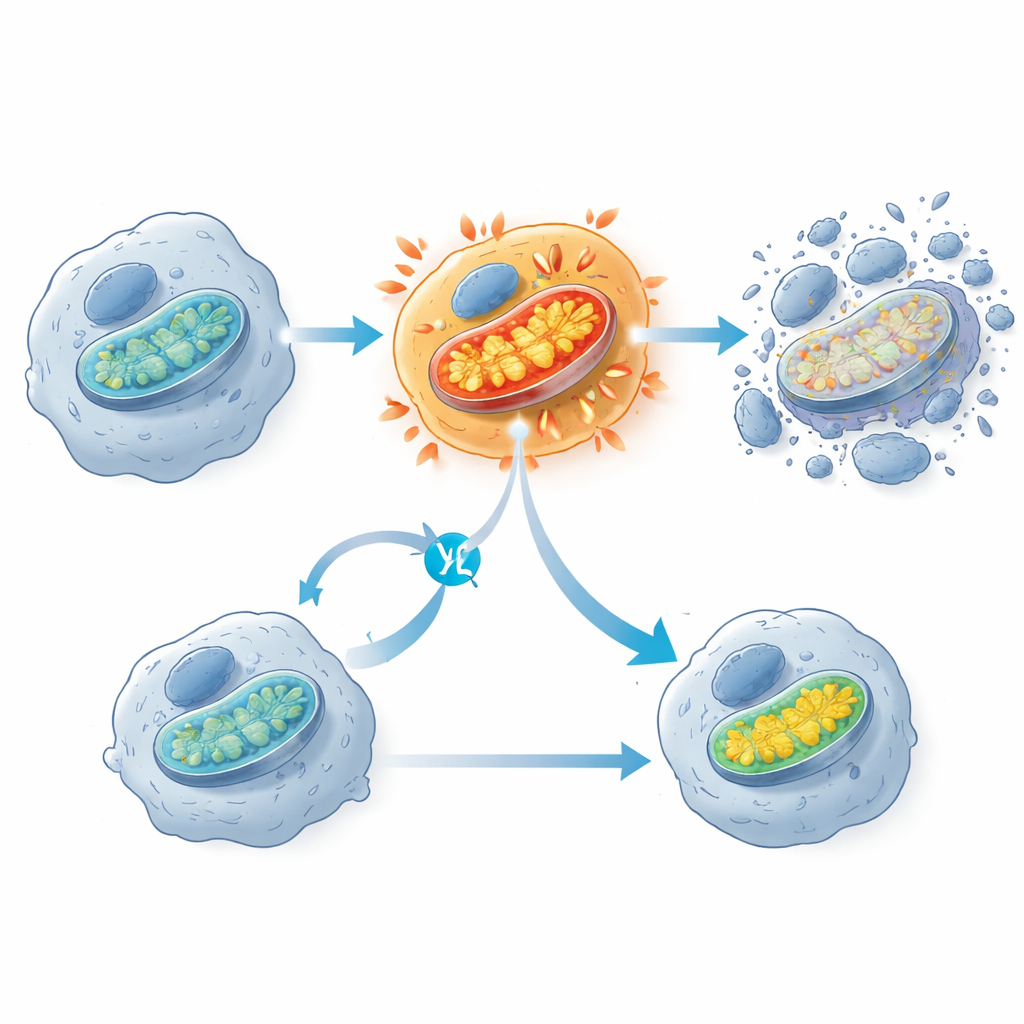
Una scoperta notevole è che gli inibitori di KRAS G12C scatenano un’esplosione precoce di attività nei mitocondri, le strutture spesso descritte come “centrali energetiche” della cellula. Poco dopo l’esposizione al farmaco, le cellule tumorali sensibili mostravano un picco nel consumo di ossigeno e nel potenziale di membrana mitocondriale, seguito alcune ore dopo dall’attivazione di enzimi che portano alla morte cellulare. Le cellule che sopravvivevano al trattamento tendevano ad avere meno componenti mitocondriali e un’attività genica mitocondriale attenuata. Quando i ricercatori hanno parzialmente bloccato la catena di trasporto degli elettroni mitocondriale con un altro farmaco, questo ha effettivamente protetto le cellule con KRAS G12C dalla morte, suggerendo che questa improvvisa sovraattivazione mitocondriale sia un passaggio chiave che spinge le cellule oltre il limite. Il team ha anche osservato segnali di danno ossidativo ai lipidi delle membrane cellulari, ma bloccare questo processo non ha impedito la morte cellulare, indicando che si tratta di un effetto collaterale piuttosto che dell’interruttore principale della morte.
Scoprire rotte di fuga nascoste e abbinamenti migliori
Poiché GENEVA profila migliaia di cellule sopravvissute, può evidenziare geni e vie che sono attivati specificamente nelle cellule tolleranti al farmaco con KRAS G12C. Lo studio ha segnalato diverse di queste rotte, inclusa la segnalazione tramite mTOR, enzimi che modificano l’impacchettamento del DNA e programmi associati a cambiamenti nella forma e nel movimento cellulare noti come transizione epitelio–mesenchimale (EMT). Molte di queste caratteristiche apparivano più marcate nei tumori che crescevano nei topi, dove è presente il microambiente tissutale circostante. Guidato da questi segnali, il team ha testato trattamenti in combinazione. L’abbinamento di un inibitore di KRAS G12C con un inibitore di mTOR o con un bloccante di TGF-β (un promotore dell’EMT) ha prodotto una riduzione tumorale più forte e duratura nei topi rispetto a qualsiasi singolo farmaco da solo.
Dalle singole cellule a terapie di precisione più intelligenti
In termini semplici, questo lavoro mostra che il modo in cui una cellula tumorale gestisce la sua energia e la sua forma può determinare se un farmaco mirato contro KRAS la curerà o soltanto la rallenterà. La piattaforma GENEVA rende possibile osservare queste decisioni dispiegarsi attraverso molti tipi tumorali e condizioni contemporaneamente, rivelando punti deboli comuni e vie di fuga. Identificando che una “sovraattivazione” mitocondriale aiuta a eliminare le cellule con KRAS G12C, e che vie come mTOR ed EMT permettono ad alcune cellule di sfuggire, lo studio indica combinazioni farmacologiche concrete che potrebbero prolungare le risposte nei pazienti. Più in generale, GENEVA offre un modo per testare futuri farmaci oncologici in modelli realistici e geneticamente diversi molto prima delle sperimentazioni cliniche, aumentando le probabilità che le terapie di precisione funzionino per più persone.
Citazione: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Parole chiave: Inibitori di KRAS G12C, eterogeneità tumorale, metabolismo mitocondriale, resistenza ai farmaci, terapia combinata contro il cancro