Clear Sky Science · ar
منصة GENEVA تُحاكي فسيفساء الأورام لتكشف تفاوتات الاستجابة لمثبطات KRAS وتحدد تركيبات دوائية محسنة
لماذا يهم هذا لعلاجات السرطان المستقبلية
تصمم الأدوية المستهدفة للسرطان لضرب نقاط ضعف جينية محددة في الأورام، ومع ذلك قد تستجيب حالات المرضى المصابين بسرطانات تبدو متشابهة بصورة مختلفة تمامًا. يقدم هذا المقال GENEVA، منصة تجريبية جديدة تعيد خلق ذلك التنوع في المختبر وعلى الفئران، ثم تتعقب كيف تستجيب آلاف الخلايا السرطانية الفردية للعلاج مع مرور الوقت. ومن خلال ذلك يكشف الباحثون عن سبب موت بعض الخلايا، ولماذا تصمد أخرى، وكيفية اختيار تراكيب دوائية أذكى قد تمنع الأورام من الارتداد.
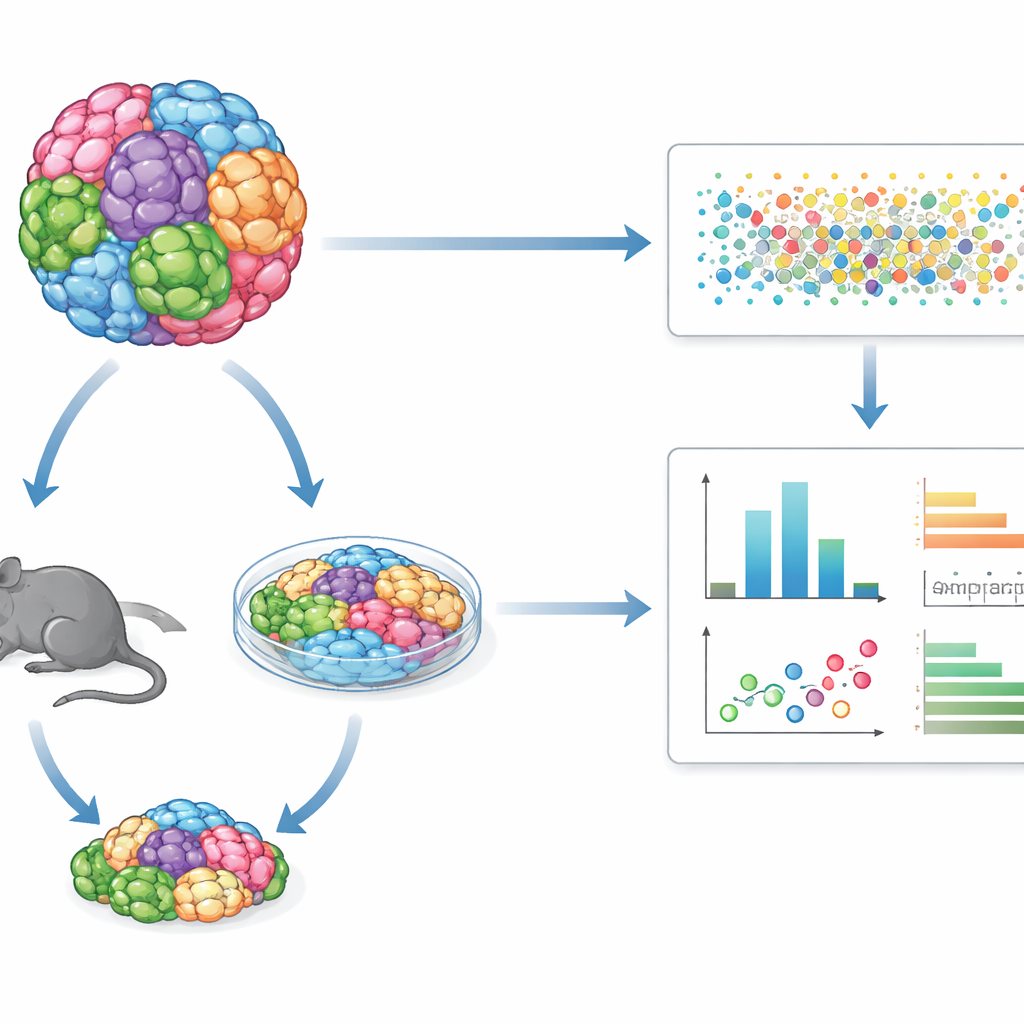
أنواع أورام متعددة في اختبار واحد مشترك
بدلاً من دراسة سطر خلوي سرطاني واحد في كل مرة، تخلط GENEVA عشرات من أسطر الخلايا السرطانية البشرية المتمايزة جينيًا أو عينات أورام مأخوذة من المرضى في مزرعة أو ورم "فسيفسائي" واحد. تزرع هذه التجمعات المختلطة إما في ثقافات ثلاثية الأبعاد في المختبر أو كأورام في الفئران. بعد العلاج بدواء، يستخدم الفريق تسلسل الحمض النووي الريبوزي أحادي الخلية وبطاقات شريطية جينية لقراءة، خليةًا خلية، الخلفية الجينية لكل خلية والحالة الجزيئية التي تكون فيها. هذا يسمح لهم بقياس ليس فقط عدد الخلايا الناجية، بل كيف تتغير برامجها الداخلية، كاشفًا أنماط الحساسية والمقاومة عبر أنواع أورام متعددة في تجربة واحدة.
استكشاف فئة جديدة من الأدوية التي تمنع KRAS
لتوضيح قوة GENEVA، ركز الباحثون على مجموعة أدوية وافقت عليها مؤخرًا وتمنع طفرة تقود السرطان تُدعى KRAS G12C. لقد وفرت هذه الأدوية فوائد حقيقية لبعض الأشخاص المصابين بسرطانات الرئة وأنواع أخرى، لكن الاستجابات غالبًا ما تكون قصيرة الأمد. باستخدام GENEVA، جمع الفريق أسطر خلايا ذات طفرة KRAS وأخرى غير طفرة وعالجها بعدة مثبطات KRAS G12C بجرعات مختلفة، سواء في الأطباق أو في الفئران. كما كان متوقعًا، كانت خلايا KRAS G12C أكثر حساسية عمومًا، لكن حتى داخل تلك المجموعة استمرت بعض الخلايا أو الأسطر، ما ألمح إلى استراتيجيات بقاء كامنة قد تفوتها الفحوص التقليدية.
اندفاع في محطات طاقة الخلية
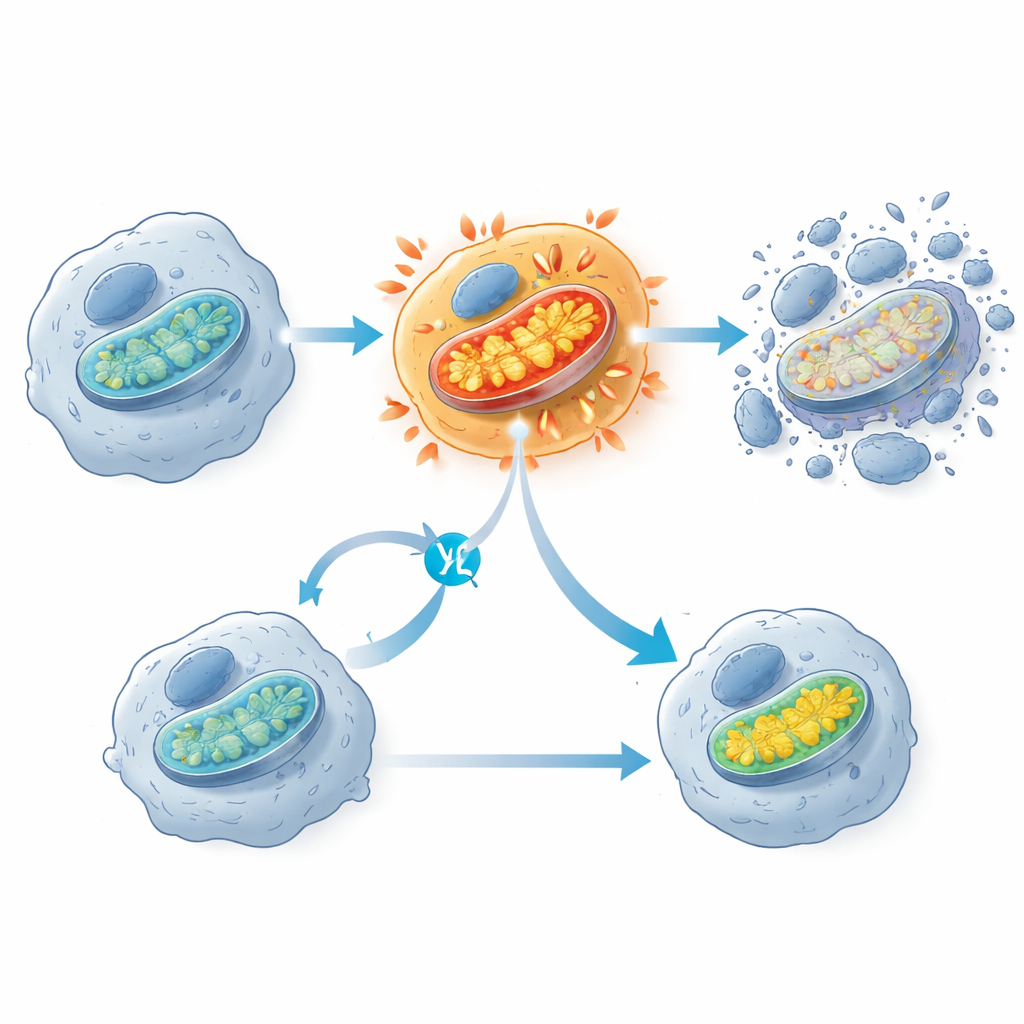
كان من النتائج اللافتة أن مثبطات KRAS G12C تحفز اندفاعًا مبكرًا في نشاط الميتوكوندريا، البُنى التي تُوصف غالبًا بأنها محطات طاقة الخلية. بعد وقت قصير من التعرض للدواء، أظهرت الخلايا السرطانية الحساسة ارتفاعًا في استهلاك الأكسجين وجهد غشاء الميتوكوندريا، تلاه بعد ساعات تنشيط إنزيمات موت الخلايا. الخلايا التي تحملت العلاج كانت تميل إلى امتلاك مكونات ميتوكوندرية أقل ونشاط جيني ميتوكوندري منخفض. عندما قام الباحثون بعرقلة جزئية لسلسلة نقل الإلكترون الميتوكوندرية بدواء آخر، فقد وفر ذلك إحباطًا لخلايا KRAS G12C من الموت، مما يشير إلى أن هذا التسارع الميتوكوندري المفاجئ خطوة أساسية تدفع الخلايا إلى حافة الهاوية. لاحظ الفريق أيضًا علامات تلف تأكسدي للدهون في أغشية الخلايا، لكن حجب هذه العملية لم يَمنع موت الخلايا، دالًا على أنها أثر جانبي وليس آلية القتل الرئيسية.
كشف منافذ فرار خفية وتوافقات أفضل
لأن GENEVA تصف آلاف الخلايا الناجية، فإنها تستطيع إبراز الجينات والمسارات التي تُنشط تحديدًا في خلايا KRAS G12C المتسامحة مع الدواء. أشارت الدراسة إلى عدة مسارات من هذا النوع، بما في ذلك الإشارة عبر mTOR، وإنزيمات تغير تغليف الحمض النووي، وبرامج مرتبطة بتغييرات في شكل الخلية وحركتها المعروفة بالتحول الظهاري-اللحمّي (EMT). ظهرت العديد من هذه الملامح بقوة أكبر في الأورام النامية في الفئران، حيث يتواجد المحيط النسيجي المحيط. استرشادًا بهذه الإشارات، اختبر الفريق علاجات مركبة. أدى اقتران مثبط KRAS G12C مع مثبط mTOR أو مع حاجب لـ TGF-β (محفز EMT) إلى انكماش أقوى وأكثر دوامًا للأورام في الفئران مقارنة بأي دواء منفرد.
من خلية مفردة إلى علاجات دقيقة أذكى
بعبارات بسيطة، تُظهر هذه الدراسة أن كيفية إدارة الخلية السرطانية لطاقةها وشكلها يمكن أن يحدد ما إذا كان دواء KRAS المستهدف سيقضي عليها أو سيبطئها فقط. تجعل منصة GENEVA من الممكن مراقبة هذه القرارات وهي تتكشف عبر أنواع أورام وظروف متعددة في آن واحد، كاشفة نقاط ضعف وطرق هروب شائعة. من خلال تحديد أن "اندفاع الطاقة" الميتوكوندري يساعد في قتل خلايا KRAS G12C، وأن مسارات مثل mTOR وEMT تتيح لبعض الخلايا الفرار، تشير الدراسة إلى تراكيب دوائية ملموسة قد تطيل الاستجابات في المرضى. وعلى نطاق أوسع، توفر GENEVA طريقة لاختبار أدوية السرطان المستقبلية في نماذج واقعية ومتنوعة جينيًا قبل التجارب السريرية بوقت طويل، مما يزيد احتمالات نجاح العلاجات الدقيقة لشريحة أكبر من الناس.
الاستشهاد: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
الكلمات المفتاحية: مثبطات KRAS G12C, تغايرية الأور tumorية, تمثيل غذائي ميitochondrial, مقاومة الأدوية, علاج السرطان بالتراكيب الدوائية