Clear Sky Science · es
La plataforma GENEVA modela el mosaico tumoral para revelar variaciones en las respuestas a inhibidores de KRAS e identificar combinaciones de fármacos mejoradas
Por qué esto importa para los futuros tratamientos contra el cáncer
Los fármacos dirigidos contra el cáncer se diseñan para atacar debilidades genéticas específicas en los tumores, sin embargo pacientes con cánceres aparentemente similares pueden responder de maneras muy diferentes. Este artículo presenta GENEVA, una nueva plataforma experimental que recrea esa diversidad del mundo real en el laboratorio y en ratones, y que luego sigue cómo miles de células cancerosas individuales responden al tratamiento a lo largo del tiempo. Al hacerlo, los investigadores descubren por qué unas células mueren, por qué otras sobreviven y cómo elegir combinaciones de fármacos más inteligentes que podrían evitar que los cánceres reaparezcan.
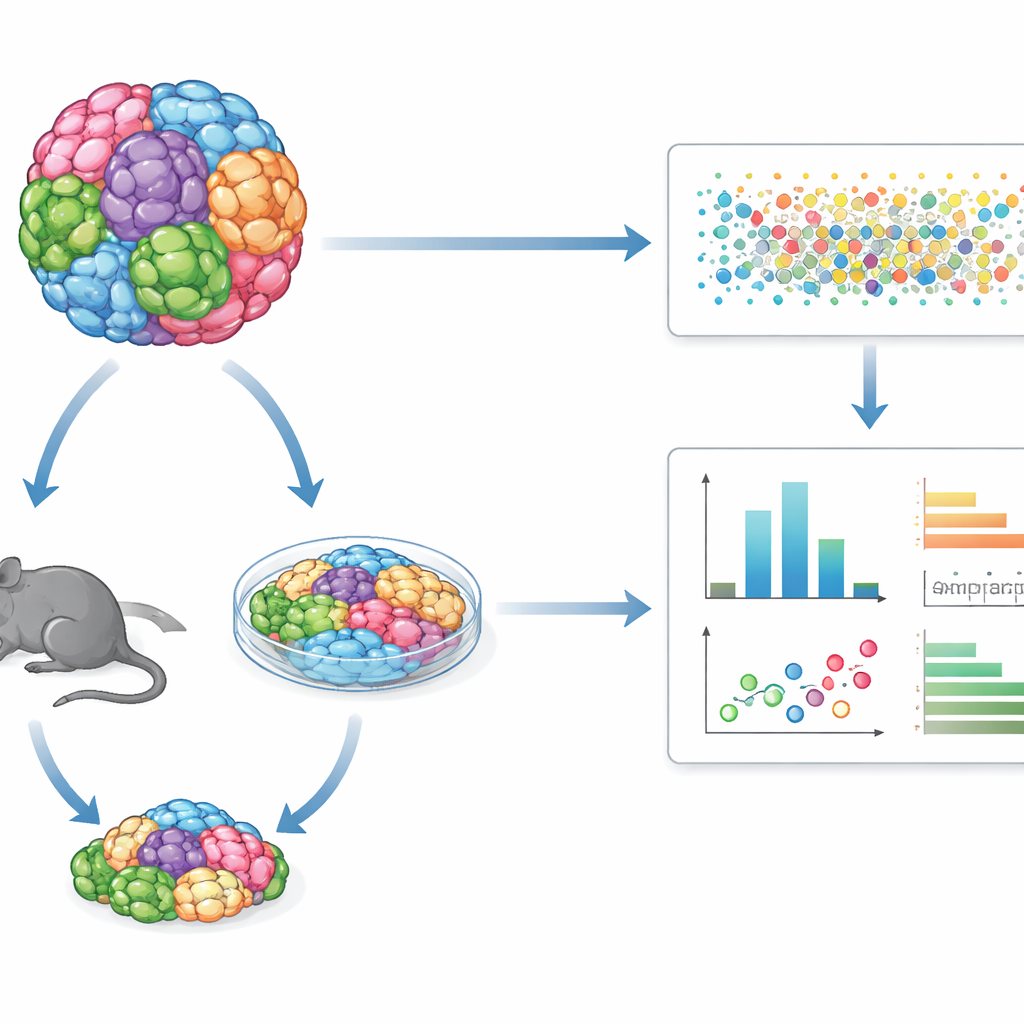
Muchos tipos de tumor en una sola prueba compartida
En lugar de estudiar una línea celular cancerosa a la vez, GENEVA mezcla docenas de líneas celulares humanas genéticamente distintas o muestras tumorales derivadas de pacientes en una sola cultura o tumor “mosaico”. Estas poblaciones mixtas se cultivan ya sea en cultivos tridimensionales o como tumores en ratones. Tras el tratamiento con un fármaco, el equipo utiliza secuenciación de ARN de célula única y códigos de barras genéticos para leer, célula por célula, de qué trasfondo genético procede cada célula y en qué estado molecular se encuentra. Esto les permite medir no solo cuántas células sobreviven, sino cómo cambian sus programas internos, revelando patrones de sensibilidad y resistencia en muchos tipos de tumor en un solo experimento.
Explorando una nueva clase de fármacos que bloquean KRAS
Para mostrar el potencial de GENEVA, los investigadores se centraron en un grupo de fármacos recientemente aprobados que bloquean una mutación impulsora del cáncer llamada KRAS G12C. Estos fármacos han aportado beneficios reales a algunas personas con cáncer de pulmón y otros tumores, pero las respuestas suelen ser de corta duración. Usando GENEVA, el equipo agrupó líneas celulares con y sin la mutación KRAS y las trató con varios inhibidores de KRAS G12C a diferentes dosis, tanto en placas como en ratones. Como era de esperar, las células KRAS G12C fueron generalmente más sensibles, pero incluso dentro de ese grupo algunas células o líneas persistieron, insinuando estrategias de supervivencia ocultas que los ensayos estándar no detectarían.
Subidón de potencia en las centrales energéticas de la célula
Un hallazgo llamativo fue que los inhibidores de KRAS G12C desencadenan una ráfaga temprana de actividad en las mitocondrias, las estructuras que a menudo se describen como las centrales energéticas de la célula. Poco después de la exposición al fármaco, las células cancerosas sensibles mostraron un pico en el consumo de oxígeno y en el potencial de membrana mitocondrial, seguido horas después por la activación de enzimas de muerte celular. Las células que resistieron el tratamiento tendían a tener menos componentes mitocondriales y una actividad génica mitocondrial atenuada. Cuando los investigadores bloquearon parcialmente la cadena de transporte de electrones mitocondrial con otro fármaco, eso protegió en realidad a las células con la mutación KRAS G12C de morir, lo que sugiere que este repentino sobreesfuerzo mitocondrial es un paso clave que lleva a las células al límite. El equipo también observó signos de daños oxidativos en los lípidos de las membranas celulares, pero bloquear este proceso no evitó la muerte celular, lo que indica que es un efecto secundario más que el interruptor principal.
Descubriendo rutas de escape ocultas y mejores emparejamientos
Porque GENEVA perfila miles de células supervivientes, puede destacar genes y vías que se activan específicamente en las células tolerantes al fármaco con KRAS G12C. El estudio señaló varias de estas rutas, incluida la señalización a través de mTOR, enzimas que alteran el empaquetamiento del ADN y programas vinculados a cambios en la forma y el movimiento celular conocidos como transición epitelio–mesénquima (EMT). Muchas de estas características aparecieron con mayor intensidad en los tumores que crecían en ratones, donde está presente el microambiente tisular circundante. Guiado por estas señales, el equipo probó tratamientos combinados. Emparejar un inhibidor de KRAS G12C con un inhibidor de mTOR o con un bloqueador de TGF-β (un impulsor de la EMT) produjo una reducción tumoral más fuerte y duradera en ratones que cualquier fármaco solo.
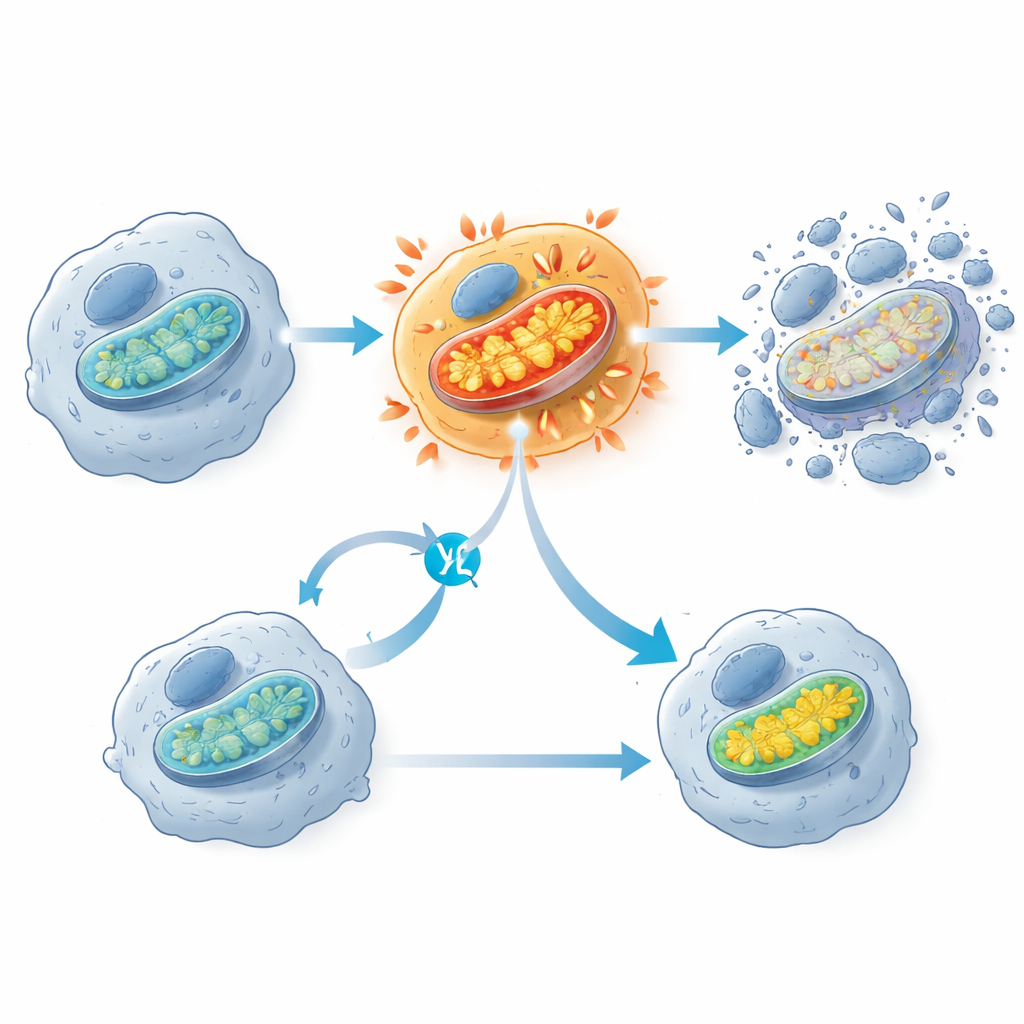
De las células individuales a terapias de precisión más inteligentes
En términos sencillos, este trabajo muestra que la forma en que una célula cancerosa gestiona su energía y su morfología puede dictar si un fármaco dirigido a KRAS la curará o simplemente la ralentizará. La plataforma GENEVA hace posible observar cómo se toman estas decisiones en muchos tipos de tumor y condiciones a la vez, revelando puntos débiles comunes y rutas de escape. Al identificar que un “subidón” mitocondrial ayuda a matar a las células con KRAS G12C, y que vías como mTOR y EMT permiten que algunas células se escapen, el estudio señala combinaciones de fármacos concretas que podrían prolongar las respuestas en los pacientes. Más ampliamente, GENEVA ofrece una manera de probar futuros fármacos contra el cáncer en modelos realistas y genéticamente diversos mucho antes de los ensayos clínicos, aumentando las probabilidades de que las terapias de precisión funcionen para más personas.
Cita: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Palabras clave: Inhibidores de KRAS G12C, Heterogeneidad tumoral, Metabolismo mitocondrial, Resistencia a fármacos, Terapia combinada contra el cáncer