Clear Sky Science · tr
GENEVA platformu tümör mozaisizmini modelleyerek KRAS inhibitörlerine yanıtlardaki farklılıkları ortaya koyuyor ve geliştirilmiş ilaç kombinasyonlarını tanımlıyor
Gelecekteki kanser tedavileri için bunun önemi
Hedefe yönelik kanser ilaçları, tümörlerdeki belirli genetik zaafları hedef almak üzere tasarlanır; ancak görünüşte benzer kanserlere sahip hastalar çok farklı yanıtlar verebilir. Bu makale, gerçek dünyadaki bu çeşitliliği laboratuvarda ve fare modellerinde yeniden yaratan ve binlerce bireysel kanser hücresinin tedaviye zaman içinde nasıl yanıt verdiğini izleyen yeni bir deneysel platform olan GENEVA’yı tanıtıyor. Araştırmacılar böylece bazı hücrelerin neden öldüğünü, bazılarının neden dayanabildiğini ve kanserlerin geri sıçramasını önleyebilecek daha akıllı ilaç kombinasyonlarının nasıl seçileceğini ortaya koyuyor.
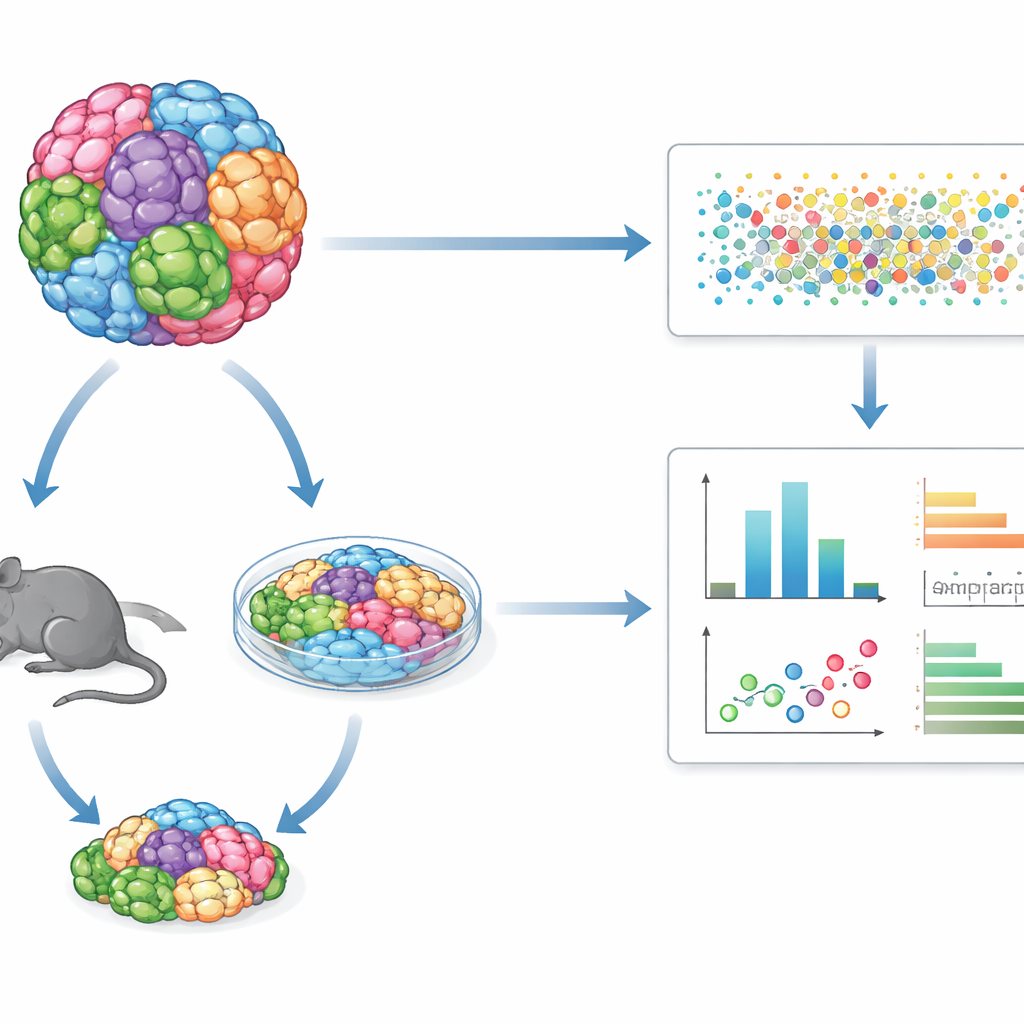
Tek bir ortak testte birçok tümör tipi
Bir kanser hücre hattını tek tek incelemek yerine GENEVA, onlarca genetik olarak farklı insan kanser hücre hattını veya hastadan türetilmiş tümör örneklerini tek bir “mozaik” kültür veya tümörde karıştırır. Bu karışık popülasyonlar ya üç boyutlu laboratuvar kültürlerinde ya da farelerde tümör olarak büyütülür. Bir ilaçla tedaviden sonra ekip, hücre hücre hangi genetik arka plandan geldiğini ve hangi moleküler durumda olduğunu okumak için tek hücre RNA sekanslaması ve genetik barkodlar kullanır. Bu, yalnızca kaç hücrenin sağ kaldığını ölçmelerine değil, aynı zamanda hücrelerin iç programlarının nasıl değiştiğini görmelerine olanak sağlar; böylece bir deneyde birçok tümör tipi arasında hassasiyet ve direnç desenleri açığa çıkar.
KRAS’ı engelleyen yeni bir ilaç sınıfını incelemek
GENEVA’nın gücünü göstermek için araştırmacılar, KRAS G12C adı verilen kanser sürükleyici bir mutasyonu engelleyen yakın zamanda onaylanmış bir ilaç grubuna odaklandı. Bu ilaçlar bazı akciğer ve diğer kanser hastalarına gerçek fayda sağladı, ancak yanıtlar genellikle kısa ömürlü oluyor. GENEVA kullanılarak ekip, KRAS-mutant ve mutant olmayan hücre hatlarını karıştırdı ve bunları hem plaklarda hem de farelerde farklı dozlarda birden fazla KRAS G12C inhibitörü ile tedavi etti. Beklendiği üzere KRAS G12C hücreleri genel olarak daha duyarlıydı, ancak bu grup içinde bile bazı hücreler veya hatlar kalıcı oldu; bu da standart testlerin kaçıracağı gizli hayatta kalma stratejilerine işaret ediyor.
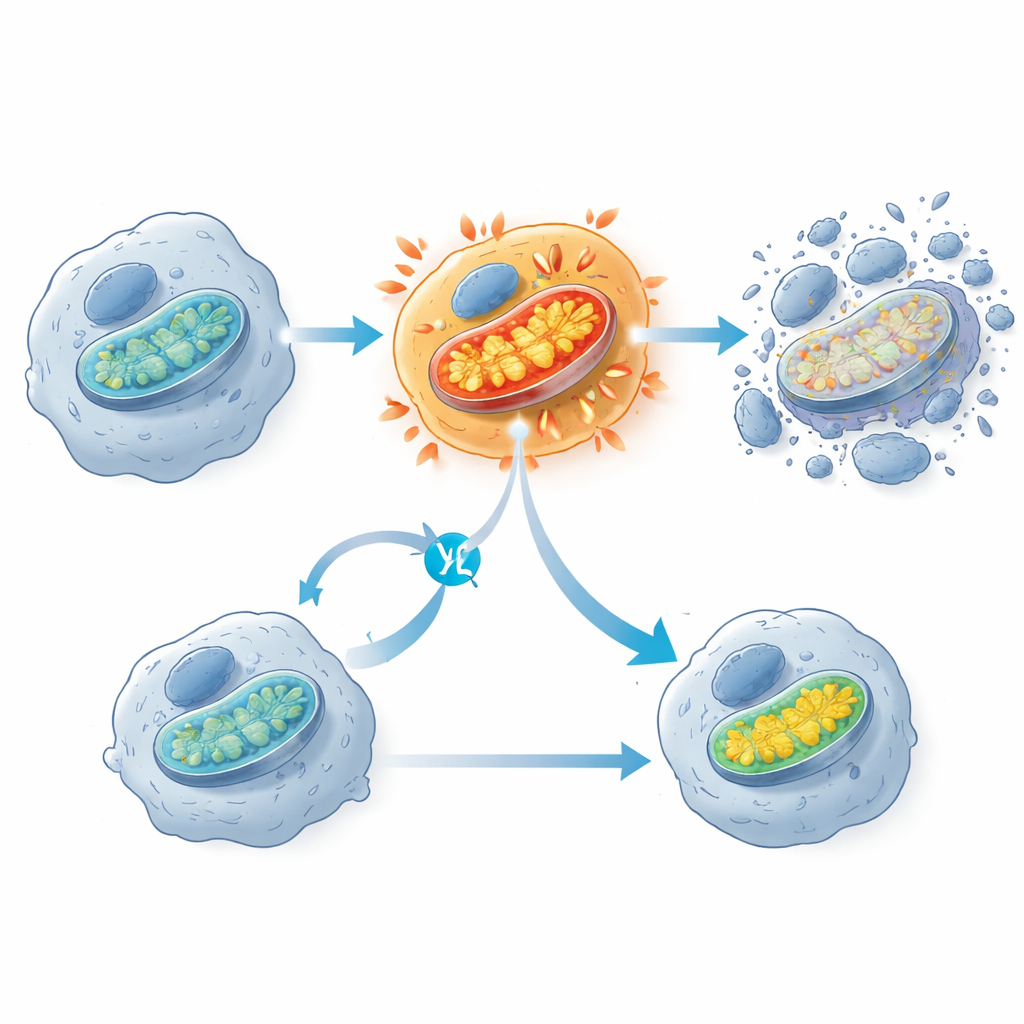
Hücresel enerji santrallerinde güç patlaması
Çarpıcı bir bulgu, KRAS G12C inhibitörlerinin mitokondrilerde erken bir aktivite patlaması tetiklemesiydi; mitokondriler genellikle hücrenin enerji santralleri olarak tanımlanır. İlaç maruziyetinin hemen ardından duyarlı kanser hücreleri oksijen tüketiminde ve mitokondriyal membran potansiyelinde bir sıçrama gösterdi; bunu birkaç saat sonra hücre ölümü enzimlerinin aktive olması izledi. Tedaviyi atlatan hücrelerde genellikle daha az mitokondri bileşeni ve baskılanmış mitokondri gen aktivitesi vardı. Araştırmacılar mitokondriyal oksit taşıma zincirini kısmen başka bir ilaçla bloke ettiklerinde, bunun KRAS G12C-mutant hücreleri öldürmekten koruduğunu gözlemlediler; bu, bu ani mitokondriyal aşırı aktivitenin hücreleri yok olma eşiğinin ötesine iten kilit bir adım olduğunu düşündürüyor. Ekip ayrıca hücre zarlarındaki yağlarda oksidatif hasar belirtileri gördü, ancak bu süreci engellemenin hücre ölümünü önlemediği, yani bunun ana öldürücü mekanizma değil yan etki olduğu görüldü.
Gizli kaçış yollarını ve daha iyi eşleştirmeleri açığa çıkarmak
GENEVA binlerce hayatta kalan hücreyi profilleyebildiği için, ilaç toleranslı KRAS G12C hücrelerinde özellikle açılan genleri ve yolları vurgulayabiliyor. Çalışma, mTOR aracılığıyla sinyal iletimini, DNA paketlemesini değiştiren enzimleri ve epitel–mezenkimal geçiş (EMT) olarak bilinen hücre şekli ve hareketindeki değişimlerle bağlantılı programları içeren birkaç yolu işaret etti. Bu özelliklerin birçoğu, çevreleyen doku mikroçevresinin bulunduğu farelerde büyüyen tümörlerde en belirgin şekilde ortaya çıktı. Bu sinyaller doğrultusunda ekip kombinasyon tedavilerini test etti. Bir KRAS G12C inhibitörünü mTOR inhibitörü veya EMT’yi tetikleyen TGF-β bloklayıcı ile eşleştirmek, farelerde tek başına herhangi bir ilaçtan daha güçlü ve daha kalıcı tümör küçülmesi sağladı.
Tek hücrelerden daha akıllı hedefe yönelik terapilere
Daha açık bir ifadeyle, bu çalışma bir kanser hücresinin enerjisini ve şeklini nasıl yönettiğinin, hedefe yönelik bir KRAS ilacının onu tedavi edip etmeyeceğini veya sadece büyümesini yavaşlatıp yavaşlatmayacağını belirleyebileceğini gösteriyor. GENEVA platformu, bu kararların birçok tümör tipi ve koşulda aynı anda nasıl şekillendiğini izlemeyi mümkün kılarak ortak zayıf noktaları ve kaçış yollarını ortaya çıkarıyor. Mitokondriyal bir “güç patlamasının” KRAS G12C-mutant hücreleri öldürmeye yardımcı olduğunu ve mTOR ile EMT gibi yolların bazı hücrelerin kaçmasını sağladığını belirleyerek çalışma, hastalarda yanıtları uzatabilecek somut ilaç kombinasyonlarına işaret ediyor. Daha geniş anlamda GENEVA, klinik denemelerden çok önce gerçekçi, genetik olarak çeşitli modellerde gelecekteki kanser ilaçlarını test etme yolu sunarak hedefe yönelik terapilerin daha fazla kişi için işe yaraması olasılığını artırıyor.
Atıf: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Anahtar kelimeler: KRAS G12C inhibitörleri, tümör heterojenitesi, mitokondriyal metabolizma, ilaç direnci, kombinasyon kanser terapisi