Clear Sky Science · nl
Het GENEVA-platform modelleert tumor-mosaicisme om variaties in reacties op KRAS-remmers te onthullen en verbeterde medicijncombinaties te identificeren
Waarom dit belangrijk is voor toekomstige kankerbehandelingen
Gerichte kankertherapieën zijn ontworpen om specifieke genetische zwaktes in tumoren aan te pakken, maar patiënten met ogenschijnlijk vergelijkbare kankers kunnen zeer verschillend reageren. Dit artikel introduceert GENEVA, een nieuw experimenteel platform dat die reële diversiteit in het laboratorium en in muizen nabootst en vervolgens bijhoudt hoe duizenden individuele kankercellen in de loop van de tijd op behandeling reageren. Daarmee onthullen de onderzoekers waarom sommige cellen sterven, waarom andere blijven bestaan, en hoe je slimmere medicijncombinaties kunt kiezen die kunnen voorkomen dat kankers terugveren.
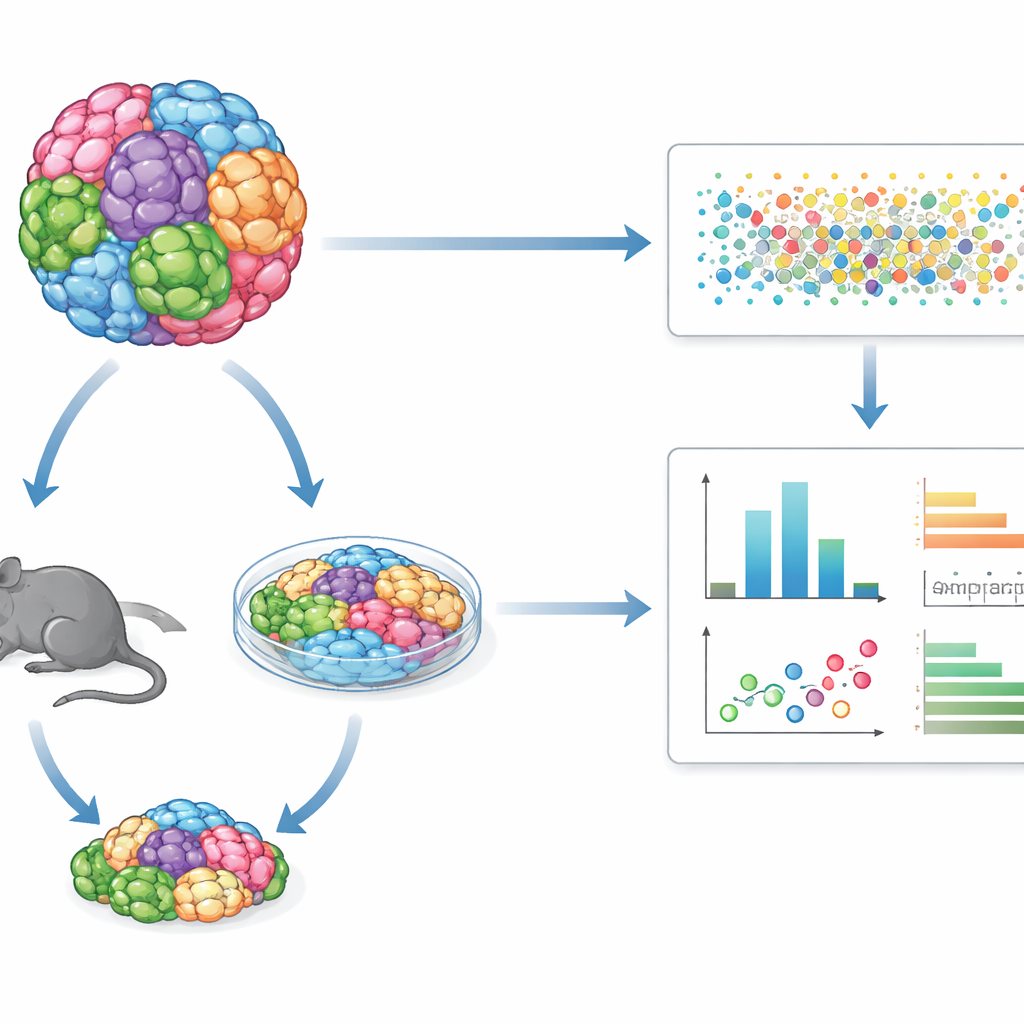
Veel tumorsoorten in één gedeelde test
In plaats van één kankercellijn tegelijk te bestuderen, mixt GENEVA tientallen genetisch verschillende menselijke kankercellijnen of patiënt-afgeleide tumormonsters in één enkele “mozaïek” kweek of tumor. Deze gemengde populaties worden gekweekt in driedimensionale labkweken of als tumoren in muizen. Na behandeling met een medicijn gebruiken de onderzoekers enkelvoudige-cel RNA-sequencing en genetische barcodes om per cel uit te lezen uit welke genetische achtergrond die cel afkomstig is en in welke moleculaire toestand zij verkeert. Dit stelt hen in staat niet alleen te meten hoeveel cellen overleven, maar ook hoe hun interne programma’s veranderen, waardoor patronen van gevoeligheid en resistentie over veel tumorsoorten in één enkel experiment zichtbaar worden.
Onderzoek naar een nieuwe klasse KRAS-blokkers
Om de kracht van GENEVA te demonstreren richtten de onderzoekers zich op een recent goedgekeurde groep medicijnen die een kankeraanjagende mutatie genaamd KRAS G12C blokkeren. Deze medicijnen hebben voor sommige mensen met long- en andere kankers echte voordelen gebracht, maar de reacties zijn vaak van korte duur. Met GENEVA poolde het team KRAS-mutante en niet-mutante cellijnen en behandelde ze met meerdere KRAS G12C-remmers in verschillende doses, zowel in kweekplaten als in muizen. Zoals verwacht waren KRAS G12C-cellen over het algemeen gevoeliger, maar zelfs binnen die groep bleven sommige cellen of lijnen bestaan, wat wijst op verborgen overlevingsstrategieën die standaardtests zouden missen.
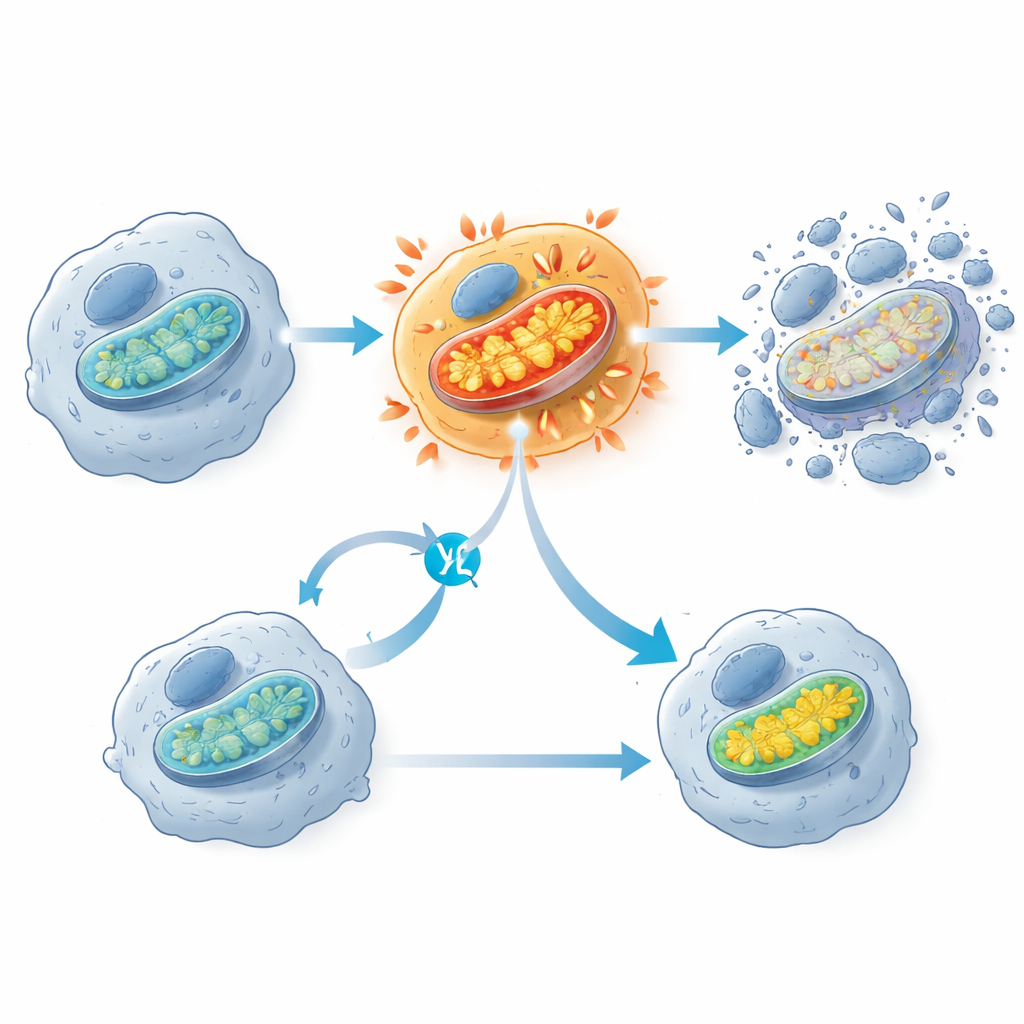
Energietoename in de energiefabriekjes van de cel
Een opvallende bevinding was dat KRAS G12C-remmers een vroege toename van activiteit in mitochondriën teweegbrengen, de structuren die vaak als de energiefabriekjes van de cel worden beschreven. Kort na blootstelling aan het medicijn lieten gevoelige kankercellen een piek zien in zuurstofverbruik en mitochondriale membraanpotentiaal, gevolgd enkele uren later door activatie van celdoodenzymen. Cellen die de behandeling doorstonden, hadden vaak minder mitochondriale componenten en een gedempte mitochondriale genactiviteit. Toen de onderzoekers de mitochondriale elektronentransportketen gedeeltelijk blokkeerden met een ander medicijn, beschermde dat KRAS G12C-mutante cellen juist tegen celdood, wat erop wijst dat deze plotselinge mitochondriale overdrive een cruciale stap is die cellen over de rand duwt. Het team zag ook aanwijzingen voor oxidatieve schade aan vetten in celmembranen, maar het blokkeren van dit proces verhinderde de celdood niet, wat aangeeft dat het een bijeffect is en niet de hoofdschakel voor doding.
Verborgen ontsnappingsroutes en betere combinaties onthullen
Omdat GENEVA duizenden overlevende cellen profiled, kan het genen en routes aanwijzen die specifiek zijn opgevoerd in medicijntolerante KRAS G12C-cellen. De studie markeerde verschillende dergelijke routes, waaronder signalering via mTOR, enzymen die DNA-verpakking aanpassen, en programma’s gekoppeld aan veranderingen in celvorm en -beweging bekend als epitheliaal–mesenchymale transitie (EMT). Veel van deze kenmerken verschenen het sterkst in tumoren die in muizen groeiden, waar de omliggende weefsel-microomgeving aanwezig is. Geleid door deze signalen testte het team combinatietherapieën. Het combineren van een KRAS G12C-remmer met een mTOR-remmer of met een remmer van TGF-β (een aanjager van EMT) gaf sterkere en duurzamere tumorkrimping in muizen dan welk enkelvoudig medicijn dan ook.
Van individuele cellen naar slimmere precisietherapieën
In eenvoudige bewoordingen laat dit werk zien dat hoe een kankercel haar energie en vorm beheert kan bepalen of een gerichte KRAS-remmer de cel uitroeit of slechts vertraagt. Het GENEVA-platform maakt het mogelijk om deze beslissingen tegelijk in veel tumorsoorten en -omstandigheden te observeren en gemeenschappelijke zwakke plekken en ontsnappingsroutes bloot te leggen. Door te identificeren dat een mitochondriale “energietoename” helpt bij het doden van KRAS G12C-mutante cellen, en dat routes zoals mTOR en EMT het sommige cellen mogelijk maken te ontsnappen, wijst de studie op concrete medicijncombinaties die reacties bij patiënten kunnen verlengen. Breder gezien biedt GENEVA een manier om toekomstige kankermedicijnen te testen in realistische, genetisch diverse modellen lang voordat klinische proeven plaatsvinden, wat de kans vergroot dat precisietherapieën voor meer mensen werken.
Bronvermelding: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Trefwoorden: KRAS G12C-remmers, tumorheterogeniteit, mitochondriaal metabolisme, medicijnresistentie, combinatietherapie bij kanker