Clear Sky Science · fr
La plateforme GENEVA modélise le mosaïcisme tumoral pour révéler les variations de réponse aux inhibiteurs de KRAS et identifier de meilleures associations médicamenteuses
Pourquoi cela compte pour les traitements du cancer à venir
Les médicaments ciblés contre le cancer sont conçus pour exploiter des faiblesses génétiques spécifiques des tumeurs, et pourtant des patients présentant des cancers apparemment similaires peuvent réagir très différemment. Cet article présente GENEVA, une nouvelle plateforme expérimentale qui recrée cette diversité du monde réel en laboratoire et chez la souris, puis suit la réponse de milliers de cellules cancéreuses individuelles au traitement au fil du temps. Ce faisant, les chercheurs mettent au jour pourquoi certaines cellules meurent, pourquoi d’autres survivent, et comment choisir des combinaisons médicamenteuses plus intelligentes susceptibles d’empêcher les cancers de repousser.
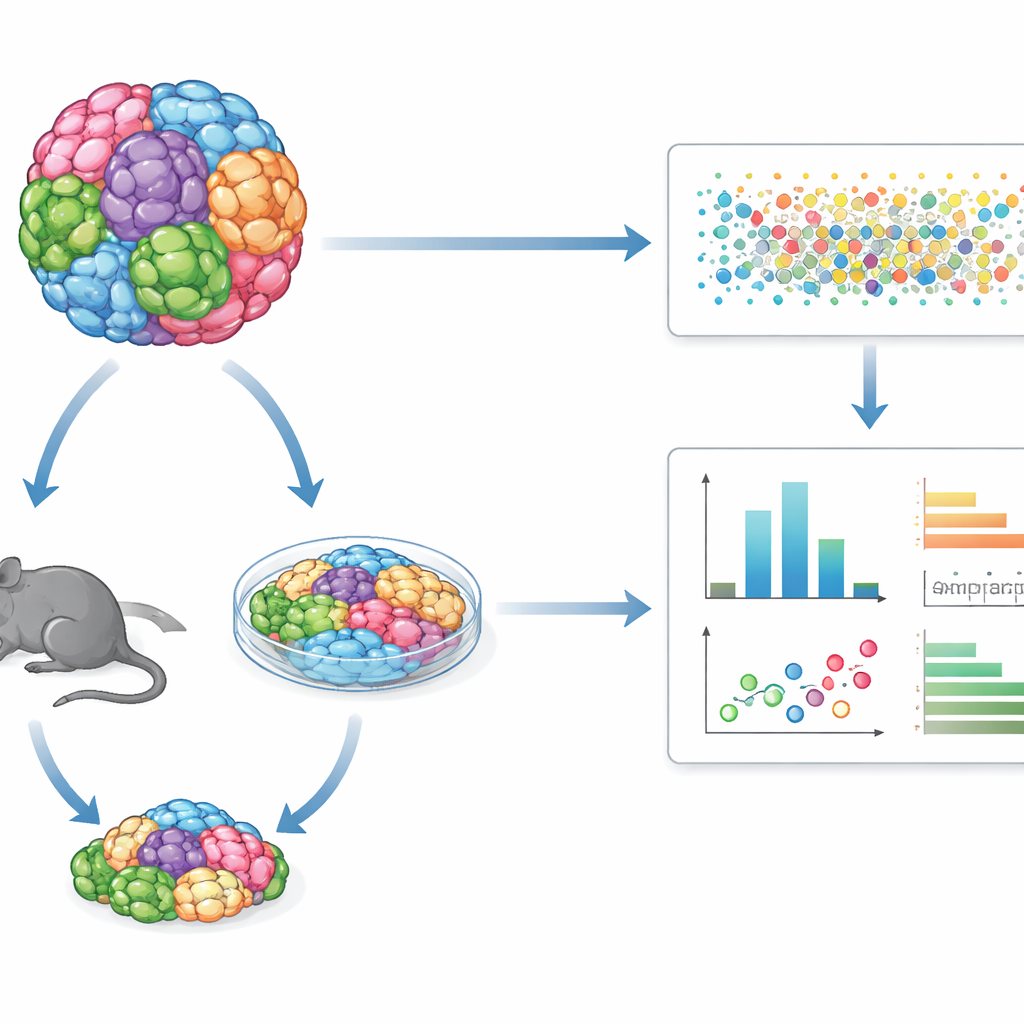
De nombreux types tumoraux dans un même essai partagé
Plutôt que d’étudier une lignée cellulaire cancéreuse à la fois, GENEVA mélange des dizaines de lignées cellulaires humaines génétiquement distinctes ou des échantillons tumoraux dérivés de patients dans une seule culture ou tumeur « mosaïque ». Ces populations mixtes sont cultivées soit en cultures tridimensionnelles en laboratoire, soit comme tumeurs chez la souris. Après traitement par un médicament, l’équipe utilise le séquençage ARN unicellulaire et des codes-barres génétiques pour lire, cellule par cellule, l’origine génétique de chaque cellule et son état moléculaire. Cela leur permet de mesurer non seulement combien de cellules survivent, mais comment leurs programmes internes changent, révélant des schémas de sensibilité et de résistance à travers de nombreux types tumoraux dans une même expérience.
Explorer une nouvelle classe de médicaments bloquant KRAS
Pour démontrer la puissance de GENEVA, les chercheurs se sont concentrés sur un groupe de médicaments récemment approuvés qui bloquent une mutation oncogène appelée KRAS G12C. Ces médicaments ont apporté des bénéfices réels pour certains patients atteints de cancers du poumon et d’autres tumeurs, mais les réponses sont souvent de courte durée. En utilisant GENEVA, l’équipe a poolé des lignées mutées pour KRAS et non mutées et les a traitées avec plusieurs inhibiteurs de KRAS G12C à différentes doses, à la fois en culture et chez la souris. Comme prévu, les cellules KRAS G12C étaient généralement plus sensibles, mais même au sein de ce groupe certaines cellules ou lignées ont persisté, suggérant des stratégies de survie cachées que les tests standard auraient manquées.
Poussée d’activité dans les centrales énergétiques de la cellule
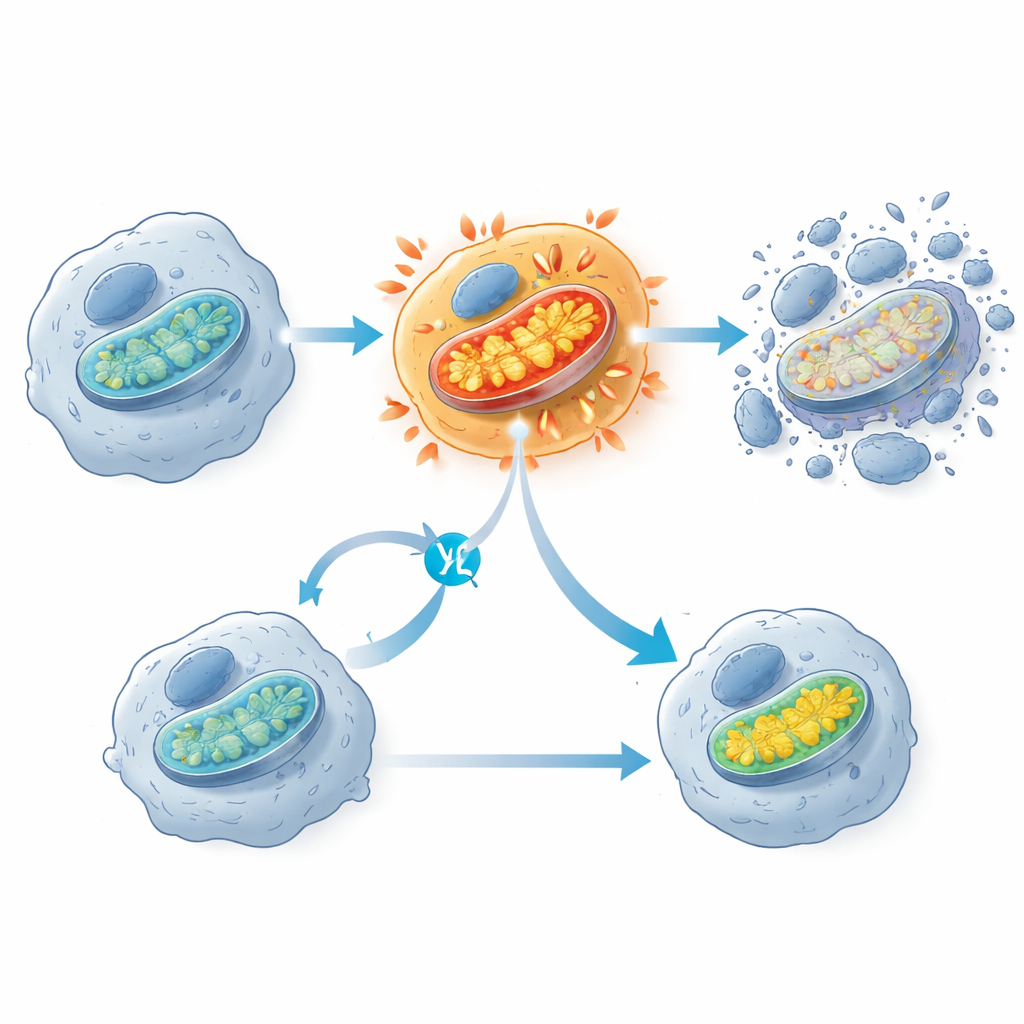
Une observation marquante est que les inhibiteurs de KRAS G12C déclenchent une poussée précoce d’activité mitochodnriale (mitochondriale), les structures souvent décrites comme les centrales énergétiques de la cellule. Peu après l’exposition au médicament, les cellules cancéreuses sensibles ont montré un pic de consommation d’oxygène et de potentiel de membrane mitochondrial, suivi quelques heures plus tard par l’activation d’enzymes responsables de la mort cellulaire. Les cellules qui ont supporté le traitement avaient tendance à présenter moins de composants mitochondriaux et une activité génique mitochondriale atténuée. Lorsque les chercheurs ont partiellement bloqué la chaîne de transport d’électrons mitochondriale avec un autre médicament, cela a en réalité protégé les cellules mutées KRAS G12C de la mort, suggérant que cette suractivité mitochondriale soudaine est une étape clé qui pousse les cellules au-delà du seuil. L’équipe a aussi observé des signes de dommages oxydatifs aux lipides des membranes cellulaires, mais le blocage de ce processus n’a pas empêché la mort cellulaire, indiquant qu’il s’agit d’un effet secondaire plutôt que du principal déclencheur.
Déceler des voies d’échappement cachées et de meilleures associations
Parce que GENEVA profile des milliers de cellules survivantes, elle peut mettre en évidence des gènes et des voies activés spécifiquement dans les cellules tolérantes au médicament KRAS G12C. L’étude a identifié plusieurs de ces voies, notamment la signalisation via mTOR, des enzymes qui modifient le compactage de l’ADN, et des programmes liés aux changements de forme et de motilité cellulaire connus sous le nom de transition épithélio–mésenchymateuse (EMT). Nombre de ces caractéristiques sont apparues de façon plus marquée dans les tumeurs croissant chez la souris, où le microenvironnement tissulaire est présent. Guidée par ces signaux, l’équipe a testé des traitements combinés. Associer un inhibiteur de KRAS G12C à un inhibiteur de mTOR ou à un bloqueur de la TGF-β (un moteur de l’EMT) a produit une réduction tumorale plus forte et plus durable chez la souris que n’importe quel médicament seul.
Des cellules individuelles à des thérapies de précision plus intelligentes
En termes simples, ce travail montre que la façon dont une cellule cancéreuse gère son énergie et sa forme peut déterminer si un médicament ciblant KRAS la guérira ou se contentera de la ralentir. La plateforme GENEVA permet d’observer ces décisions se dérouler simultanément à travers de nombreux types tumoraux et conditions, révélant des points faibles et des voies d’échappement communs. En identifiant qu’une « poussée » mitochondriale aide à tuer les cellules porteuses de KRAS G12C, et que des voies comme mTOR et l’EMT permettent à certaines cellules de s’échapper, l’étude indique des combinaisons médicamenteuses concrètes susceptibles de prolonger les réponses chez les patients. Plus largement, GENEVA offre un moyen de tester de futurs médicaments anticancéreux dans des modèles réalistes et génétiquement divers bien avant les essais cliniques, augmentant les chances que les thérapies de précision fonctionnent pour un plus grand nombre de personnes.
Citation: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Mots-clés: Inhibiteurs KRAS G12C, hétérogénéité tumorale, métabolisme mitochondrial, résistance aux médicaments, thérapie combinée contre le cancer