Clear Sky Science · pt
A plataforma GENEVA modela o mosaico tumoral para revelar variações nas respostas aos inibidores de KRAS e identificar combinações de drogas aprimoradas
Por que isso importa para tratamentos futuros do câncer
Medicamentos direcionados contra o câncer são projetados para atacar fraquezas genéticas específicas nos tumores, mas pacientes com cânceres aparentemente semelhantes podem responder de maneiras muito diferentes. Este artigo apresenta o GENEVA, uma nova plataforma experimental que recria essa diversidade do mundo real em laboratório e em camundongos, e então monitora como milhares de células cancerosas individuais respondem ao tratamento ao longo do tempo. Ao fazer isso, os pesquisadores revelam por que algumas células morrem, por que outras persistem e como escolher combinações de drogas mais inteligentes que poderiam impedir que os cânceres retornem.
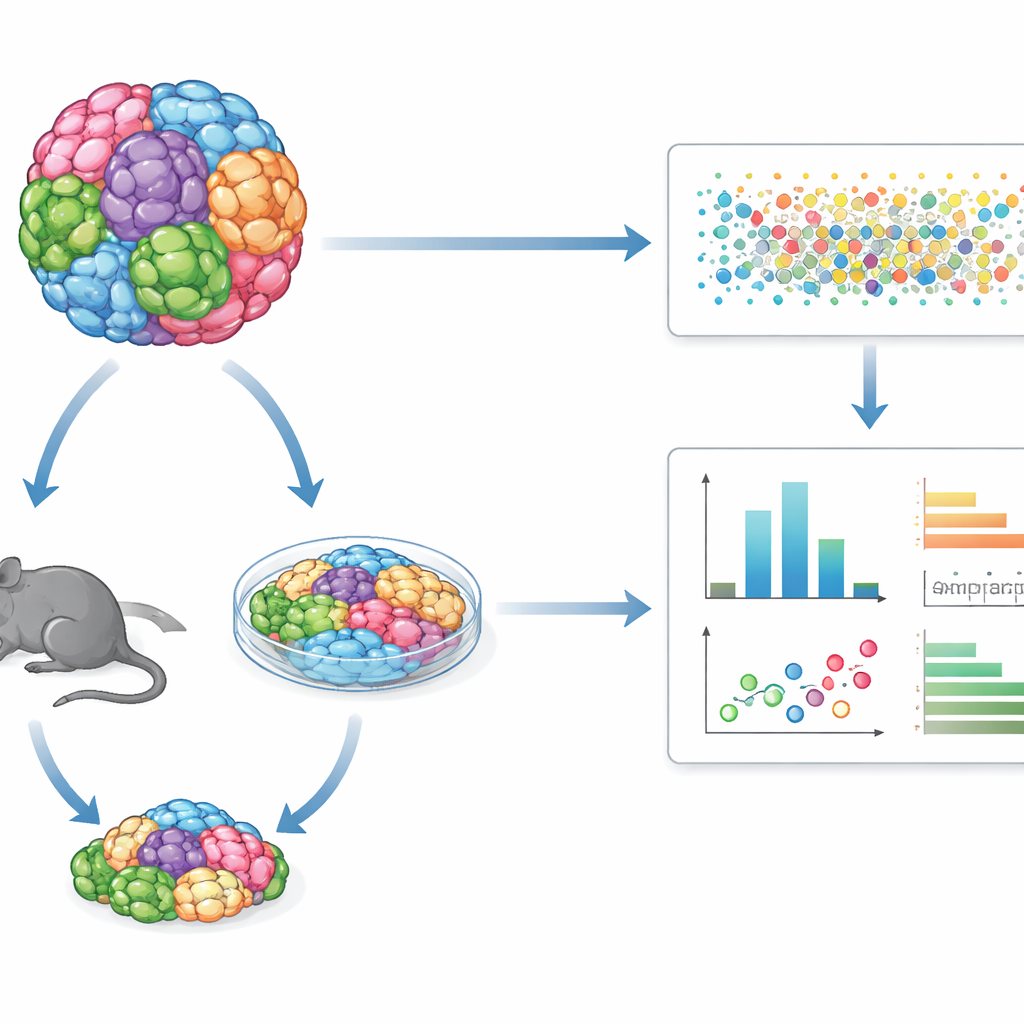
Muitos tipos de tumor em um único teste compartilhado
Em vez de estudar uma linha de células cancerosas por vez, o GENEVA mistura dezenas de linhas celulares humanas geneticamente distintas ou amostras tumorais derivadas de pacientes em uma única cultura ou tumor “mosaico”. Essas populações mistas são cultivadas tanto em culturas tridimensionais no laboratório quanto como tumores em camundongos. Após o tratamento com um fármaco, a equipe usa sequenciamento de RNA de célula única e códigos genéticos (barcodes) para identificar, célula a célula, de que fundo genético cada célula veio e em que estado molecular ela se encontra. Isso permite medir não apenas quantas células sobrevivem, mas como seus programas internos mudam, revelando padrões de sensibilidade e resistência através de muitos tipos tumorais em um único experimento.
Investigando uma nova classe de drogas que bloqueiam KRAS
Para demonstrar o poder do GENEVA, os pesquisadores se concentraram em um grupo recentemente aprovado de fármacos que bloqueiam uma mutação oncogênica chamada KRAS G12C. Essas drogas trouxeram benefícios reais para algumas pessoas com câncer de pulmão e outros tipos, mas as respostas costumam ser de curta duração. Usando o GENEVA, a equipe agrupou linhas com mutação em KRAS e linhas não mutantes e as tratou com vários inibidores de KRAS G12C em diferentes doses, tanto em placas quanto em camundongos. Como esperado, células com KRAS G12C foram, em geral, mais sensíveis, mas mesmo dentro desse grupo algumas células ou linhas persistiram, sugerindo estratégias de sobrevivência ocultas que ensaios padrão não detectariam.
Surto de energia nas usinas de força da célula
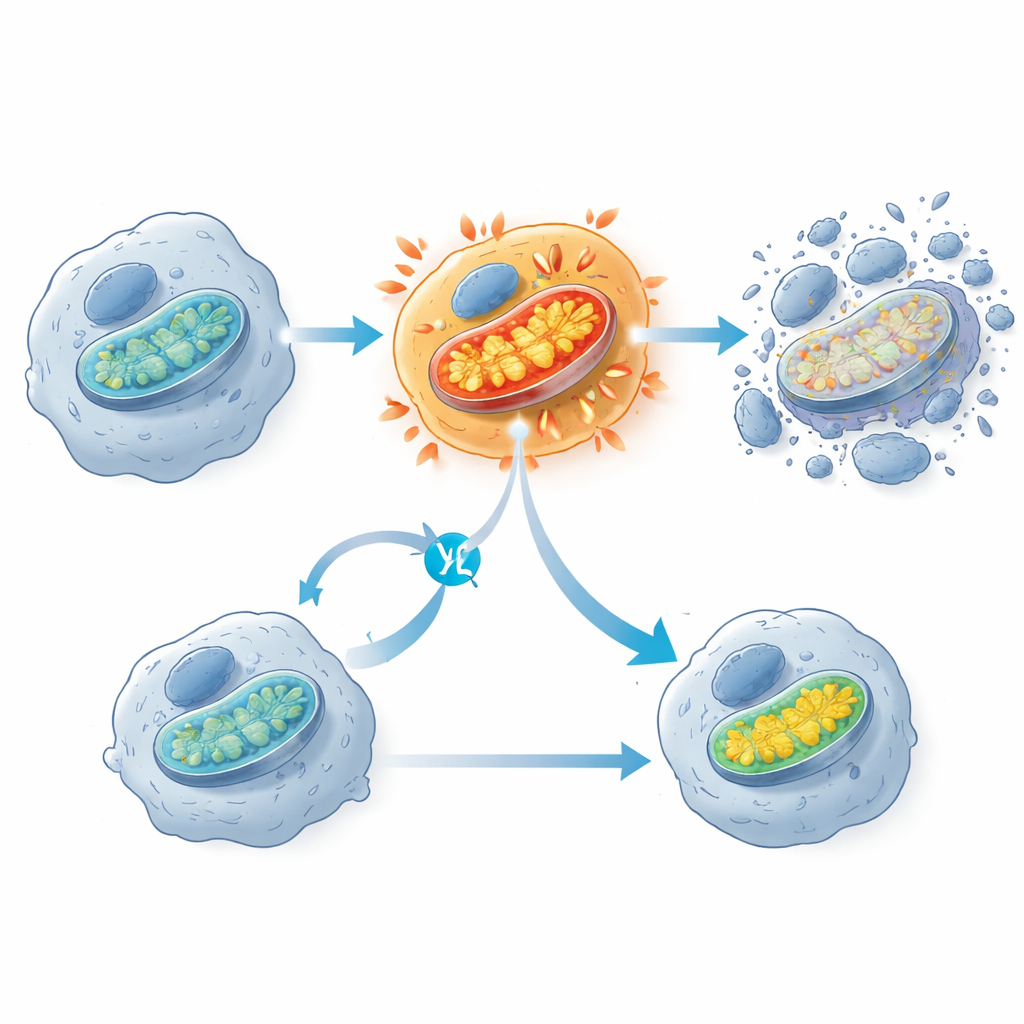
Uma descoberta marcante foi que os inibidores de KRAS G12C desencadeiam um surto precoce de atividade nas mitocôndrias, estruturas frequentemente descritas como as usinas de força da célula. Pouco depois da exposição ao fármaco, células sensíveis mostraram um pico no consumo de oxigênio e no potencial de membrana mitocondrial, seguido horas depois pela ativação de enzimas de morte celular. Células que resistiram ao tratamento tendiam a ter menos componentes mitocondriais e atividade gênica mitocondrial reduzida. Quando os pesquisadores bloquearam parcialmente a cadeia respiratória mitocondrial com outro fármaco, isso, na verdade, protegeu as células mutantes KRAS G12C da morte, sugerindo que esse súbito excesso de atividade mitocondrial é um passo chave que leva as células além do ponto de não retorno. A equipe também observou sinais de dano oxidativo a lipídios nas membranas celulares, mas bloquear esse processo não impediu a morte celular, indicando que se trata de um efeito colateral e não do gatilho principal.
Revelando rotas de escape ocultas e pares mais eficazes
Porque o GENEVA perfila milhares de células sobreviventes, ele consegue destacar genes e vias que são ativados especificamente em células tolerantes ao fármaco com KRAS G12C. O estudo apontou várias dessas rotas, incluindo sinalização via mTOR, enzimas que alteram o empacotamento do DNA e programas ligados a mudanças na forma e movimento celular conhecidas como transição epitélio–mesênquima (EMT). Muitas dessas características apareceram de forma mais pronunciada em tumores crescentes em camundongos, onde o microambiente tecidual ao redor está presente. Guiada por esses sinais, a equipe testou tratamentos combinados. Parear um inibidor de KRAS G12C com um inibidor de mTOR ou com um bloqueador de TGF-β (um indutor de EMT) produziu um encolhimento tumoral mais forte e duradouro em camundongos do que qualquer droga isolada.
Das células individuais a terapias de precisão mais inteligentes
Em termos simples, este trabalho mostra que a forma como uma célula cancerosa gerencia sua energia e sua morfologia pode determinar se um medicamento direcionado a KRAS a curará ou apenas a retardará. A plataforma GENEVA torna possível observar essas decisões se desenrolando em muitos tipos e condições tumorais ao mesmo tempo, revelando pontos fracos e rotas de escape comuns. Ao identificar que um “surto de energia” mitocondrial ajuda a matar células mutantes KRAS G12C, e que vias como mTOR e EMT permitem que algumas células escapem, o estudo aponta combinações de medicamentos concretas que podem prolongar as respostas em pacientes. Mais amplamente, o GENEVA oferece uma maneira de testar futuros fármacos contra o câncer em modelos realistas e geneticamente diversos muito antes de ensaios clínicos, aumentando as chances de que terapias de precisão funcionem para mais pessoas.
Citação: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Palavras-chave: inibidores de KRAS G12C, heterogeneidade tumoral, metabolismo mitocondrial, resistência a medicamentos, terapia combinada contra o câncer