Clear Sky Science · sv
GENEVA-plattformen modellerar tumörmosaik för att avslöja variationer i svar på KRAS-hämmare och identifiera förbättrade läkemedelskombinationer
Varför detta spelar roll för framtida cancerbehandlingar
Målinriktade cancerläkemedel utformas för att angripa specifika genetiska svagheter i tumörer, men patienter med till synes likartade cancerformer kan svara mycket olika. Denna artikel presenterar GENEVA, en ny experimentell plattform som återskapar den verkliga mångfalden i laboratoriet och hos möss, för att sedan följa hur tusentals enskilda cancerceller svarar på behandling över tid. Genom detta avslöjar forskarna varför vissa celler dör, varför andra överlever och hur man väljer smartare läkemedelskombinationer som kan hindra cancer från att komma tillbaka.
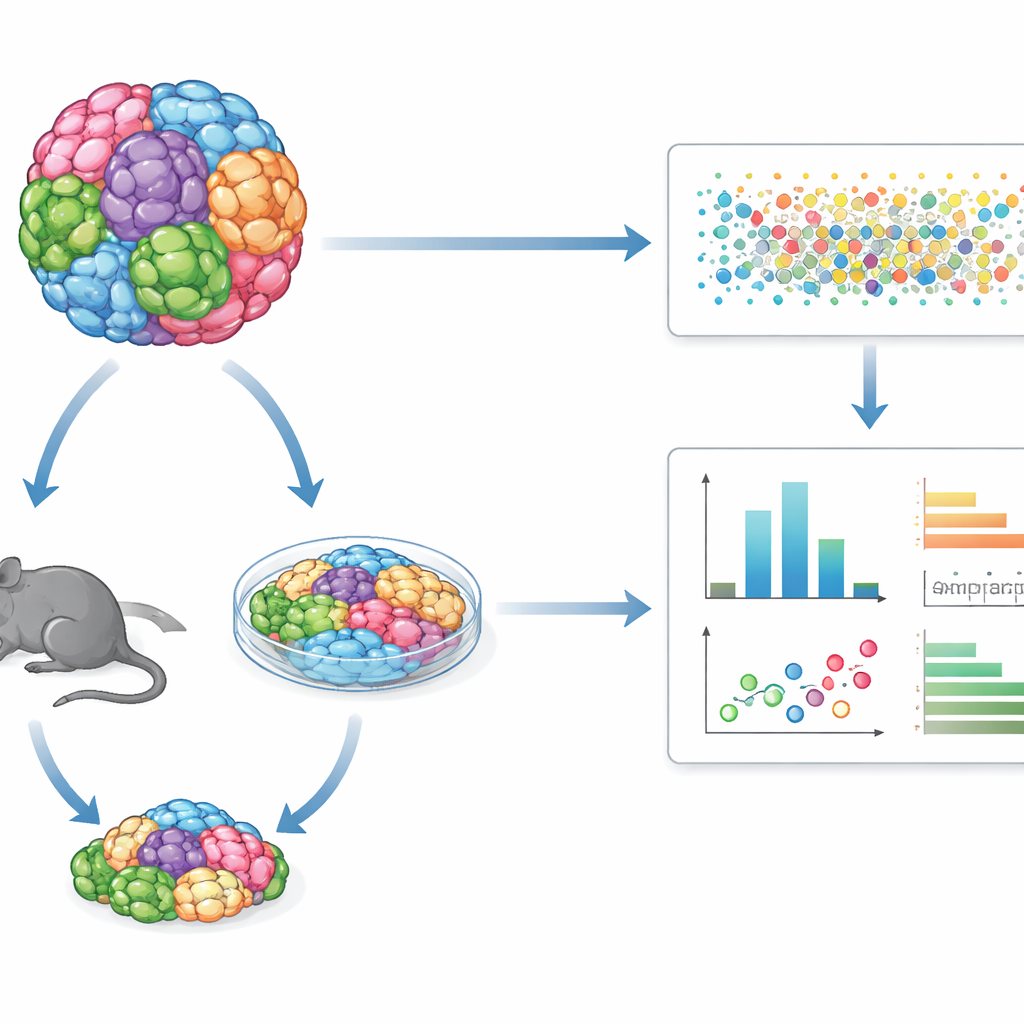
Många tumörtyper i ett och samma test
I stället för att studera en cancercellinje åt gången blandar GENEVA flera dussin genetiskt olika humana cancercellinjer eller tumörprover från patienter till en enskild ”mosaik” odling eller tumör. Dessa blandade populationer odlas antingen i tredimensionella laboratorieodlingar eller som tumörer i möss. Efter behandling med ett läkemedel använder teamet enkelcells-RNA-sekvensering och genetiska streckkoder för att läsa av, cell för cell, vilken genetisk bakgrund varje cell kommer från och vilket molekylärt tillstånd den befinner sig i. Detta låter dem mäta inte bara hur många celler som överlever, utan hur deras interna program förändras, vilket blottlägger mönster av känslighet och resistens över många tumörtyper i ett enda experiment.
Undersöker en ny klass KRAS-blockerande läkemedel
För att demonstrera GENEVA:s potential fokuserade forskarna på en nyligen godkänd grupp läkemedel som blockerar en cancerdrivande mutation kallad KRAS G12C. Dessa läkemedel har gett verklig nytta för vissa personer med lung- och andra cancerformer, men svaren är ofta kortvariga. Med GENEVA poolade teamet KRAS-mutanta och icke-mutanta cellinjer och behandlade dem med flera olika KRAS G12C-hämmare i olika doser, både i odlingsskålar och i möss. Som förväntat var KRAS G12C-celler i allmänhet mer känsliga, men även inom den gruppen överlevde vissa celler eller cellinjer, vilket antyder dolda överlevnadsstrategier som standardanalyser skulle missa.
Kraftökning i cellens kraftverk
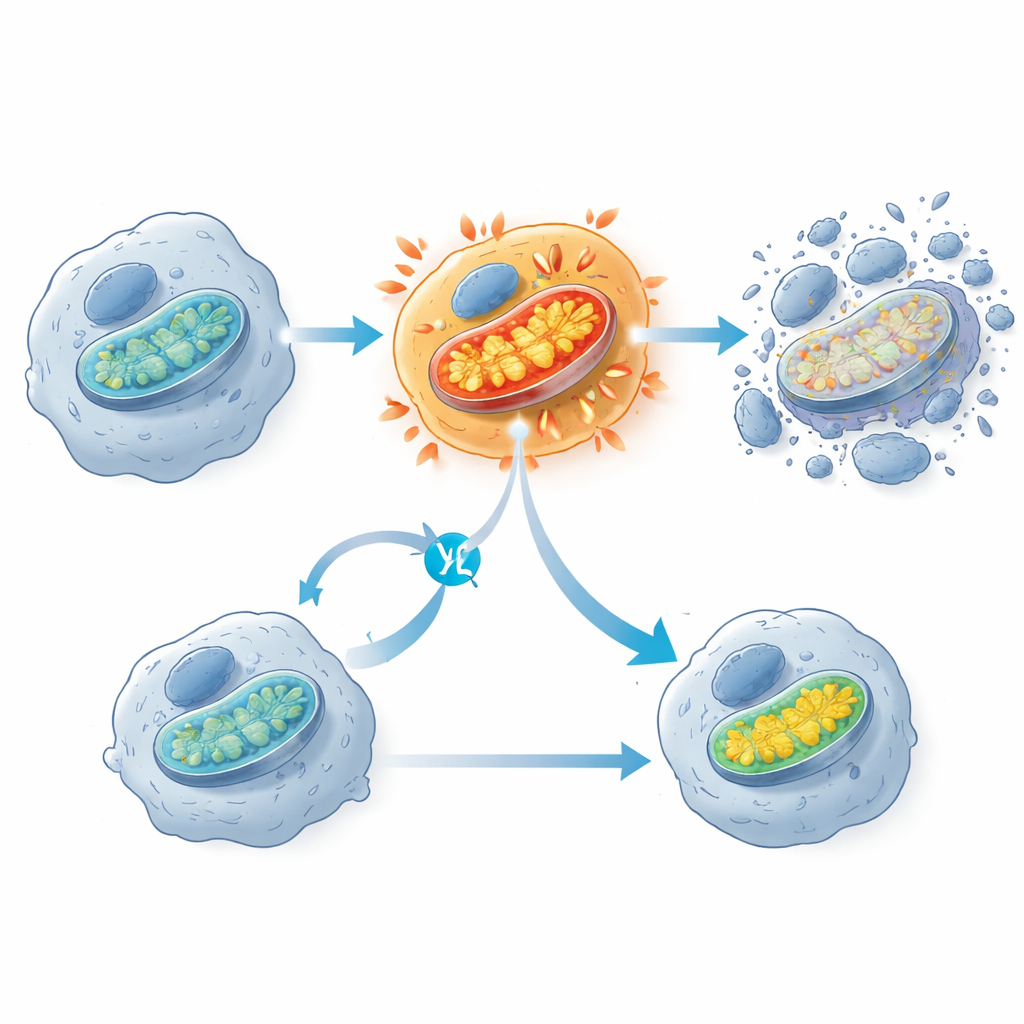
Ett iögonfallande fynd var att KRAS G12C-hämmare utlöser en tidig ökning av aktiviteten i mitokondrierna, de strukturer som ofta beskrivs som cellens kraftverk. Kort efter läkemedelsexponering visade känsliga cancerceller en topp i syreförbrukning och mitokondriell membranpotential, följt flera timmar senare av aktivering av cellens dödsenzym. Celler som klarade behandlingen tenderade att ha färre mitokondriella komponenter och dämpad aktivitet i mitokondriella gener. När forskarna delvis blockerade mitokondriens elektrontransportkedja med ett annat läkemedel skyddade det faktiskt KRAS G12C-mutanta celler från att dö, vilket tyder på att denna plötsliga mitokondriella överdrift är ett avgörande steg som pressar cellerna över gränsen. Teamet observerade också tecken på oxidativ skada på fetter i cellmembran, men att blockera denna process förhindrade inte celldöd, vilket indikerar att det är en bieffekt snarare än huvudmekanismen för cellernas undergång.
Avslöjar dolda flyktrutter och bättre kombinationer
Eftersom GENEVA profilerar tusentals överlevande celler kan plattformen belysa gener och signalvägar som är särskilt uppreglerade i läkemedelstoleranta KRAS G12C-celler. Studien pekade ut flera sådana vägar, inklusive signalering genom mTOR, enzymer som förändrar DNA-paketering, och program kopplade till förändringar i cellform och rörelse kända som epitelial–mesenkymal transition (EMT). Många av dessa egenskaper framträdde starkast i tumörer som växte i möss, där den omgivande vävnadens mikromiljö finns närvarande. Med ledning av dessa signaler testade teamet kombinationsbehandlingar. Att kombinera en KRAS G12C-hämmare med en mTOR-hämmare eller med en blockare av TGF-β (en drivkraft för EMT) gav starkare och mer varaktig tumörinvolution i möss än något enskilt läkemedel ensam.
Från enskilda celler till smartare precisionsbehandlingar
Enkelt uttryckt visar detta arbete att hur en cancercell hanterar sin energi och sin form kan avgöra om ett riktat KRAS-läkemedel kommer att bota den eller bara bromsa den. GENEVA-plattformen gör det möjligt att iaktta dessa beslut utvecklas över många tumörtyper och förhållanden samtidigt, och avslöjar gemensamma svaga punkter och flyktrutter. Genom att identifiera att en mitokondriell ”kraftökning” hjälper till att döda KRAS G12C-mutanta celler, och att vägar som mTOR och EMT låter vissa celler smita undan, pekar studien på konkreta läkemedelskombinationer som kan förlänga svarstider hos patienter. Mer generellt erbjuder GENEVA ett sätt att testa framtida cancerläkemedel i realistiska, genetiskt mångfaldiga modeller långt innan kliniska prövningar, vilket ökar sannolikheten att precisionsbehandlingar fungerar för fler människor.
Citering: Yu, J.X., Suh, J.M., Popova, K.D. et al. The GENEVA platform models tumor mosaicism to reveal variations of responses to KRAS inhibitors and identify improved drug combinations. Nat Cancer 7, 522–537 (2026). https://doi.org/10.1038/s43018-026-01130-5
Nyckelord: KRAS G12C-hämmare, tumörheterogenitet, mitokondriell metabolism, läkemedelsresistens, kombinationsterapi mot cancer