Clear Sky Science · zh
统计晶体学揭示了SARS-CoV-2主蛋白酶中的一个变构网络
蛋白质形态变换如何助力冠状病毒酶的功能
导致COVID-19的病毒依赖一种名为主蛋白酶的分子机器,将长的病毒多肽链切割成可工作的片段。已有药物针对该酶,但科学家仍难以看清其微妙的内部运动如何控制酶何时开启或关闭。本研究利用超过一千个将酶“锁定”在晶体中的快照,揭示了分子远端区域如何与执行化学反应的核心部位进行通信——并展示了这种隐蔽通信如何被干扰。
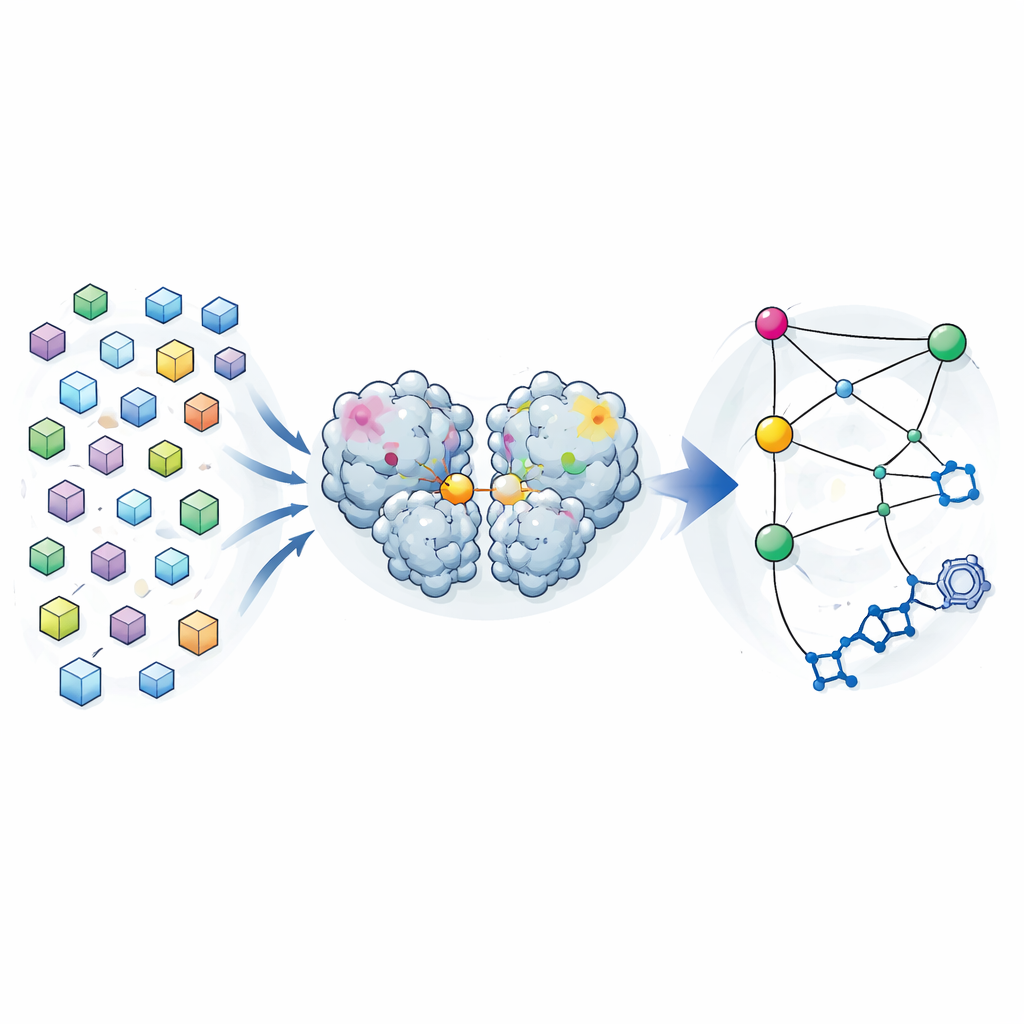
不是只有一个结构,而是许多快照
传统晶体学旨在提供蛋白质的单一“最佳”结构,这是许多晶体分子平均后的结果。作者反其道而行。在一次早期的药物筛选活动中,他们从近7000个SARS-CoV-2主蛋白酶的晶体收集了衍射数据。经过严格筛除含有结合化合物的晶体并施加严格的质量限制后,最终获得1146个高分辨率的酶单独结构。与其把这些结构间的小差异视为噪音,他们将其作为蛋白酶在仍接近其工作构象时能够采用的一组形态分布来分析。
在酶内部发现远距离关联
通过比较每个原子在不同结构间位置的变化,团队构建了一个协方差图谱——一种显示哪些区域倾向于一起移动的统计指纹。他们发现,这些基于晶体的相关性与通过长时程分子动力学模拟预测的溶液中酶的运动高度相似。这表明被冻结在晶体中的变异反映了酶在水溶液中真实探索的弯曲运动。当他们关注不同区域与活性位点(执行切割的口袋)之间的相关性时,发现了位于蛋白酶二聚化结构域的三个“热点”。这些热点距离活性位点较远,但似乎与催化口袋的变化紧密相连。
用定向突变测试这些热点
为了探查这些统计上识别出的位点是否真正控制功能,研究者通过将每个热点的单个氨基酸替换为丙氨酸来改变它们,这是常用来微调局部结构的方法。随后他们测量了每个突变体酶的二聚形成能力、对类底物片段的结合能力以及切割荧光测试肽的效率。有一个位置,N214,被确认为“变构热点”:该突变使二聚形成能力降低超过十倍,即便在存在足够二聚体的情况下,催化速率仍下降约一个数量级。突变体的高分辨率结构揭示了原因:通常稳定形成活性位点中“氧负离子孔”的关键环的局部氢键网络被破坏,该环部分失序并在化学反应中错位。
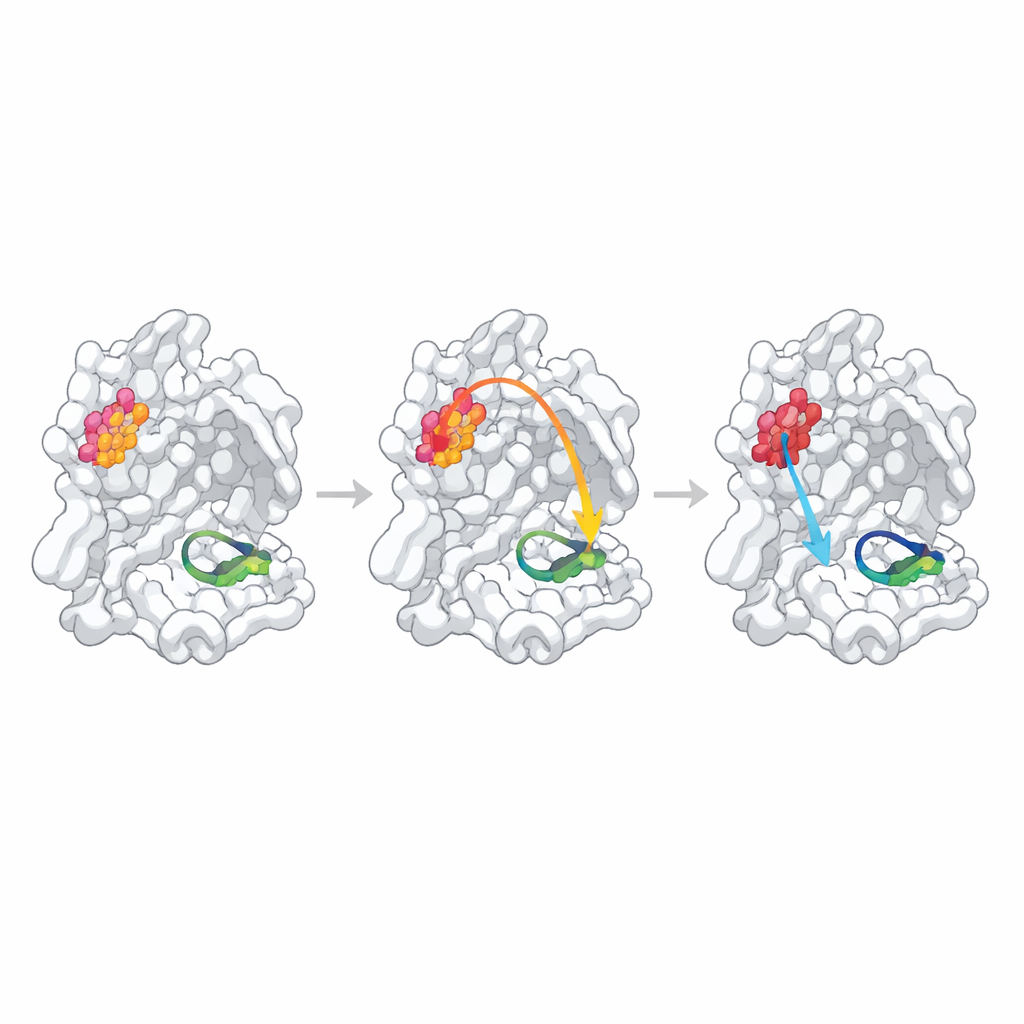
当预测的联系薄弱或被掩盖时
另外两个预测的热点表现不同。改变Q256(一个暴露于溶剂且表面上与二聚接触无明显关联的残基)仅引起活性轻微下降,这主要可归因于二聚形成略弱和对测试抑制剂结合能力略差。其晶体结构显示出一种全新的堆积排列,邻近分子填补了突变留下的空腔,使得难以区分是真正的内部通信还是晶体特异性的效应。第三个位点S284位于连接两个酶拷贝的小“拉链”中。与相关冠状病毒的序列比较所预期的那样,替换该残基几乎不影响结构或功能,表明此处的丙氨酸替换对测试预测通路而言过于温和。
晶体作为微小的力学实验
该工作一个有趣的副产物是,许多晶体间的结构差异可追溯于晶格——蛋白质与溶剂的重复排列——的微小变化。在操作过程中,晶体干燥程度略有差异时,晶胞会收缩或伸展,这些变化拉扯了相邻蛋白酶分子之间的接触点。这些力沿蛋白传播,产生了支撑协方差分析的结构多样性。换言之,每个晶体都像一个小型机械实验,沿不同方向轻微拉伸蛋白酶,从而在不使其解体的情况下揭示其弯曲方式。
这对生物学与药物设计有何意义
通过将数千个晶体结构视为一个统计群体而非单一答案,作者得以推断出一个将二聚界面残基N214与SARS-CoV-2主蛋白酶催化中心相连的变构网络。破坏该位点并非仅仅减少二聚体的数量;它还特异性地扰乱了活性环用于高效催化的几何构型。这一发现证实了酶活性受蛋白内部长程通信支配。更广泛地说,该研究展示了一种“统计晶体学”方法,其中对晶体的非受控、日常扰动——例如干燥程度的细微差异——成为绘制功能性运动图谱的资源。随着对其他蛋白产生类似数据集,这一策略可帮助发现新的调控位点,并指导设计不仅通过堵塞活性位点而是通过重接内部“对话”来发挥作用的药物。
引用: Creon, A., Scheer, T.E.S., Reinke, P. et al. Statistical crystallography reveals an allosteric network in SARS-CoV-2 Mpro. Commun Biol 9, 602 (2026). https://doi.org/10.1038/s42003-026-10127-w
关键词: SARS-CoV-2 主蛋白酶, 变构调节, 蛋白质动力学, 晶体学, 药物发现