Clear Sky Science · ar
علم البلورات الإحصائي يكشف شبكة كلوسترية في إنزيم Mpro الخاص بـ SARS-CoV-2
كيف تساعد تغيُّرات شكل البروتين إنزيمًا لفيروس كورونا على العمل
الفيروس المسبب لكوفيد-19 يعتمد على آلة جزيئية تُدعى البروتياز الرئيسي لقص سلاسل فيروسية طويلة إلى أجزاء عاملة. تستهدف الأدوية هذا الإنزيم بالفعل، لكن العلماء ما زالوا يواجهون صعوبة في رؤية كيف تتحكَّم حركاته الداخلية الدقيقة في تشغيله أو إيقافه. تستخدم هذه الدراسة أكثر من ألف لقطة للبروتياز محبوسة في بلورات لكشف كيفية تواصل أجزاء بعيدة من الجزيء مع مركز العمل الذي تتم فيه التفاعلات الكيميائية — وتظهر كيف يمكن تعطيل هذا التواصل الخفي.
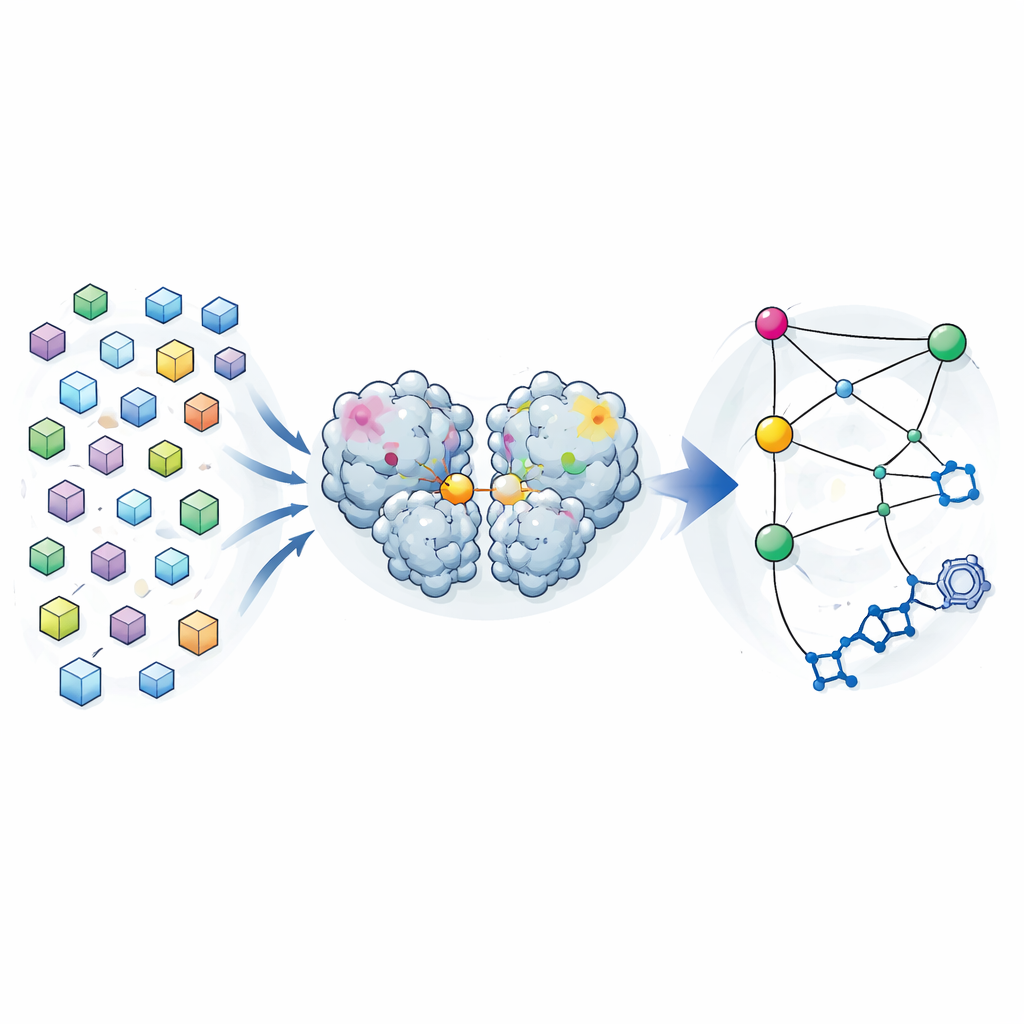
العديد من اللقطات بدلاً من بنية واحدة فقط
يسعى علم البلورات التقليدي إلى تقديم «أفضل» بنية مفردة للبروتين، مُعدَّلة على أساس متوسط مواقف العديد من الجزيئات في البلورة. قلب المؤلفون هذا المنطق. خلال حملة سابقة للبحث عن أدوية، جمعوا بيانات حيود من ما يقرب من 7000 بلورة لبروتياز SARS-CoV-2 الرئيسي. بعد تصفية دقيقة لاستبعاد أي بلورات احتوت على مركبات مرتبطة وفرض حدود جودة صارمة، تبقَّوا مع 1146 بنية عالية الدقة للإنزيم وحده. وبدلاً من اعتبار الاختلافات الصغيرة بين هذه الهياكل مجرد ضوضاء، حللوها كتوزيع من الأشكال التي يمكن أن يتَّخذها البروتياز أثناء بقائه قريبًا من حالته العاملة.
اكتشاف اتصالات بعيدة المدى داخل الإنزيم
بمقارنة كيفية تفاوت مواضع كل ذرة من بنية إلى أخرى، بنى الفريق خريطة تغاير — نوع من البصمة الإحصائية التي تُبيّن أي المناطق تميل إلى التحرك معًا. وجدوا أن هذه الترابطات المستخرجة من البلورات تشبه إلى حد كبير تلك التي توقَّعتها محاكاة ديناميكا جزيئية طويلة للبروتياز في المحلول. وهذا يشير إلى أن التباين المتجمِّد داخل البلورات يعكس حركات ثني حقيقية يستكشفها الإنزيم في الماء. عند تركيزهم على كيفية ارتباط مناطق مختلفة بموقع النشاط — الجيب الذي يقوم بالقص — كشفوا عن ثلاث «نقاط ساخنة» في مجال التزاوج الثنائي للبروتياز، الجزء الذي يساعد نسختين من الإنزيم على الاقتران. بدا أن التغيرات في هذه النقاط الساخنة، البعيدة عن موقع النشاط، مرتبطة ارتباطًا وثيقًا بتغيرات في الجيب التحفيزي.
اختبار النقاط الساخنة بتغييرات مستهدفة
لاختبار ما إذا كانت هذه المواقع المحددة إحصائيًا تتحكم بالفعل في الوظيفة، غيَّر الباحثون كل نقطة ساخنة باستبدال حمض أميني واحد بالألانين، وهي طريقة معيارية لتحفيز تعديل محلي في البنية. ثم قيَّموا قدرة كل متحوِّر من البروتياز على تشكيل أزواج ثنائية، وارتباطه بجزيء شبيه بالركيزة، وقدرته على قص ببتيد اختبار فلوري. تصرَّف موضع واحد، N214، كـ «نقطة ساخنة كلوسترية» مؤكدة: أضعف الطفرة تشكيل الأزواج بأكثر من عشرة أضعاف وحتى عندما كانت الأزواج كافية، انخفض معدل الحفزية بنحو ترتيب من الحجم. أظهرت هياكل الدقة العالية للمتحوِّر السبب: انكسر نظام الروابط الهيدروجينية المحلي الذي كان يستقرر حلقة حرجة تشكِّل «جوف الأكسانيون» في موقع النشاط، وأصبحت تلك الحلقة جزئيًا غير مرتبة ومخطئة المحاذاة للعمل الكيميائي.
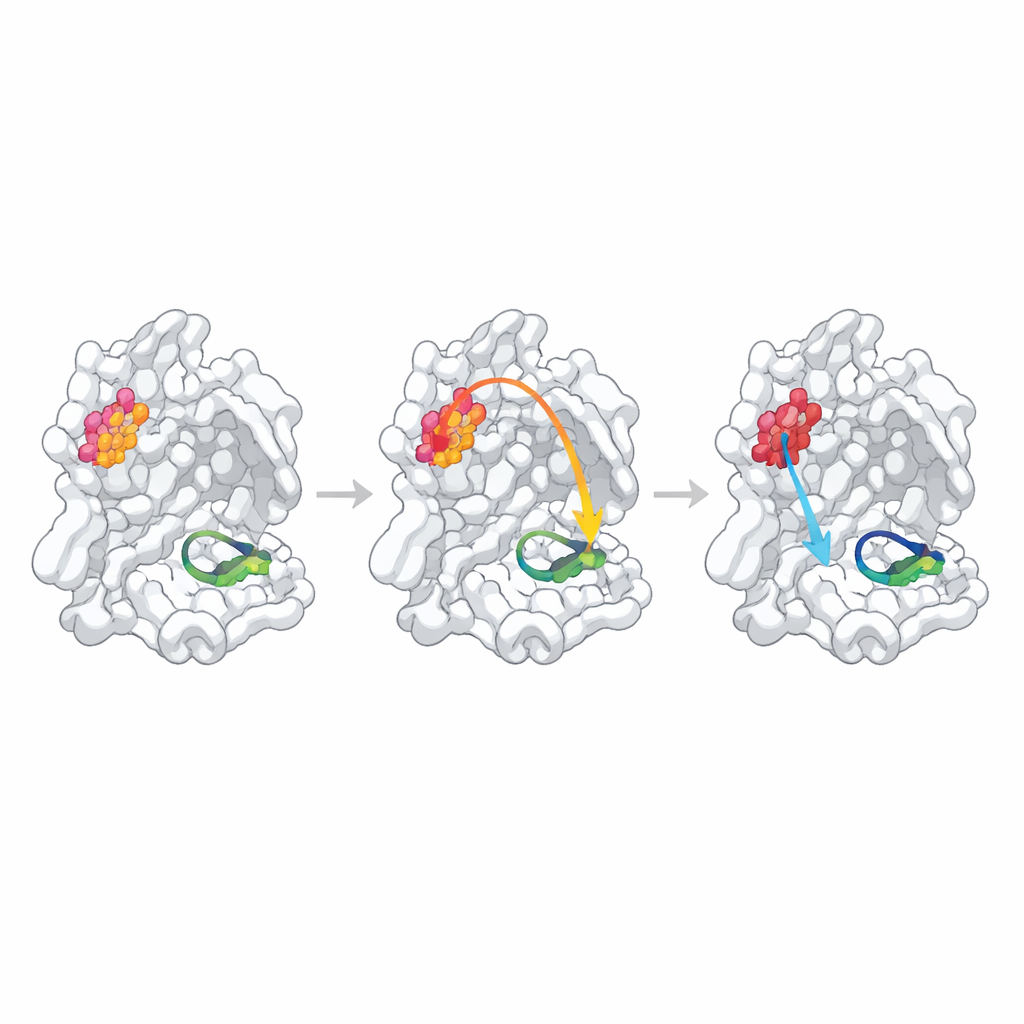
عندما تكون الروابط المتوقعة ضعيفة أو مخفية
تصرَّفت النقطتان الساخنتان الأخريان بشكل مختلف. أدى تغيير Q256، بقاعدة عرضة للمذيب وغير متورطة بوضوح في اتصالات التزاوج الثنائي، إلى انخفاض طفيف فقط في النشاط يمكن تفسيره في الغالب بضعف طفيف في تشكيل الأزواج وضعف طفيف في ارتباط مثبط الاختبار. كشفت بنية بلورتها عن ترتيب تعبئٍ جديد تمامًا حيث ملأت الجزيئات المجاورة الفراغ الناتج عن الطفرة، مما جعل من الصعب التمييز بين التواصل الداخلي الحقيقي وتأثيرات خاصة بالبلورة. الموقع الثالث، S284، يقع في «سحّاب» صغير يربط النسختين من الإنزيم. كما كان متوقعًا من مقارنات التتابع مع فيروسات كورونا ذات صلة، لم يحدث لاستبدال هذا البقايا تأثير تقريبًا على البنية أو الوظيفة، مما يشير إلى أن استبدال الألانين هنا كان تعديلًا لطيفًا جدًا لاختبار المسار المتوقع.
البلورات كتجارب قوة دقيقة
نتيجة جانبية مثيرة للعمل هي أن العديد من الاختلافات الهيكلية بين البلورات عُزيت إلى تغيُّرات طفيفة في بلّورة البلورة — الترتيب المتكرر للبروتينات والمذيب. أثناء تجفيف البلورات بدرجات طفيفة مختلفة أثناء المعالجة، انكمشت أو امتدت خلايا الوحدة لديها، وكانت هذه التحولات تشد نقاط التماس بين جزيئات البروتياز المجاورة. انتشرت تلك القوى عبر البروتين، مولِّدةً التنوع البنيوي الذي دعَّم تحليل التغاير. بعبارة أخرى، عملت كل بلورة كتجربة ميكانيكية صغيرة، تشد البروتياز برفق على طول اتجاهات مختلفة وتكشف كيف ينثني دون أن يتفكك.
لماذا يهم هذا للأحياء وتصميم الأدوية
من خلال معاملة آلاف هياكل البلورات كسكان إحصائي بدلاً من إجابة واحدة، تمكن المؤلفون من استنتاج شبكة كلوسترية تربط بقايا واجهة التزاوج الثنائي، N214، بالمركز الحفزي للبروتياز الرئيسي لـ SARS-CoV-2. إن تعطيل هذا الموقع لا يقلل ببساطة من عدد الأزواج المتكوِّنة؛ بل يعبث تحديدًا بهندسة الحلقة الفعالة المطلوبة للحفزية الكفوءة. هذا يؤكد أن نشاط الإنزيم تحكمه اتصالات طويلة المدى عبر البروتين. وبشكل أوسع، تُبيّن الدراسة نهجًا لـ «علم البلورات الإحصائي» حيث تصبح الاضطرابات اليومية غير المسيطر عليها للبلورات — مثل اختلافات طفيفة في التجفيف — مورداً لرسم خرائط الحركات الوظيفية. ومع جمع مجموعات بيانات مماثلة لبروتينات أخرى، قد تساعد هذه الاستراتيجية في الكشف عن مواقع تنظيمية جديدة وتوجيه تصميم أدوية تعمل ليس فقط عن طريق سد مواقع النشاط، بل بإعادة توصيل المحادثات الداخلية التي تجعل البروتينات تعمل.
الاستشهاد: Creon, A., Scheer, T.E.S., Reinke, P. et al. Statistical crystallography reveals an allosteric network in SARS-CoV-2 Mpro. Commun Biol 9, 602 (2026). https://doi.org/10.1038/s42003-026-10127-w
الكلمات المفتاحية: البروتياز الرئيسي لـ SARS-CoV-2, كلوستيرية (تنظيم خارجي), ديناميكية البروتين, علم البلورات, اكتشاف الأدوية