Clear Sky Science · ja
統計結晶学が明らかにしたSARS-CoV-2 Mproのアロステリックネットワーク
タンパク質の形の変化がコロナウイルス酵素の働きを助ける仕組み
COVID-19の原因ウイルスは、長いウイルスポリペプチドを機能パーツに切断するために「主プロテアーゼ」と呼ばれる分子機械に依存しています。既にこの酵素を標的とする薬は存在しますが、その微妙な内部運動がいつオンまたはオフに切り替わるかをどう制御しているかは依然として分かりにくい。本研究は、結晶に閉じ込められたプロテアーゼの千を超えるスナップショットを用いて、分子の遠隔部位が化学反応の起こる活動中心とどのように会話しているかを明らかにし、この隠れた通信がどのように妨げられ得るかを示しています。
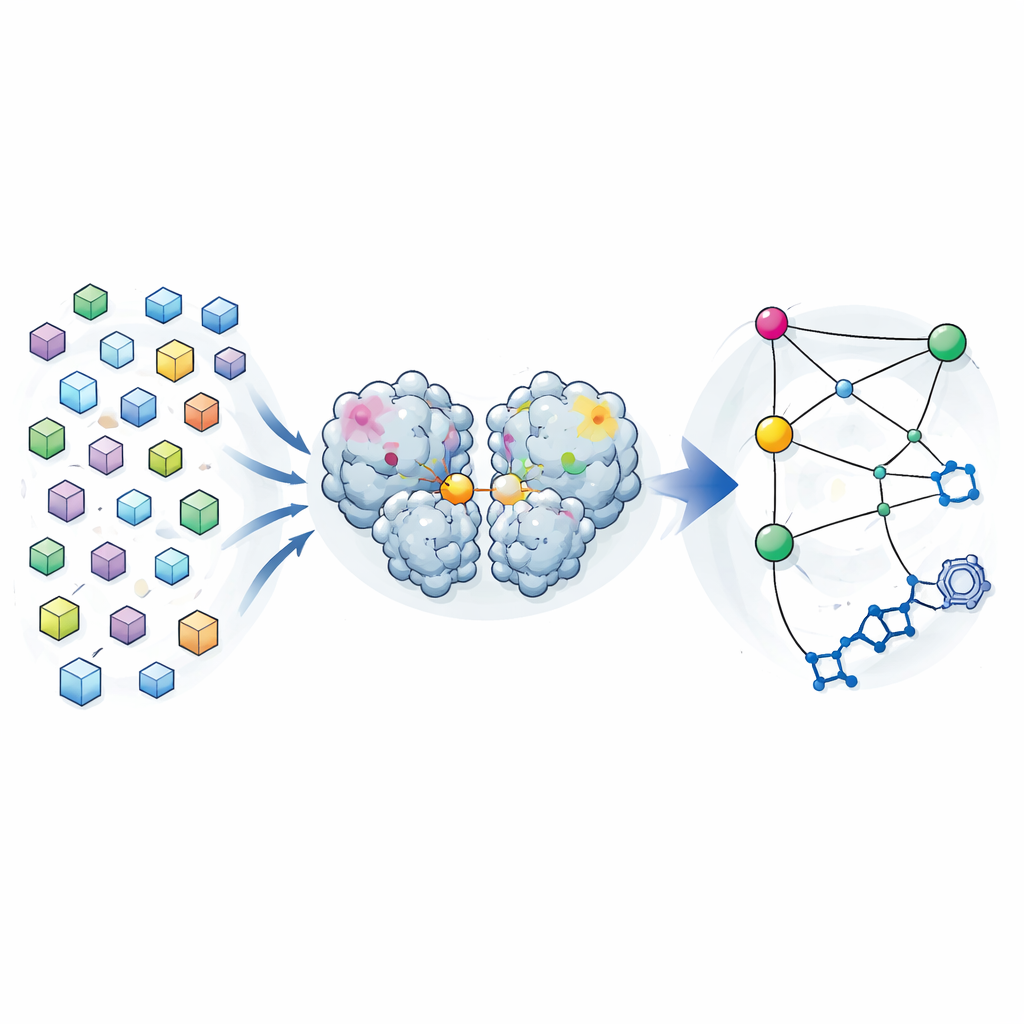
1つではなく多数のスナップショット
従来の結晶学は、結晶中の多数の分子を平均した「最良」の単一構造を与えることを目標にします。著者らはこの発想を逆転させました。以前の薬物探索キャンペーンで、彼らはSARS-CoV-2主プロテアーゼの約7000個の結晶から回折データを収集していました。結合化合物を含む結晶を慎重に除外し、厳格な品質基準を適用した結果、単独酵素の高解像度構造が1146件残りました。これらの構造間の小さな差異を単なるノイズとみなすのではなく、プロテアーゼが機能形に近いまま採り得る形状の分布として解析しました。
酵素内部の長距離結びつきを見つける
各原子の位置が構造ごとにどのように変動するかを比較することで、チームは共分散マップ—どの領域が一緒に動く傾向があるかを示す一種の統計的指紋—を作成しました。これらの結晶ベースの相関は、溶液中での長時間の分子動力学シミュレーションで予測されたものとよく似ていました。これは、結晶に凍結された変動が水中で酵素が探索する実際の柔軟な運動を反映していることを示唆します。異なる領域が触媒部位—切断を行うポケット—とどのように相関するかに焦点を当てると、酵素が二量体を形成するのを助ける二量化ドメインに三つの「ホットスポット」が存在することが明らかになりました。これらのホットスポットでの変化は、活性部位から遠く離れていても触媒ポケットの変化と密接に結びついているように見えました。
標的変化でホットスポットを試す
統計的に同定された部位が本当に機能を制御しているかを調べるために、研究者らは各ホットスポットで単一のアミノ酸をアラニンに置き換えるという標準的な手法で局所構造に小さな変更を加えました。次に各変異型プロテアーゼが二量体を形成する能力、基質に類似した断片への結合、蛍光試験ペプチドの切断能を測定しました。位置N214は確定した「アロステリックホットスポット」として振る舞いました:変異は二量体形成を10倍以上弱め、十分な二量体が存在しても触媒速度は約1桁低下しました。変異体の高解像度構造はその理由を示しています。通常は活性部位で「オキサニオンホール」を形成する重要なループを安定化する局所的な水素結合ネットワークが壊れ、そのループは部分的に無秩序になり化学反応に対して位置ずれを起こしていました。
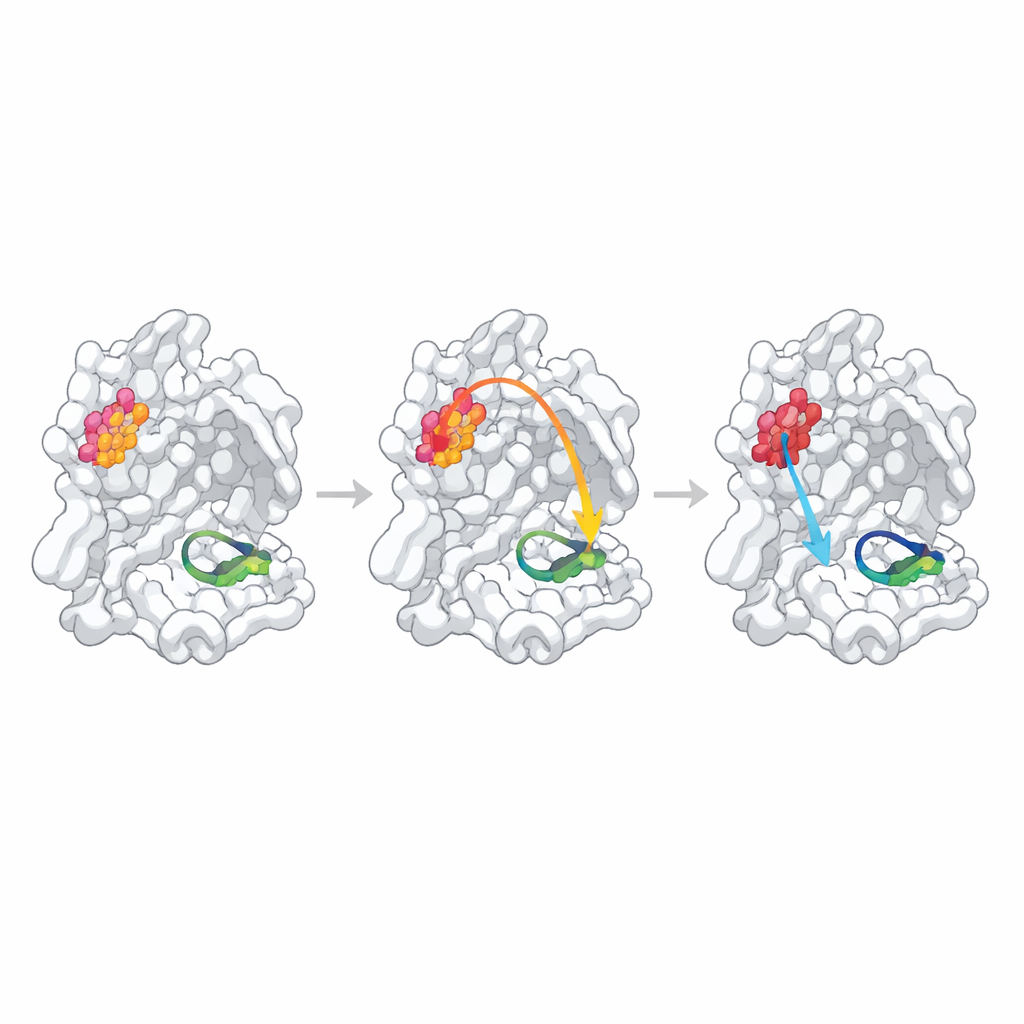
予測された結びつきが弱いか隠れている場合
他の二つの予測ホットスポットは異なる振る舞いを示しました。溶媒に露出し、二量体接触に明らかに関与していない残基Q256の置換は、活動のわずかな低下しかもたらさず、その多くは二量体形成の若干の弱化と試験阻害剤の結合のやや低下で説明できました。その結晶構造は、変異によって生じた空洞を隣接分子が埋めるまったく新しいパッキング配列を示し、内部の真のコミュニケーションと結晶特有の効果を区別することを難しくしました。三つ目の部位S284は二つの酵素コピーを橋渡しする小さな「ジッパー」に位置します。関連するコロナウイルスとの配列比較から予想されるように、この残基の置換は構造や機能にほとんど影響を与えませんでした。これは、この特定のアラニン置換が予測された経路を試すには穏やかすぎる摂動であったことを示しています。
結晶を小さな力学実験として見る
興味深い副産物として、多くの結晶間の構造差は結晶格子—タンパク質と溶媒の繰り返し配置—のわずかな変化に起因することがたどれました。結晶が取り扱い中にわずかに乾燥した度合いの違いにより、単位胞が縮んだり伸びたりし、これらの変化が隣接するプロテアーゼ分子間の接触点を引っ張りました。それらの力はタンパク質全体に波及し、共分散解析の基盤となる構造的多様性を生み出しました。言い換えれば、各結晶は小さな機械的実験として作用し、プロテアーゼを異なる方向に穏やかに引き伸ばすことで、崩壊することなくどのようにしなやかに変形するかを明らかにしました。
生物学と創薬にとっての意義
何千もの結晶構造を単一の答えとしてではなく統計的集団として扱うことで、著者らは二量体界面残基N214とSARS-CoV-2主プロテアーゼの触媒中心を結ぶアロステリックネットワークを推定できました。この部位を乱すことは単に二量体の数を減らすだけではなく、効率的な触媒に必要な活性ループの幾何学を特異的に乱します。これは酵素活性がタンパク質全体にわたる長距離の通信によって支配されていることを確認します。より広く言えば、本研究は、結晶のわずかな乾燥など日常的で制御されていない摂動を機能的運動のマッピングに利用する「統計結晶学」アプローチを示しています。類似のデータセットが他のタンパク質でも収集されれば、この戦略は新しい調節部位の発見や、活性部位に詰め物をするだけでなく、タンパク質内部の会話を書き換える薬の設計を導くのに役立つ可能性があります。
引用: Creon, A., Scheer, T.E.S., Reinke, P. et al. Statistical crystallography reveals an allosteric network in SARS-CoV-2 Mpro. Commun Biol 9, 602 (2026). https://doi.org/10.1038/s42003-026-10127-w
キーワード: SARS-CoV-2 主プロテアーゼ, アロステリー, タンパク質のダイナミクス, 結晶学, 創薬