Clear Sky Science · tr
İstatistiksel kristalografya, SARS-CoV-2 Mpro’da allosterik bir ağı ortaya koyuyor
Protein Şekil Değiştirmenin Bir Koronavirüs Enzimine Nasıl Yardımcı Olduğu
COVID-19’a neden olan virüs, uzun viral zincirleri çalışır parçalara kesmek için ana proteaz adı verilen bir moleküler makineye bağımlıdır. İlaçlar zaten bu enzimi hedefliyor, ancak bilim insanları hâlâ ince iç hareketlerin enzimin ne zaman açık veya kapalı olduğunu nasıl kontrol ettiğini görmekte zorlanıyor. Bu çalışma, proteazın kristallerde kilitlenmiş binin üzerindeki anlık görüntüsünü kullanarak molekülün uzak bölümlerinin kimyanın yapıldığı iş merkezine nasıl ileti gönderdiğini ortaya koyuyor — ve bu gizli iletişimin nasıl bozulabileceğini gösteriyor.
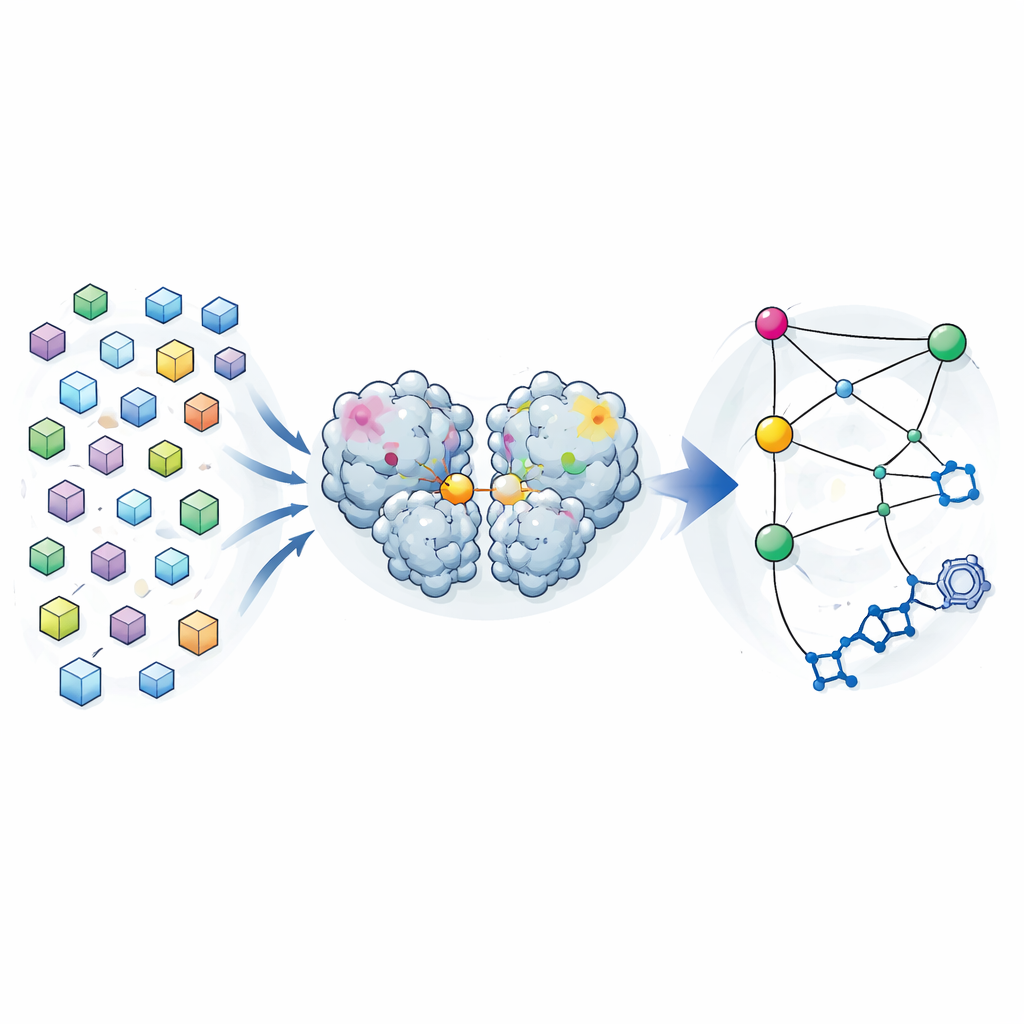
Sadece Bir Görüntü Yerine Birçok Anlık Görüntü
Geleneksel kristalografi, bir proteinin birçok molekülün ortalaması alınmış tek bir “en iyi” yapısını sağlamayı amaçlar. Yazarlar bu mantığı tersine çevirdi. Önceki bir ilaç arama kampanyası sırasında, SARS-CoV-2 ana proteazın neredeyse 7000 kristalinden difraksiyon verisi toplamışlardı. Bağlı bileşik içeren kristalleri dikkatle eler ve sıkı kalite sınırlarını uyguladıktan sonra geriye yalnızca enzimin yüksek çözünürlüklü 1146 yapısı kaldı. Bu yapılar arasındaki küçük farkları sıradan gürültü olarak ele almak yerine, proteazın çalışır formuna yakın kalırken benimseyebileceği şekillerin bir dağılımı olarak analiz ettiler.
Enzim İçinde Uzun Mesafe Bağlantılarını Bulmak
Her atomun konumunun yapıdan yapıya nasıl değiştiğini karşılaştırarak ekip bir kovaryans haritası — hangi bölgelerin birlikte hareket etme eğiliminde olduğunu gösteren bir tür istatistiksel parmak izi — oluşturdu. Bu kristal tabanlı korelasyonların, proteazın çözeltideki uzun moleküler dinamik simülasyonlarıyla öngörülenlere yakından benzediğini buldular. Bu, kristallere donmuş değişkenliğin enzimin suda keşfettiği gerçek esneme hareketlerini yansıttığını düşündürdü. Farklı bölgelerin aktif bölge — yani kesmeyi yapan cep — ile nasıl korele olduğunu incelediklerinde, proteazın dimerizasyon alanında üç “sıcak nokta” keşfettiler; bu bölüm enzimin iki kopyasının eşleşmesine yardımcı olur. Bu sıcak noktalardaki değişiklikler, aktif bölgeden uzakta olmasına rağmen katalitik cepteki değişikliklerle sıkı bağlantılı görünüyordu.
Sıcak Noktaları Hedefli Değişikliklerle Test Etmek
Bu istatistiksel olarak tanımlanmış bölgelerin gerçekten fonksiyonu kontrol edip etmediğini araştırmak için araştırmacılar her sıcak noktayı alanin ile tek bir amino asidi değiştirerek ayarladı; bu, yerel yapıyı hafifçe dürtecek standart bir yöntemdir. Ardından her mutant proteazın dimer oluşturma yeteneğini, bir substrat benzeri fragmanı bağlama kapasitesini ve floresan bir test peptidini kesme becerisini ölçtüler. Bir konum, N214, doğrulanmış bir “allosterik sıcak nokta” olarak davrandı: mutasyon dimer oluşumunu on kattan fazla zayıflatırken, yeterli dimer mevcut olsa bile katalitik hız yaklaşık bir mertebe düştü. Mutantın yüksek çözünürlüklü yapıları bunun nedenini gösterdi: aktif bölgede “oksianiyon deliği”ni oluşturan kritik bir halkayı normalde stabilize eden yerel hidrojen bağları ağı bozulmuş, ve bu halka kısmen düzensizleşip kimya için hizalanmamıştı.
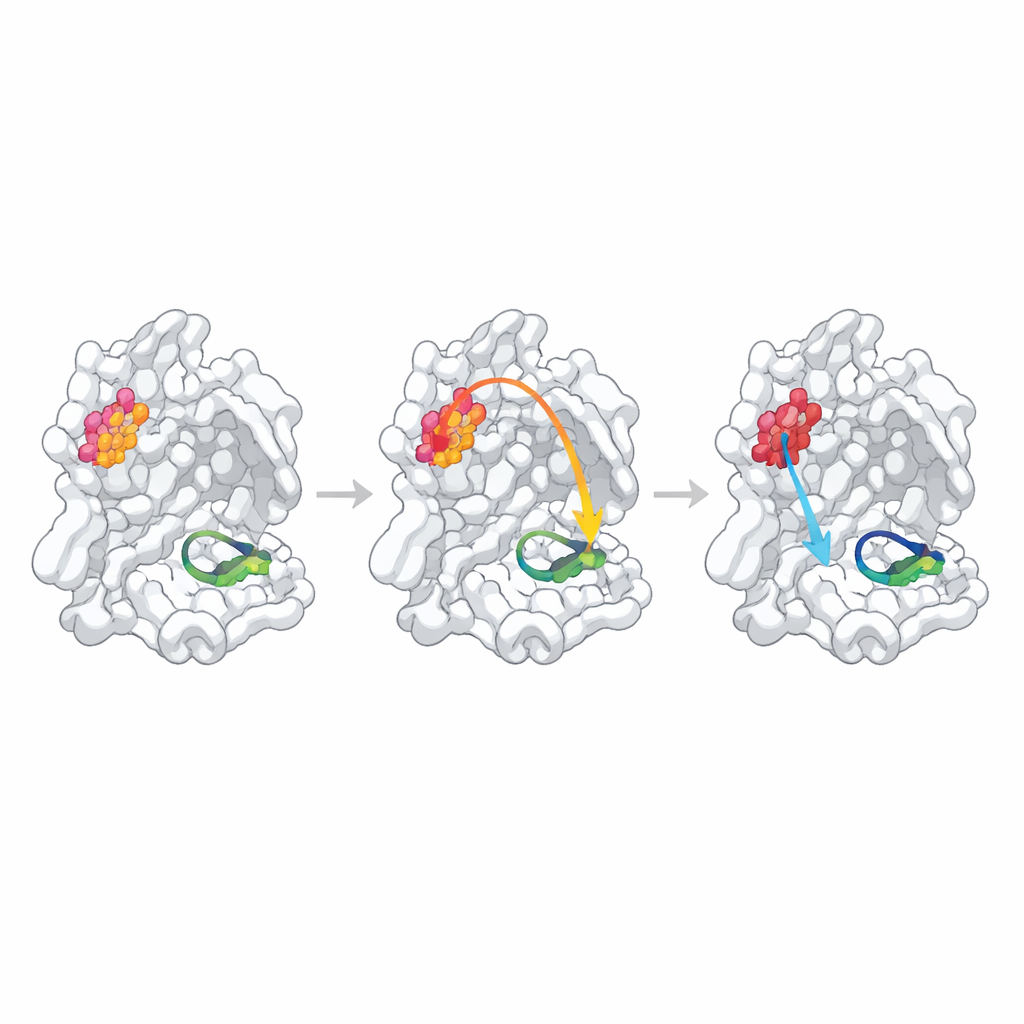
Öngörülen Bağlantılar Zayıf veya Gizlendiğinde
Diğer iki öngörülen sıcak nokta farklı davrandı. Dimer temaslarında açıkça rolü olmayan, çözücüye maruz bir kalıntı olan Q256’nın değiştirilmesi, esasen biraz zayıf dimer oluşumu ve biraz daha kötü test inhibitörü bağlanmasıyla büyük ölçüde açıklanabilen yalnızca ılımlı bir aktivite azalmasına yol açtı. Onun kristal yapısı, komşu moleküllerin mutasyonun bıraktığı boşluğu doldurduğu tamamen yeni bir paketleme düzenini ortaya koydu; bu da gerçek iç iletişimi kristal-spesifik etkilerden ayırmayı zorlaştırdı. Üçüncü bölge, S284, iki enzim kopyasını birleştiren küçük bir “fermuar” içinde yer alır. İlgili koronavirüslerle yapılan dizi karşılaştırmalarından beklendiği gibi, bu kalıntının yerine alanin konması yapı veya işlev üzerinde hemen hemen hiçbir etki göstermedi; bu da söz konusu alanin değişikliğinin öngörülen yolu test etmek için çok hafif bir bozulma olduğunu gösteriyor.
Kristaller Küçük Kuvvet Deneyleri Gibi
Çalışmanın ilginç yan sonuçlarından biri, kristaller arasındaki birçok yapısal farkın kristal örgüsündeki — proteinlerin ve çözücünün tekrar eden düzeni — küçük değişikliklere bağlanabilmesiydi. Kristaller işlem sırasında hafifçe farklı derecelerde kurudukça, birim hücreleri küçülüp genişledi ve bu kaymalar komşu proteaz molekülleri arasındaki temas noktalarını çekti. Bu kuvvetler protein boyunca dalga dalga yayılarak kovaryans analizinin dayandığı yapısal çeşitliliği üretti. Başka bir deyişle, her kristal küçük bir mekanik deney gibi davranarak proteazı farklı yönlere nazikçe geriyor ve parçalanmadan nasıl esnediğini ortaya koyuyordu.
Bu Neden Biyoloji ve İlaç Tasarımı İçin Önemli
Binin üzerinde kristal yapısını tek bir yanıt yerine istatistiksel bir popülasyon olarak ele alarak yazarlar, dimer ara yüzü kalıntısı N214’ü SARS-CoV-2 ana proteazının katalitik merkeziyle bağlayan bir allosterik ağı çıkarabildiler. Bu bölgenin bozulması yalnızca kaç dimer oluştuğunu azaltmaz; etkin kataliz için gerekli aktif halkanın geometrisini özel olarak karıştırır. Bu, enzimin aktivitesinin protein boyunca uzun menzilli iletişimle yönetildiğini doğrular. Daha genel olarak, çalışma, kristallerdeki kontrolsüz, günlük pertürbasyonların — örneğin kuruma farklılıkları gibi — işlevsel hareketleri eşlemeye yarayan bir kaynak haline geldiği “istatistiksel kristalografi” yaklaşımını gösterir. Benzer veri kümeleri diğer proteinler için toplandıkça, bu strateji yeni düzenleyici bölgeleri ortaya çıkarmaya ve sadece aktif bölgeleri tıkamakla kalmayıp proteinlerin iç konuşmalarını yeniden yapılandıran ilaçların tasarımına rehberlik etmeye yardımcı olabilir.
Atıf: Creon, A., Scheer, T.E.S., Reinke, P. et al. Statistical crystallography reveals an allosteric network in SARS-CoV-2 Mpro. Commun Biol 9, 602 (2026). https://doi.org/10.1038/s42003-026-10127-w
Anahtar kelimeler: SARS-CoV-2 ana proteaz, allosteri, protein dinamiği, kristalografi, ilaç keşfi